
【題目】今有常溫下兩種溶液:①0.1mol/LNH3·H2O溶液②0.1mol/LNH4Cl溶液
(1)溶液①的PH______7(填“>”、“<”或“=”),寫出NH3·H2O的電離方程式______________。
(2)溶液②呈________性(填“酸”、“堿”或“中”)。
(3)關于兩種溶液中c(NH4+)的大小敘述正確的是________(填序號)。
A.兩種溶液中c (NH4+)都等于0.lmol/L
B.兩種溶液中c (NH4+)都小于0.lmol/L
C.NH4Cl溶液中c(NH4+)小于NH3·H2O溶液中c(NH4+)
(4)將溶液中①逐滴加入溶液②中,當溶液pH=7時,c(NH4+)______ c(Cl一)(填“>”、“<”或“=”)。
【答案】 > NH3·H2O![]() NH4++OH- 酸 B =
NH4++OH- 酸 B =
【解析】考查弱電解質的電離和鹽類水解,以及電荷守恒,(1)NH3·H2O屬于弱堿,NH3·H2O![]() NH4++OH-,溶液顯堿性,即pH>7;(2)NH4Cl屬于強酸弱堿鹽,NH4++H2O
NH4++OH-,溶液顯堿性,即pH>7;(2)NH4Cl屬于強酸弱堿鹽,NH4++H2O![]() NH3·H2O+H+,溶液顯酸性;(3)A、NH3·H2O屬于弱堿,部分電離,因此NH4+濃度小于0.1mol·L-1,NH4Cl屬于強酸弱堿鹽,NH4+發生水解,因此NH4+濃度小于0.1mol·L-1,故A錯誤;B、根據選項A的分析,故B正確;C、NH3·H2O的電離和NH4+的水解都是微弱的,因此NH4Cl溶液中c(NH4+)大于NH3·H2O中NH4+的濃度,故C錯誤;(4)根據電荷守恒,c(NH4+)+c(H+)=c(Cl-)+c(OH-),因為溶液pH=7,即c(H+)=c(OH-),因此c(NH4+)=c(Cl-)。
NH3·H2O+H+,溶液顯酸性;(3)A、NH3·H2O屬于弱堿,部分電離,因此NH4+濃度小于0.1mol·L-1,NH4Cl屬于強酸弱堿鹽,NH4+發生水解,因此NH4+濃度小于0.1mol·L-1,故A錯誤;B、根據選項A的分析,故B正確;C、NH3·H2O的電離和NH4+的水解都是微弱的,因此NH4Cl溶液中c(NH4+)大于NH3·H2O中NH4+的濃度,故C錯誤;(4)根據電荷守恒,c(NH4+)+c(H+)=c(Cl-)+c(OH-),因為溶液pH=7,即c(H+)=c(OH-),因此c(NH4+)=c(Cl-)。


 應用題天天練四川大學出版社系列答案
應用題天天練四川大學出版社系列答案科目:高中化學 來源: 題型:
【題目】下列事實的解釋中錯誤的是
A. 在蔗糖中加入濃硫酸后出現發黑現象,說明濃硫酸具有脫水性
B. 濃硫酸和濃鹽酸混合可制氯化氫,說明濃硫酸具有吸水性
C. 常溫下能夠用鋁罐儲存濃硫酸,是因為濃硫酸的強氧化性可使鋁發生鈍化
D. 反應:C+2H2SO4(濃)![]() CO2↑+2H2O+2SO2↑中,H2SO4既體現酸性又體現了強氧化性
CO2↑+2H2O+2SO2↑中,H2SO4既體現酸性又體現了強氧化性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂被稱為“國防金屬”,鎂及其合金用途很廣,目前世界上60%的鎂從海水中提取。從海水中提取鎂的流程如下:
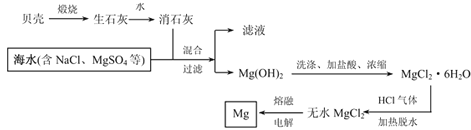
請根據上述流程圖和鎂及化合物的性質回答下列問題:
(1)用貝殼煅燒生石灰的反應方程式:________________
(2)氫氧化鎂溶于鹽酸的離子方程式為:_____________。
(3)簡述,由MgCl2·6H2O制無水MgCl2,加熱時通HCl氣體的主要原因是:___________。
(4)金屬鎂屬于(填寫下列編號):___________。
a.黑色金屬 b.有色金屬 c.輕金屬 d.重金屬 e.貴金屬
(5)Mg(OH)2煅燒可得熔點很高的MgO,MgO的電子式為:____________。
(6)MgCl2和AlCl3的熔點均較低,加MgO和Al2O3的熔點都很高。為什么冶煉金屬鎂是電解MgCl2,而冶煉金屬鋁則電解Al2O3:_______________。
(7)某MgCl2溶液的濃度為0.01mol/L,在該溶液中滴加NaOH溶液至pH=10,此時溶液中的Mg2+是否沉淀完全?_________(填“是”或“否”),此時c(Mg2+)=_________。
(已知:Ksp[Mg(OH)2]=1.8×10-11)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C是中學化學中常見的三種物質,它們之間的相互轉化關系如下(部分反應條件及產物略去):

(1)若A是一種金屬,C是淡黃色固體,則B的化學式為 _____________________,A→C反應的化學方程式為______________________。
(2)若A是一種非金屬,其常見單質為黑色固體,C是最重要的溫室氣體,則C的分子式是___________,B→C反應的化學方程式為______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】濃度為0.50mol·L-1的某金屬陽離子Mn+的溶液10.00mL,與0.40mol·L-1的NaOH溶液12.50mL完全反應,生成沉淀,則n等于
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能源短缺是人類社會面臨的重大問題。甲醇是一種可再生能源,具有廣泛的開犮和應用前景。工業上通過媒的氣化生成的CO和H2合成甲醇,反應原理為:CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
(1)在一容積可變的密閉容器中充有10 mol CO和20mol H2,在催化劑作用下發生反應生成甲醇。CO的平衡轉化率(a)與溫度(T)、壓強(p)的關系如圖1所示。
①合成甲醇的反應為_____(填“放熱”或“吸熱”)反應。判斷理由是_________。平衡常數KA_____KC(填“>”、“<”或“=”)。
②下列有關該反應的說法正確的是_____(填字母序號)。
A.當v(CO)生成=2v消耗(H2) 時該反應達到平衡狀態
B.其它條件不變,只改變CO和H2的投料量,該反應的焓變發生改變
C.在反應過程中混合氣體的密度和相對平均分子質量均不發生變化
D.使用催化劑可以減小反應的活化能
(2)下列措施可以提高甲醇產率的是________。
A.壓縮容器體積
B.恒容條件下充入He,使體系總壓強增大
C.將CH3OH (g)從體系中分離
D.恒壓條件下再充入10mol CO和20mol H2
(3)甲醇一一空氣燃料電池裝置如圖2所示。
①該電池甲電極的電極反應式為_________。
②若用此甲醇燃料電池電解200mL —定濃度NaCl與CuSO4的混合溶液(電極為惰性電極,不參與反應),電極產生氣體體積(標況下)與電解時間的關系圖如圖3所示,此溶液中硫酸銅的濃度為______mol/L。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com