
FeCl3在現代工業生產中應用廣泛。某化學研究性學習小組模擬工業流程制備無水FeCl3,再用副產品FeCl3溶液吸收有毒的H2S。
I、經查閱資料得知:無水FeCl3在空氣中易潮解,加熱易升華。他們設計了制備無水 FeCl3的實驗方案,裝置示意圖(加熱及夾持裝置略去)及操作步驟如下:
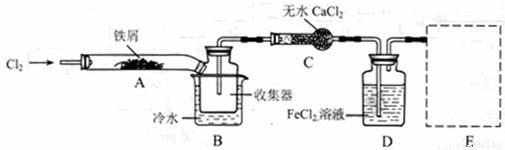
①檢驗裝置的氣密性;
②通入干燥的Cl2,趕盡裝置中的空氣;
③用酒精燈在鐵屑下方加熱至反應完成;
④……
⑤體系冷卻后,停止通入Cl2,并用干燥的H2趕盡Cl2,將收集器密封。
請回答下列問題:
(1)裝置A中反應的化學方程式為 。
(2)第③步加熱后,生成的煙狀FeCl3大部分進入收集器,少量沉積在反應管A右端。要使沉積的FeCl3進入收集器,第④步操作是 。
(3)操作步驟中,為防止FeCl3潮解所采取的措施有(填步驟序號) 。
(4)如果沒有裝置C的設計,會導致 。
(5)用離子方程式表示虛線框E中所增加裝置和試劑的作用: 。
(6)用裝置D中的副產品FeCl3溶液吸收H2S,得到單質硫,
請寫出反應的離子方程式: 。
Ⅱ、反應結束后,將收集器中所得固體完全溶于稀鹽酸,小組同學對所得溶液金屬陽離子的成分有三種觀點:①只有Fe3+;②只有Fe2+;③ 。
為探究溶液的組成,實驗如下:
|
實驗步驟 |
實驗現象 |
實驗結論及反應離子方程式 |
|
①取少量所得溶液于試管中,加入少量KSCN溶液。 |
|
說明:假設②不成立,假設①或③成立;的離子方程式是 。 |
|
②另取少量所得溶液于試管中,加入少量酸性 KMnO4溶液。 |
溶液紫紅色退去 |
說明: 。 |
綜合上述實驗分析,所得溶液中含有的金屬陽離子有 。
Ⅰ、(1)2Fe+3Cl2  2FeCl3(2分)
2FeCl3(2分)
(2)用酒精燈對沉積在A右端的FeCl3加熱(1分) (3)②⑤(2分)
(4)D裝置中水揮發到接受器,使FeCl3潮解(2分)
(5)Cl2+2OH-=Cl-+ClO-+H2O (2分)
(6)2Fe3++2H2S=2Fe2++2 H++S↓(2分)
Ⅱ、③既有Fe3+又有Fe2+(1分)
|
實驗步驟 |
實驗現象 |
實驗結論及反應離子方程式 |
|
|
溶液中出現紅色。(1分) |
Fe3++3SCN-= Fe(SCN)3。(2分) |
|
|
|
假設②或③成立 |
Fe3+、Fe2+(1分)
【解析】
試題分析:(1)裝置A中Fe與Cl2反應生成FeCl3,注意條件和配平可得2Fe+3Cl2  2FeCl3。
2FeCl3。
(2)要使沉積的FeCl3進入收集器,根據FeCl3加熱易升華的性質,第④的操作應該是:在沉積的的FeCl3固體下方加熱。
(3)裝置干燥,通入的氣體干燥均可防止其潮解,故步驟中②⑤合題意。
(4)裝置C中CaCl2具有吸水性,可把D中揮發出的水分吸收,如果沒有裝置C,D裝置中水揮發到接受器,使FeCl3潮解。
(5)虛線框E中盛放試劑為NaOH溶液,作用為吸收尾氣中的Cl2,所以離子方程式為:Cl2+2OH-=Cl-+ClO-+H2O。
(6)Fe3+具有氧化性,把H2S氧化為S,可寫出離子方程式為:2Fe3++2H2S=2Fe2++2 H++S↓。
Ⅱ、根據①②可得③觀點為既有Fe3+又有Fe2+;假設②不成立,假設①或③成立,說明溶液含有Fe3+,加入少量KSCN溶液,發生絡合反應生成Fe(SCN)3,使溶液變為紅色,離子方程式為:Fe3++3SCN-= Fe(SCN)3;加入少量酸性 KMnO4溶液,紫紅色退去,說明溶液含有Fe2+,則假設②或③成立,所以溶液中含有的金屬陽離子為Fe2+、Fe3+。
考點:本題考查化學方程式和離子方程式的書寫、離子的推斷、試劑與裝置的作用、實驗方案的分析。


科目:高中化學 來源: 題型:閱讀理解
| ||
| ||
查看答案和解析>>
科目:高中化學 來源:天津 題型:問答題
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
FeCl3在現代工業生產中應用廣泛。某化學研究性學習小組模擬工業生產流程制備無水FeCl3,再用副產品FeCl3溶液吸收有毒的H2S。
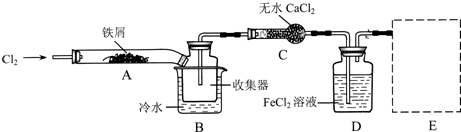
I.經查閱資料得知:無水FeCl3在空氣中易潮解,加熱易升華。他們設計了制備無水FeCl3的實驗方案,裝置示意圖(加熱及夾持裝置略去)及操作步驟如下:

①檢查裝置的氣密性;
②通入干燥的Cl2,趕盡裝置中的空氣;
③用酒精燈在鐵屑下方加熱至反應完成
④.。。。。。。。。
⑤體系冷卻后,停止通入Cl2,并用干燥的N2趕盡Cl2,將收集器密封
請回答下列問題:
(1) 裝置A中反應的化學方程式為——————
(2) 第③步加熱后,生成的煙狀FeCl3大部分進入收集器,少量沉積在反應管A的右端。要使沉積得FeCl3進入收集器,第④步操作是——————
(3) 操作步驟中,為防止FeCl3潮解所采取的措施有(填步驟序號)——
(4) 裝置B中的冷水作用為——————;裝置C的名稱為————;裝置D中FeCl2全部反應完后,因為失去吸收Cl2的作用而失效,寫出檢驗FeCl2是否失效的試劑:——
(5) 在虛線框內畫出尾氣吸收裝置E并注明試劑
II.該組同學用裝置D中的副產品FeCl3溶液吸收H2S,得到單質硫;過濾后,再以石墨為電極,在一定條件下電解濾液。
(6) FeCl3與H2S反應的離子方程式為——————————————————
(7) 電解池中H+再陰極放電產生H2,陽極的電極反應為————————
(8) 綜合分析實驗II的兩個反應,可知該實驗有兩個顯著優點:
①H2S的原子利用率100%;②——————————————————
查看答案和解析>>
科目:高中化學 來源:2013年全國普通高等學校招生統一考試理科綜合能力測試化學(天津卷帶解析) 題型:實驗題
FeCl3在現代工業生產中應用廣泛。某化學研究性學習小組模擬工業生產流程制備無水FeCl3,再用副產品FeCl3溶液吸收有毒的H2S。
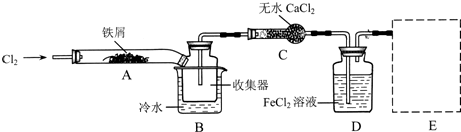
Ⅰ.經查閱資料得知:無水FeCl3在空氣中易潮解,加熱易升華。他們設計了制備無水FeCl3的實驗方案,裝置示意圖(加熱及夾持裝置略去)及操作步驟如下:
①檢查裝置的氣密性;②通入干燥的Cl2,趕盡裝置中的空氣;③用酒精燈在鐵屑下方加熱至反應完成;④…… ⑤體系冷卻后,停止通入Cl2,并用干燥的N2趕盡Cl2,將收集器密封。
請回答下列問題:
(1)裝置A中反應的化學方程式為 。
(2)第③步加熱后,生成的煙狀FeCl3大部分進入收集器,少量沉積在反應管A的右端。要使沉積得FeCl3進入收集器,第④步操作是 。
(3)操作步驟中,為防止FeCl3潮解所采取的措施有(填步驟序號) 。
(4)裝置B中的冷水作用為 ;裝置C的名稱為 ;裝置D中FeCl2全部反應完后,因為失去吸收Cl2的作用而失效,寫出檢驗FeCl2是否失效的試劑: 。
(5)在虛線框內畫出尾氣吸收裝置E并注明試劑
Ⅱ.該組同學用裝置D中的副產品FeCl3溶液吸收H2S,得到單質硫;過濾后,再以石墨為電極,在一定條件下電解濾液。
(6)FeCl3與H2S反應的離子方程式為 。
(7)電解池中H+在陰極放電產生H2,陽極的電極反應為 。
(8)綜合分析實驗Ⅱ的兩個反應,可知該實驗有兩個顯著優點:
①H2S的原子利用率100%;② 。
查看答案和解析>>
科目:高中化學 來源:2014屆福建省高三上學期第三次月考化學試卷(解析版 題型:實驗題
FeCl3在現代工業生產中應用廣泛。某化學研究性學習小組模擬工業流程制備無水FeCl3,再用副產品FeCl3溶液吸收有毒的H2S。
I、經查閱資料得知:無水FeCl3在空氣中易潮解,加熱易升華。他們設計了制備無水 FeCl3的實驗方案,裝置示意圖(加熱及夾持裝置略去)及操作步驟如下:

①檢驗裝置的氣密性;
②通入干燥的Cl2,趕盡裝置中的空氣;
③用酒精燈在鐵屑下方加熱至反應完成;
④……
⑤體系冷卻后,停止通入Cl2,并用干燥的H2趕盡Cl2,將收集器密封。
請回答下列問題:
(1)裝置A中反應的化學方程式為 。
(2)操作步驟中,為防止FeCl3潮解所采取的措施有(填步驟序號) 。
(3)如果沒有裝置C的設計,會導致
(4)用離子方程式表示虛線框E中所增加裝置和試劑的作用: 。
(5)用裝置D中的副產品FeCl3溶液吸收H2S,得到單質硫,請寫出反應的離子方程式: 。
Ⅱ、反應結束后,將收集器中所得固體完全溶于稀鹽酸,小組同學對所得溶液金屬陽離子的成分有三種觀點:①只有Fe3+;②只有Fe2+;③ 。
為探究溶液的組成,實驗如下:
|
實驗步驟 |
實驗現象 |
實驗結論及反應離子方程式 |
|
①取少量所得溶液于試管中,加入少量KSCN溶液。 |
_________________。 |
說明:假設②不成立,假設①或③成立;反應的離子方程式是_____________。 |
|
②另取少量所得溶液于試管中,加入少量酸性 KMnO4溶液。 |
溶液紫紅色退去 |
說明:________________________。 |
綜合上述實驗分析,所得溶液中含有的金屬陽離子有 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com