
| ||
| ||
| ||
| ||
|
| 12.8g |
| 14g |


 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案科目:高中化學 來源: 題型:閱讀理解
 (2013?閘北區二模)含有硫的化合物在工業生產中應用廣泛,回答下列問題:
(2013?閘北區二模)含有硫的化合物在工業生產中應用廣泛,回答下列問題:| 裝置 | A (試管+粉末) |
B | C |
| 反應前 | 42.0g | 75.0g | 140.0g |
| 反應后 | 37.0g | 79.0g | 140.5g |
| 高溫 |
| 高溫 |
查看答案和解析>>
科目:高中化學 來源:2012-2013學年上海市閘北區高三下學期二模化學試卷(解析版) 題型:計算題
含有硫的化合物在工業生產中應用廣泛,回答下列問題:
(1)黃銅礦是工業煉銅的主要原料,其主要成分為CuFeS2。
①測得某黃銅礦(CuFeS2)中含硫20%(質量分數),求該礦石含銅的質量分數。
②現有一種天然黃銅礦(含少量脈石),為了測定該黃銅礦的純度,某同學設計了如下實驗:稱取
研細的黃銅礦樣品1.150g,在空氣中進行煅燒,生成Cu、Fe3O4和SO2氣體,用100 mL滴有淀粉的
蒸餾水全部吸收SO2,然后取10mL吸收液,用0.05mol/L標準碘溶液進行滴定,用去標準碘溶液的體
積為20.00mL。求該黃銅礦的純度。
(2)將FeS和Fe2O3的混和物56.6 g,用足量稀H2SO4溶解后可得3.2 g硫,原混和物中FeS的質量。
(3)一定溫度下,硫酸銅受熱分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被堿石灰和氫氧
化鈉溶液吸收。利用下圖裝置加熱無水硫酸銅粉末直至完全分解。若無水硫酸銅粉末質量為10.0 g,
完全分解后,各裝置的質量變化關系如下表所示。
|
裝置 |
A(試管+粉末) |
B |
C |
|
反應前 |
42.0 g |
75.0 g |
140.0 g |
|
反應后 |
37.0 g |
79.0 g |
140.5 g |

請通過計算,推斷出該實驗條件下硫酸銅分解的化學方程式。
(4)硫化鈉是用于皮革的重要化學試劑,可用無水Na2SO4與炭粉在高溫下反應制得,化學方程式如下:
①Na2SO4
+ 4C Na2S + 4CO↑ ②Na2SO4
+ 4CO
Na2S + 4CO↑ ②Na2SO4
+ 4CO Na2S + 4CO2
Na2S + 4CO2
a.若在反應過程中,產生CO和CO2混合氣體為2mol,求生成Na2S的物質的量。
b.硫化鈉晶體放置在空氣中,會緩慢氧化成Na2SO3,甚至是Na2SO4,現將43.72g部分變質的硫化鈉樣品溶于水中,加入足量鹽酸后,過濾得4.8g沉淀和1.12L H2S 氣體(標準狀況,假設溶液中氣體全部逸出),在濾液中加入足量的BaCl2后過濾得2.33g沉淀,分析該硫化鈉樣品的成分及其物質的量。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 含有硫的化合物在工業生產中應用廣泛,回答下列問題:
含有硫的化合物在工業生產中應用廣泛,回答下列問題:| 裝置 | A (試管+粉末) | B | C |
| 反應前 | 42.0g | 75.0g | 140.0g |
| 反應后 | 37.0g | 79.0g | 140.5g |
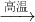 Na2S+4CO ②Na2SO4+4CO
Na2S+4CO ②Na2SO4+4CO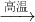 Na2S+4CO2
Na2S+4CO2查看答案和解析>>
科目:高中化學 來源:2013年上海市閘北區高考化學二模試卷(解析版) 題型:解答題
| 裝置 | A (試管+粉末) | B | C |
| 反應前 | 42.0g | 75.0g | 140.0g |
| 反應后 | 37.0g | 79.0g | 140.5g |
 Na2S+4CO ②Na2SO4+4CO
Na2S+4CO ②Na2SO4+4CO Na2S+4CO2
Na2S+4CO2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com