
【題目】乙炔(C2H2)氣體的燃燒熱為ΔH=-1299.6kJ·mol-1,分別寫出表示乙炔燃燒反應的熱化學方程式和表示乙炔燃燒熱的熱化學方程式____、____。
【答案】2C2H2(g)+ 5O2(g)=4CO2(g)+2H2O(l) ΔH=-2599.2kJ·mol-1 C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) ΔH=-1299.6kJ·mol-1
O2(g)=2CO2(g)+H2O(l) ΔH=-1299.6kJ·mol-1
【解析】
乙炔的燃燒熱(△H)為-1299.6kJ/mol,則1molC2H2(g)完全燃燒生成水和二氧化碳放出1366.8KJ的熱量。
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-QkJ·mol-1,由(C2H2)燃燒熱為ΔH=-1299.6 kJ·mol-1知Q=2599.2。表示燃燒反應的熱化學方程式為2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-2599.2 kJ·mol-1。表示燃燒熱的熱化學方程式中可燃物的化學計量數必為1,則表示燃燒熱的熱化學方程式為C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) ΔH=-1299.6 kJ·mol-1,
O2(g)=2CO2(g)+H2O(l) ΔH=-1299.6 kJ·mol-1,
故答案為:2C2H2(g)+ 5O2(g)=4CO2(g)+2H2O(l)ΔH=-2599.2kJ·mol-1;C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) ΔH=-1299.6kJ·mol-1。
O2(g)=2CO2(g)+H2O(l) ΔH=-1299.6kJ·mol-1。


科目:高中化學 來源: 題型:
【題目】鋁(熔點660℃)是一種應用廣泛的金屬,工業上用![]() (熔點2045℃)和冰晶石(
(熔點2045℃)和冰晶石(![]() )混合熔融后電解制得。請回答下列問題:
)混合熔融后電解制得。請回答下列問題:
(1)鋁屬于活潑金屬卻能在空氣中穩定存在,其原因是__________,冶金工業上常用金屬鋁作還原劑冶煉釩、鉻、錳等金屬,請寫出鋁與V2O5在高溫下反應的化學方程式:___________。
(2)將![]() 液和
液和![]() 溶液混合制取
溶液混合制取![]() 。該實驗用于盛裝NaF溶液的試劑瓶_________(填“能”或“不能”)用玻璃瓶,原因是_______。
。該實驗用于盛裝NaF溶液的試劑瓶_________(填“能”或“不能”)用玻璃瓶,原因是_______。
(3)下列關于鋁元素的敘述不正確的是__________(填序號)。
A.鋁是人類最早使用的金屬
B.鎂鋁合金既可完全溶于過量的鹽酸,又可完全溶于過量的NaOH溶液
C.氫氧化鋁是一種兩性氫氧化物,既能溶于鹽酸又能溶于NaOH溶液
D.鋁是人體必需的微量元素之一,因此在生活中人們應盡量使用鋁制炊具和餐具更有利于身體健康
(4)某工廠排放出有毒物質NOCl,它遇水就會生成![]() 。NOCl分子中各原子均滿足8電子穩定結構,則NOCl的電子式為_________,水源中的
。NOCl分子中各原子均滿足8電子穩定結構,則NOCl的電子式為_________,水源中的![]() 對人類健康會產生危害,為了降低水源中
對人類健康會產生危害,為了降低水源中![]() 的濃度,有研究人員建議在堿性條件下用鋁粉將
的濃度,有研究人員建議在堿性條件下用鋁粉將![]() 還原為N2,此時鋁主要以
還原為N2,此時鋁主要以![]() 的形式存在于溶液中,請寫出該反應的離子方程式:__________,當該反應轉移5mol電子時,產生的
的形式存在于溶液中,請寫出該反應的離子方程式:__________,當該反應轉移5mol電子時,產生的![]() 在標況下的體積約為_______L。
在標況下的體積約為_______L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現以0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1HCl溶液為例,討論強堿滴定強酸的情況,通過計算完成下表(已知:lg2=0.3,lg5=0.7。溶液混合時的體積變化忽略不計)。
加入NaOH溶液的體積V/mL | 0.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
剩余鹽酸溶液的體積V/mL | 20.00 | 2.00 | 0.20 | 0.02 | 0.00 | / | / | / | / |
過量NaOH溶液的體積V/mL | / | / | / | / | / | 0.02 | 0.20 | 2.00 | 20.00 |
pH | 1.00 | 2.28 | 3.30 | __ | 7.00 | 9.70 | __ | 11.70 | 12.50 |
(1)請利用表的數據繪制滴定曲線_____。
(2)如果初讀數和末讀數如圖所示,滴定液的用量為__mL。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知熱化學方程式:SO2(g)+![]() O2(g)
O2(g)![]() SO3(g) ΔH=-98.32 kJ/mol,在容器中充入2 mol SO2和1 mol O2充分反應,最終放出的熱量為( )
SO3(g) ΔH=-98.32 kJ/mol,在容器中充入2 mol SO2和1 mol O2充分反應,最終放出的熱量為( )
A.196.64 kJB.196.64 kJ/molC.<196.64 kJD.>196.64 kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】羰基硫(COS)與氫氣或與水在催化劑作用下的反應如下:
Ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g) △H1=-17kJ/mol;
H2S(g)+CO(g) △H1=-17kJ/mol;
Ⅱ.COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H2=-35kJ/mol。
H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列問題:
(1)兩個反應在熱力學上趨勢均不大,其原因是:________________。
(2)反應CO(g)+H2O(g)![]() H2(g)+CO2(g)的△H=_______。
H2(g)+CO2(g)的△H=_______。
(3)羰基硫、氫氣、水蒸氣共混體系初始投料比不變,提高羰基硫與水蒸氣反應的選擇性的關鍵因素是______。
(4)在充有催化劑的恒壓密閉容器中只進行反應Ⅰ![]() 設起始充入的n(H2):n(COS)=m,相同時間內測得COS轉化率與m和溫度(T)的關系如圖所示:
設起始充入的n(H2):n(COS)=m,相同時間內測得COS轉化率與m和溫度(T)的關系如圖所示:

①m1______m2(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 。
。
②溫度高于T0,COS轉化率減小的可能原因為:i有副應發生;ii______;iii______。
(5)在充有催化劑的恒壓密閉容器中進行反應Ⅱ.COS(g)與H2O(g)投料比分別為1:3和1:1,反應物的總物質的量相同時,COS(g)的平衡轉化率與溫度的關系曲線如圖所示:
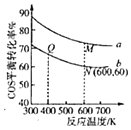
①M點對應的平衡常數______Q點![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ;
;
②N點對應的平衡混合氣中COS(g)物質的量分數為______;
③M點和Q點對應的平衡混合氣體的總物質的量之比為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨著世界工業經濟的發展、人口的劇增,全球能源緊張及世界氣候面臨越來越嚴重的問題,如何降低大氣中CO2的含量及有效地開發利用CO2引起了全世界的普遍重視。
(1)甲醇是一種可再生能源,具有開發和應用的廣闊前景,工業上可用如下方法合成甲醇:
方法一 CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
方法二 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
在25 ℃、101 kPa下,1g液態甲醇完全燃燒放熱22.68 kJ,寫出甲醇燃燒熱的熱化學方程式:_________________。
(2)金屬鈦冶煉過程中其中一步反應是將原料金紅石轉化:
TiO2(金紅石)+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
已知:C(s)+O2(g)=CO2(g) ΔH=﹣393.5kJ/mol
2CO(g)+O2(g)=2CO2(g) ΔH=﹣566 kJ/mol
TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=+141 kJ/mol
則TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______________________。
(3)臭氧可用于凈化空氣,飲用水消毒,處理工業廢物和作為漂白劑。臭氧幾乎可與除鉑、金、銥、氟以外的所有單質反應如6Ag(s)+O3(g)=3Ag2O(s) ΔH=﹣235.8 kJ/mol,
已知:2Ag2O(s)=4Ag(s)+O2(g) ΔH= +62.2 kJ/mol,則O3轉化為O2的熱化學方程式為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煤的氣化就是將煤轉化為可燃氣體的過程。水蒸氣通過灼熱的煤所產生的混和氣,其主要成份是CO、H2還含有CO2和水蒸氣。用下列裝置檢驗混和氣中部分物質,下列說法不正確的是( )
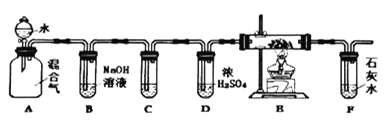
A.若A和B之間增加裝無水CuSO4的干燥管可檢驗H2O的存在
B.若試管C和E中分別裝澄清石灰水、CuO,可檢驗CO的存在
C.在裝置F之后,應該放置一只燃著的酒精燈,防止CO污染空氣
D.工業上將煤氣化,其目的是獲得潔凈的燃料和化工原料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物A是一種不穩定的物質,它的分子組成可用OXFY表示。10mLA氣體能分解生成15mL O2和10mL F2(同溫同壓下)
(1)A的化學式是____________,推斷時依據的定律是___________
(2)已知A分子中x個氧原子呈…-O-O-O-…鏈狀排列,則A分子的電子式是_________結構式是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以鉻鐵礦[主要成份為Fe(CrO2)2,含有Al2O3、Fe2O3、SiO2等雜質]為主要原料生產重鉻酸鈉晶體(Na2Cr2O7·2H2O)的主要工藝流程如圖:
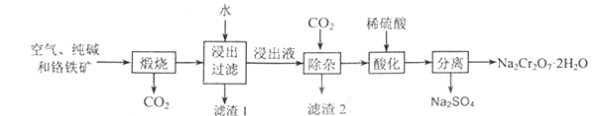
(1)煅燒過程中,鉻鐵礦中的Al2O3與純堿反應的化學方程式為:____。
(2)濾渣1的成分為_____,濾渣2的成分為_____。
(3)該工藝中某種產物可以再利用,該物質的化學式為:_____。
(4)酸化時發生的反應為:2CrO42-+2H+![]() Cr2O72-+H2O,若1L酸化后所得溶液中含鉻元素的質量為28.6g,CrO42-有
Cr2O72-+H2O,若1L酸化后所得溶液中含鉻元素的質量為28.6g,CrO42-有![]() 轉化為Cr2O72-。
轉化為Cr2O72-。
①酸化時發生反應的平衡常數的表達式為K=_____。
②酸化后所得溶液中c(Cr2O72-)=____。
(3)根據有關國家標準,含CrO42-的廢水要經化學處理,使其濃度降至5.0×10-7mol·L-1以下才能排放。含CrO42-的廢水處理通常有以下兩種方法。
①沉淀法:加入可溶性鋇鹽生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸鹽處理多余的Ba2+。加入可溶性鋇鹽后的廢水中Ba2+的濃度應不小于____mol·L-1,后續廢水處理方能達到國家排放標準。
②還原法:CrO42-![]() Cr3+
Cr3+![]() Cr(OH)3。寫出酸性條件下CrO42-與綠礬反應的離子方程式____。
Cr(OH)3。寫出酸性條件下CrO42-與綠礬反應的離子方程式____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com