
| A. | 丙烷分子的球棍模型是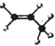 | B. | 2-氯甲苯的結構簡式: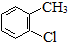 | ||
| C. | 乙醛分子的結構簡式是CH3COH | D. | 葡萄糖、淀粉的最簡式都是CH2O |
分析 A.丙烷中存在單鍵,C原子滿足4對共價鍵,H原子形成1對共價鍵,據此判斷;
B.官能團氯原子位于甲基的鄰位,甲基處于苯環的1號C,則氯原子位于2號C;
C.乙醛的結構簡式含有官能團醛基:-CHO,醛基的書寫不規范;
D.最簡式是用元素符號表示化合物分子中各元素的原子個數比的最簡關系式;
解答 解:A.丙烷中含有3個碳原子和8個H原子,此球棍模型中少2個H,應為丙烯,故A錯誤;
B.2-氯甲苯中,氯原子處于甲基的鄰位,其結構簡式為: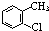 ,故B正確;
,故B正確;
C.乙醛中含有官能團醛基:-CHO,乙醛正確的結構簡式為CH3CHO,故C錯誤;
D.葡萄糖的化學式為C6H12O6,故葡萄糖的最簡式(實驗式):CH2O,淀粉的化學式為(C6H10O5)n,故淀粉的最簡式(實驗式):C6H10O5,故D錯誤;
故選B.
點評 本題主要考查了有機物球棍模型、結構簡式、最簡式等知識,題目難度不大,注意掌握常見化學用語的表示方法.


 智能訓練練測考系列答案
智能訓練練測考系列答案 計算高手系列答案
計算高手系列答案科目:高中化學 來源: 題型:選擇題

| A. | 夏季氣溫高,PAN含量高 | |
| B. | 氣壓低,化學平衡常數增大,PAN含量高 | |
| C. | 減少氮氧化物的排放可以減少PAN的含量 | |
| D. | 大氣中灰塵可起催化作用,能提高過氧乙酰基的轉化率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②④⑤ | B. | ①②③⑤ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某物質的溶液中由水電離出的c(H+)=1×10-amol/L,若a>7時,則該溶液的pH一定為14-a | |
| B. | 某溶液中存在的離子有S2-、HS-、OH-、Na+、H+,則離子濃度一定是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) | |
| C. | pH=3的二元弱酸H2R溶液與 pH=11的NaOH溶液混合后,混合液的pH等于7,則反應后的混合液:c(R2-)+c(HR-)=c(Na+) | |
| D. | 將0.2 mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等體積混合后溶液pH大于7,則反應后的混合液:c(OH-)+c(A-)=c(H+)+c(Na+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷的電子式: | |
| B. | 氮原子的L層電子軌道表示式: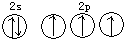 | |
| C. | 硫離子的核外電子排布式:1s22s22p63s23p4 | |
| D. | 碳-12原子:126C |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 在某一容積為5L的密閉容器內,加入0.2mol的CO和0.2mol 的H2O(g),在催化劑存在的條件下高溫加熱,發生如下反應:CO(g)+H2O(g)═CO2(g)+H2(g),反應放出熱量.反應中CO2的濃度隨時間變化的情況如圖所示:
在某一容積為5L的密閉容器內,加入0.2mol的CO和0.2mol 的H2O(g),在催化劑存在的條件下高溫加熱,發生如下反應:CO(g)+H2O(g)═CO2(g)+H2(g),反應放出熱量.反應中CO2的濃度隨時間變化的情況如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 天然氣在生產、生活中具有廣泛的應用.
天然氣在生產、生活中具有廣泛的應用.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com