
某工廠實驗室用一氧化碳和氫氣制備甲醇,其原理為:
CO(g)+2H2(g)![]() CH3OH(g)△H<0。
CH3OH(g)△H<0。
試回答下列問題:
(1)若該反應在298K、398K時化學平衡常數分別為K1、K2,則K1 K2(填“>”“=”或“<”);
(2)在恒溫恒容條件下,判斷該反應達到化學平衡狀態的依據是 (填序號);
A.v(H2)逆=2v(CH3OH)正 B.v(H2)逆=v(CO)正
C.容器內壓強保持不變 D.混合氣體的密度保持不變
(3)某溫度時,向一定容積的密閉容器中充入CO和H2,濃度分別為1mol?L-1、2mol?L-1,達到平衡時CO的濃度為0.6mol?L-1。試求該溫度下的化學平衡常數。
 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案 名題訓練系列答案
名題訓練系列答案科目:高中化學 來源: 題型:閱讀理解
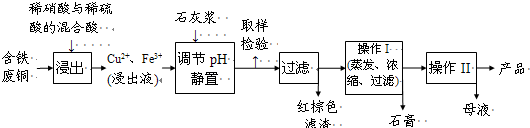
| 溫度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 膽礬 | 32 | 44.6 | 61.8 | 83.8 | 114 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com