
(分)已知四種強電解質溶液,分別含有下列陰、陽離子中的各一種,并且互不重復:NH![]() 、Ba2+、Na+、H+、SO
、Ba2+、Na+、H+、SO![]() 、NO
、NO![]() 、OH-、CO
、OH-、CO![]() 。將這四種溶液分別標記為A、B、C、D,進行如下實驗:
。將這四種溶液分別標記為A、B、C、D,進行如下實驗:
①在A或D中滴入C,均有沉淀生成
②D和B反應生成的氣體能被A吸收
③A和D反應生成的氣體能被B吸收
試回答下列問題:
(1)D的化學式是
(2)寫出B物質的化學式:
(3)寫出實驗②中有關反應的離子方程式
。
科目:高中化學 來源: 題型:閱讀理解
| ② | |||
| ⑦ | ⑧ |
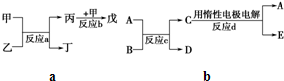
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 .
.
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 1 |
| 2 |
| 1 |
| 2 |
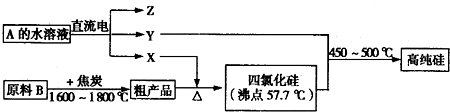
查看答案和解析>>
科目:高中化學 來源:2012-2013學年河南省扶溝縣高級中學高二第三次考試化學試卷(帶解析) 題型:填空題
(12分) 有A、B、C、D四種強電解質,它們在水中電離時可產生下列離子:(每種物質只含一種陽離子和一種陰離子且互不重復)
| 陽離子 | Na+、Ba2+、NH4+、K+ |
| 陰離子 | CH3COO-、Cl-、OH-、SO42- |
查看答案和解析>>
科目:高中化學 來源:2014屆河南省高二第三次考試化學試卷(解析版) 題型:填空題
(12分) 有A、B、C、D四種強電解質,它們在水中電離時可產生下列離子:(每種物質只含一種陽離子和一種陰離子且互不重復)
|
陽離子 |
Na+、Ba2+、NH4+、K+ |
|
陰離子 |
CH3COO-、Cl-、OH-、SO42- |
已知:①A、C溶液的pH均大于7,B溶液的pH小于7,A、B溶液中水的電離程度相同;D溶液焰色反應顯黃色。
②C溶液和D溶液相遇時只生成白色沉淀,B溶液和C溶液相遇時只生成有刺激性氣味的氣體,A溶液和D溶液混合時無明顯現象。
(1)A的名稱是____________。
(2)用離子方程式表示A的水溶液顯堿性的原因______________________________。
(3)25 ℃時pH=9的A溶液和pH=9的C溶液中水的電離程度較小的是________(填寫A或C的化學式)。
(4)25 ℃時用惰性電極電解D的水溶液,一段時間后溶液的pH________7(填“>”、“<”或“=”)。
(5)將等體積、等物質的量濃度的B溶液和C溶液混合,反應后溶液中各種離子濃度由大到小的順序為__________________________________________________。
(6)室溫時在一定體積0.2 mol·L-1的C溶液中,加入一定體積的0.1 mol·L-1的鹽酸時,混合溶液的pH=13,若反應后溶液的體積等于C溶液與鹽酸的體積之和,則C溶液與鹽酸的體積比是________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com