
| A. | 可能由pH=2的鹽酸與pH=12的氨水等體積混合而成 | |
| B. | 該溶液可能由等物質的量濃度的鹽酸和氨水等體積混合而成 | |
| C. | 加入適量氨水,溶液中離子濃度可能為:c (NH4+)>c (Cl-)>c (OH-)>c(H+) | |
| D. | 該溶液中c (NH4+)=c (Cl-)+c (OH-)-c(H+) |
分析 A.常溫下,pH=3的HCl與pH=11的NH3•H2O溶液中,c(NH3•H2O)>c(HCl),二者等體積混合氨水有剩余,溶液呈堿性;
B.氯化銨是強酸弱堿鹽,銨根離子水解導致氯化銨溶液呈酸性;
C.加入適量NH3•H2O,一水合氨的電離程度大于銨根離子水解程度會導致溶液呈堿性,再結合電荷守恒判斷;
D.任何電解質溶液中都存在電荷守恒,根據電荷守恒判斷.
解答 解:A.一水合氨是弱電解質、HCl是強電解質,常溫下,pH=2的HCl與pH=12的NH3•H2O溶液中,c(NH3•H2O)遠遠大于c(HCl),二者等體積混合氨水有剩余,導致溶液呈堿性而不是酸性,故A錯誤;
B.等物質的量濃度、等體積的HCl溶液和NH3•H2O溶液混合,二者恰好反應生成氯化銨,氯化銨是強酸弱堿鹽,銨根離子水解而氯離子不水解導致氯化銨溶液呈酸性,故B正確;
C.加入適量NH3•H2O,一水合氨的電離程度大于銨根離子水解程度會導致溶液呈堿性,根據電荷守恒得c(NH4+)>c(Cl-),溶液中水的電離程度較小,可能出現離子濃度大小順序是c(NH4+)>c(Cl-)>c(OH-)>c(H+),故C正確;
D.任何電解質溶液中都存在電荷守恒,根據電荷守恒得c(NH4+)+c(H+)=c(OH-)+c(Cl-),c (NH4+)=c (Cl-)+c (OH-)-c(H+),故D正確;
故選A.
點評 本題考查了離子濃度大小比較,根據溶液酸堿性再結合電荷守恒確定溶液中離子濃度大小,知道物質的性質是解本題關鍵,題目難度中等.


 期末復習檢測系列答案
期末復習檢測系列答案 超能學典單元期中期末專題沖刺100分系列答案
超能學典單元期中期末專題沖刺100分系列答案 黃岡360度定制密卷系列答案
黃岡360度定制密卷系列答案 陽光考場單元測試卷系列答案
陽光考場單元測試卷系列答案科目:高中化學 來源: 題型:選擇題
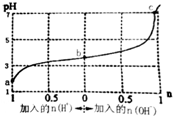
| A. | b點溶液中c(A-)>c(Na+)>c(HA) | |
| B. | 通入HCl后,c(HA)/c(A-)增大 | |
| C. | 當加入1 mol NaOH后,溶液中c(Na+)=c(A-) | |
| D. | a、b、c三點溶液中水的電離程度依次增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
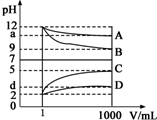 物質A~D為CH3COOH、NaOH、HCl、NH3•H2O中的各一種,常溫下將各物質的溶液從1mL稀釋到1000mL,pH的變化關系如圖所示.請回答下列問題:
物質A~D為CH3COOH、NaOH、HCl、NH3•H2O中的各一種,常溫下將各物質的溶液從1mL稀釋到1000mL,pH的變化關系如圖所示.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 時間/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0020 | 0.0032 | 0.0040 | 0.0040 |
| A. | 前20min的反應速率v(H2O)=2.5×10-5mol•L-1•min-1 | |
| B. | 達平衡時,至少需要從外界吸收的能量為0.968kJ | |
| C. | 增大c(H2O),可以提高水的分解率 | |
| D. | 使用納米級Cu2O顆粒是為了提高催化效果 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
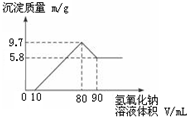 將一定質量的鎂鋁合金投入200mL一定濃度的鹽酸中,合金完全溶解.向所得溶液中滴加濃度為5mol•L-1的NaOH溶液,生成的沉淀跟加入NaOH溶液體積的關系如圖.
將一定質量的鎂鋁合金投入200mL一定濃度的鹽酸中,合金完全溶解.向所得溶液中滴加濃度為5mol•L-1的NaOH溶液,生成的沉淀跟加入NaOH溶液體積的關系如圖.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
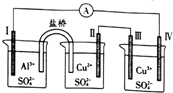
| A. | 電子流向:電極Ⅳ→(A)→電極I | |
| B. | 電極Ⅲ的電極反應:2H2O一4e一=4H++O2↑ | |
| C. | 電極Ⅱ的質量減少,電極Ⅲ的質量增加 | |
| D. | 三個燒杯中的SO42-濃度都始終保持不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業上用電解熔融氯化鎂制單質鎂 | |
| B. | 工業上用電解飽和食鹽水制氯氣 | |
| C. | 工業上用二氧化硅在高溫下與焦炭反應制得高純度的硅 | |
| D. | 工業上煉鐵時,常用石灰石除去鐵礦石中的SiO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
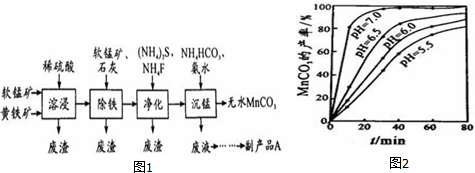
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com