


分析 Ⅰ.(1)組裝儀器完畢,需要檢驗裝置的氣密性;
(2)B中的堿石灰是吸收置換反應生成的水的,為了防止空氣成分對實驗的影響,要加一個裝置吸收空氣中的水以及二氧化碳;
(3)反應后裝置B增重1.35g,即氫氣和氧化鐵反應后固體質量的增加值,可以根據差量法來計算;
Ⅱ.(1)煮沸可以將水中的氣體趕走;
(2)根據滴定試驗以及滴定過程中的實驗誤差分析知識來回答判斷;
(3)根據元素守恒和化學反應方程式進行計算.
解答 解:Ⅰ.(1)組裝儀器完畢,需要檢驗裝置的氣密性,
故答案為:檢驗裝置的氣密性;
(2)該實驗中,氫氣和氧化鐵反應生成金屬鐵和水,根據固體質量的變化來計算鐵的含量,B處的干燥管作用是吸收產生的水蒸氣,所以C裝置要防止防止空氣中的水蒸氣和CO2進入B中,影響測定結果,
故答案為:防止空氣中的水蒸氣和CO2進入B中,影響測定結果;
(3)測的反應后裝置B增重1.35g,根據反應的實質,增加的是水的質量,根據質量守恒定律,所以鐵礦石中氧的百分含量是:$\frac{\frac{1.35}{18}×16}{5.0}$×100%=24%,
故答案為:24%;
Ⅱ.(1)向鐵礦石中加入硫酸,化反應生成硫酸的鐵鹽溶液,還存在過量的硫酸溶液,加入過量的氯氣,煮沸后可以降低氯氣的溶解度,趕走溶液中溶解的過量的Cl2,
故答案為:趕走溶液中溶解的過量的Cl2;
(2)a.滴定管用蒸餾水洗滌后必須用標準液潤洗,故a錯誤;
b.錐形瓶不需要用待測液潤洗,故b正確;
c.滴定過程中,眼睛注視錐形瓶中顏色的變化,故c錯誤;
d.滴定結束后,30s內溶液不恢復原來的顏色再讀數,故d正確.
故答案為:bd;
(3)根據反應的方程式為2Fe3++2I-=2Fe2++I2可知,消耗的碘離子與鐵離子物質的量相等,n(Fe3+)=n(KI),即:0.4000mol•L-1×0.025L=c(Fe3+)×0.02L,解得c(Fe3+)=0.5mol•L-1,所以鐵元素的百分含量為:$\frac{0.5mol/L×0.25L×56g/mol}{10g}$×100%=70%,
故答案為:70%.
點評 本題考查了探究鐵礦石中氧元素和鐵元素的含量的方法,該題是高考中的常見題型,屬于中等難度的試題,側重對學生能力的培養和訓練,有利于培養學生規范嚴謹的實驗設計、操作能力;該類試題綜合性強,理論和實踐的聯系緊密,要求學生必須認真、細致的審題,聯系所學過的知識和技能,全面細致的思考才能得出正確的結論,難度中等.


 學練快車道快樂假期寒假作業系列答案
學練快車道快樂假期寒假作業系列答案 新思維寒假作業系列答案
新思維寒假作業系列答案科目:高中化學 來源: 題型:解答題
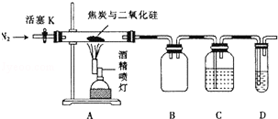 某實驗小組設計了如下裝置對焦炭還原二氧化硅的氣體產物的成分進行探究.
某實驗小組設計了如下裝置對焦炭還原二氧化硅的氣體產物的成分進行探究.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
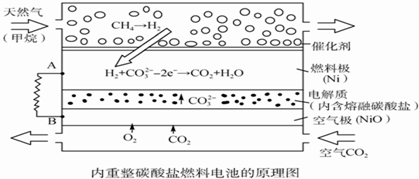
| A. | 以此電池為電源電解精煉銅,當有0.1 mol e-轉移時,有3.2 g銅溶解 | |
| B. | 若以甲烷為燃料氣時負極電極反應式:CH4+5O2--8e-═CO32-+2H2O | |
| C. | 該電池使用過程中需補充Li2CO3和K2CO3 | |
| D. | 空氣極發生的電極反應式為O2+4e-+2CO2═2CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 甲烷作為一種新能源在化學領域應用廣泛,請回答下列問題:
甲烷作為一種新能源在化學領域應用廣泛,請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯氣可使濕的紅布條褪色,所以氯氣具有漂白性 | |
| B. | 氯氣沒有漂白性,但通入品紅溶液中,品紅褪色 | |
| C. | 氯氣不跟非金屬反應 | |
| D. | 氯氣有毒,聞其氣味時要小心將集氣瓶放在鼻孔下直接聞其氣味 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解飽和食鹽水時,陰極的電極反應式為 2Cl--2e-═Cl2↑ | |
| B. | 放電時,鉛蓄電池中硫酸濃度不斷減小 | |
| C. | 氫氧燃料電池中,當電路上有1mol 電子通過時,則正極上消耗氧氣為5.6L | |
| D. | 以鋅片、銅片、稀硫酸組成原電池,當溶液中通過0.2mol電子時,負極減輕6.5g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com