
 乙醇的沸點是78℃,能與水以任意比混溶,易與氯化鈣結合生成配合物.乙醚的沸點為34.6℃,難溶于水,乙醚極易燃燒.實驗室制乙醚的反應原理是:
乙醇的沸點是78℃,能與水以任意比混溶,易與氯化鈣結合生成配合物.乙醚的沸點為34.6℃,難溶于水,乙醚極易燃燒.實驗室制乙醚的反應原理是:分析 (1)液體加熱加沸石,是防止液體瀑沸,如果實驗中忘記加沸石,停止加熱,冷卻后補加,否則也會引起瀑沸;
(2)乙醚的制備過程中要測量反應溶液的溫度,而精制過程中需要測量蒸出物的沸點,據此判斷;
(3)根據裝置圖判斷儀器C的名稱;
(4)乙醇在濃硫酸作用下加熱到170℃就可以生成乙烯;
(5)精制乙醚中,餾出物中可能有酸性雜質,餾出物中乙醇,可以用飽和氯化鈣溶液除去.
解答 解:(1)液體加熱加沸石,是防止液體瀑沸,如果實驗中忘記加沸石,停止加熱,冷卻后補加,否則也會引起瀑沸,所以乙醚的制備和精制過程中都需要使用沸石,其作用是防止暴沸,如果實驗中忘記加沸石,停止加熱,冷卻后補加,
故答案為:防止暴沸;如果實驗中忘記加沸石,停止加熱,冷卻后補加;
(2)乙醚的制備過程中要測量反應溶液的溫度,所以水銀球位置在溶液中間,而精制過程中需要測量蒸出物的沸點,水銀球位置在蒸餾燒瓶的支管處,所以它們的位置不同,
故答案為:否;制備要控制反應液的溫度,水銀球要放在反應液里;蒸餾要測餾份的溫度,要放在支管口處;
(3)根據裝置圖可知儀器C的名稱為冷凝管,故答案為:冷凝管;
(4)乙醇在濃硫酸作用下加熱到170℃就可以生成乙烯,如果溫度太高,將會發生副反應,產物是乙烯,故答案為:乙烯;
(5)精制乙醚中,餾出物中可能有酸性雜質,餾出物中乙醇,可以用飽和氯化鈣溶液除去,精制乙醚中,加入15% NaOH溶液的作用是 除去酸性雜質,加入飽和氯化鈣溶液的作用是除乙醇,
故答案為:除去酸性雜質;除乙醇.
點評 本題通過考查乙醚的制取,考查了對信息的處理能力,對基本實驗操作的掌握情況,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 150 mL 2 mol•L-1鹽酸 | B. | 150 mL 2 mol•L-1硫酸 | ||
| C. | 500 mL 3 mol•L-1鹽酸 | D. | 500 mL 18.4 mol•L-1濃硫酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
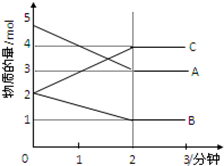 某可逆反應在某體積為5L的密閉容器中進行,在從0~3分鐘各物質的量的變化情況如圖所示(A,B,C均為氣體)
某可逆反應在某體積為5L的密閉容器中進行,在從0~3分鐘各物質的量的變化情況如圖所示(A,B,C均為氣體)查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com