
【題目】在給定的條件下,下列選項所示的物質間轉化均能一步實現的是( )
A.Fe![]() FeCl3(aq)
FeCl3(aq)![]() FeCl2(aq)
FeCl2(aq)
B.S![]() SO2
SO2![]() (NH4)2SO4(aq)
(NH4)2SO4(aq)
C.NaCl(熔融)![]() Na
Na![]() Na2O
Na2O
D.CuSO4(aq)![]() Cu(OH)2(s)
Cu(OH)2(s)![]() Cu2O(s)
Cu2O(s)
 百分學生作業本題練王系列答案
百分學生作業本題練王系列答案 互動課堂系列答案
互動課堂系列答案科目:高中化學 來源: 題型:
【題目】在25 ℃時,密閉容器中X、Y、Z三種氣體的初始濃度和平衡濃度如下表:
物質 | X | Y | Z |
初始濃度/(mol·L-1) | 0.1 | 0.2 | 0 |
平衡濃度/(mol·L-1) | 0.05 | 0.05 | 0.1 |
下列說法錯誤的是( )
A.增大壓強使平衡向生成Z的方向移動,平衡常數增大
B.反應可表示為X+3Y![]() 2Z,其平衡常數為1600
2Z,其平衡常數為1600
C.反應達平衡時,X的轉化率為50%
D.改變溫度可以改變此反應的平衡常數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下將NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH與離子濃度變化的關系如圖所示。下列敘述錯誤的是

A. Ka2(H2X)的數量級為10-6
B. 曲線N表示pH與 的變化關系
的變化關系
C. NaHX溶液中c(H+)>c(OH-)
D. 當混合溶液呈中性時,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H是一種香料,其合成路線如下:
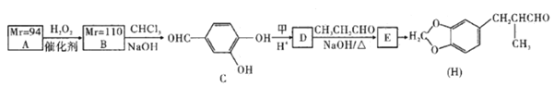
已知: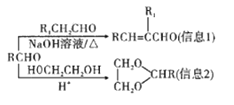
回答下列問題:
(1)A遇氯化鐵溶液發生顯色反應且A僅含C、H、0三種元素,則A的名稱是________。
(2)甲的相對分子質量為30,下列有關甲的說法正確的是______(填字母)。
a.常溫下,甲能使溴水(或酸性高錳酸鉀溶液)褪色
b. 1 mol甲與足量銀氨溶液反應最多生成2 mol Ag
c.甲和葡萄糖的最簡式相同
d.甲在常溫常壓下呈液態
(3)寫出A—B反應的原子利用率的表達式為_________________________________。
(4)在一定條件下,甲和A合成電木的化學方程式為_______________________。
(5)參照上述信息,以苯甲醇和乙醛為原料合成肉桂酸(![]() ),設計合成路線:___(無機試劑任用,合成路線流程圖示例見本題題干)。
),設計合成路線:___(無機試劑任用,合成路線流程圖示例見本題題干)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦呈銀白色,因它堅硬、強度大、耐熱、密度小,被稱為高技術金屬。目前生產鈦采用氯化法,即將金紅石或鈦鐵礦與焦炭混合,通入氯氣并加熱制得TiCl4:2FeTiO3+7Cl2+6C![]() 2TiCl4+2FeCl3+6CO; TiO2+2Cl2+2C
2TiCl4+2FeCl3+6CO; TiO2+2Cl2+2C![]() TiCl4+2CO。將TiCl4蒸餾并提純,在氬氣保護下與鎂共熱得到鈦:TiCl4+2Mg
TiCl4+2CO。將TiCl4蒸餾并提純,在氬氣保護下與鎂共熱得到鈦:TiCl4+2Mg![]() Ti+2MgCl2,MgCl2和過量Mg用稀鹽酸溶解后得海綿狀鈦,再在真空熔化鑄成鈦錠。請回答下列問題:
Ti+2MgCl2,MgCl2和過量Mg用稀鹽酸溶解后得海綿狀鈦,再在真空熔化鑄成鈦錠。請回答下列問題:
(1)基態鈦原子的價電子排布式為_______________________________。
(2)與CO互為等電子體的離子為_____(填化學式)。
(3)在CH2Cl2、C6H6、CO2、C2H4中,碳原子采取sp雜化的分子有__________ 。
(4)TiCl4在常溫下是無色液體,在水或潮濕空氣中易水解而冒白煙。則TiCl4屬于______(填“原子”、“分子”或“離子”)晶體。
(5)與鈦同周期的另一種元素鈷(Co)可形成分子式均為Co(NH3)5BrSO4的兩種配合物,其中一種化學式為[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液時,現象是_____________;往另一種配合物的溶液中加入BaCl2溶液時,無明顯現象,若加入AgNO3溶液時,產生淡黃色沉淀,則第二種配合物的化學式為 __________。
(6)在自然界中TiO2有金紅石、板鈦礦、銳鈦礦三種晶型,其中金紅石的晶胞如右圖所示,則其中Ti4+的配位數為__________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是電解CuCl2溶液的裝置,其中c、d為石墨電極。則下列判斷正確的是( )
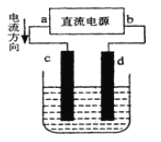
A.a為負極、b為正極
B.電解過程中,c電極上發生氧化反應
C.d為陽極,電極反應為:2Cl--2e-=Cl2↑
D.電解過程中,電能轉化為化學能
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的值。下列敘述中正確的是
A. l00g 9%的葡萄糖水溶液中氧原子數為0.3 NA
B. 標準狀況下,2.24L F2通入足量飽和食鹽水中可置換出0.1NA個Cl2
C. 工業合成氨每斷裂NA個N≡N鍵,同時斷裂6NA個N-H鍵,則反應達到平衡
D. 常溫下l LpH=7的1mol/LCH3COONH4溶液中CH3COO-與NH4+數目均為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示為“鐵鏈環”結構,圖中兩環相交部分A、B、C、D 表示物質間的反應。下列對應部分反應的離子方程式書寫不正確的是
![]()
A.Cl2+2OH-=Cl-+ClO-+H2O
B.Cu2++2OH-=Cu(OH)2↓
C.Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓
D.OH-+HCO3-=H2O+CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖為某同學設計的原電池裝置
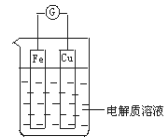
(1)當電解質溶液為稀硫酸時:
①Fe電極是_______(填“正”或“負”)極,其電極反應為_______
②Cu電極的電極反應為_________,該電極發生______反應(填“氧化”或“還原”)反應。原電池工作一段時間后,鐵片的質量減少了2.8克,銅片表面產生氣體____L(標準狀況下),導線中通過_____mol電子。
(2)當電解質溶液為稀硝酸時:
①Fe電極是______極,其電極反應為________________,
②Cu電極是_____極,其電極反應為_________________,
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com