
氧化還原滴定與酸堿中和滴定一樣是化學實驗室常用的定量測定方法。某氧化還 原滴定的反應體系中有反應物和生成物共六種,
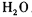 ,其中H2SO3的還原性最強,KMnO4的氧化性最強。對此反應體系:
,其中H2SO3的還原性最強,KMnO4的氧化性最強。對此反應體系:
(1) 被氧化的元素是_______;發生還原反應的過程是________→______。
(2) 請用這六種物質組織一個合理的化學反應,寫出它的離子方程式:_______
(3) 反應中H2SO4是_______ (填編號)
A,氧化劑 B.氧化產物 C.生成物 D.反應物
(4) 當有20mL 0.1mol/L的氧化劑參加反應時,電子轉移數目是_______ 。
(5) 用標準KMnO4溶液滴定H2SO3時,滴定終點時顏色變化是_______。
(6) 滴定過程中.下列圖像所表示的關系正確的是_______(填編號)。
(11分) (1) +4價的 S(1分); KMnO4 → MnSO4(2分);
(2) 2MnO4- +5H2SO3 =2Mn2+ +5SO42- +4H++3H2O(1分);
(3) B、C (2分); (4) 0.01NA(或6.02×1021)(2分);
(5)溶液由無色變為紫紅色,且半分鐘內不變色 (1分);(6) (a)(c) (2分)
【解析】
試題分析:(1) H2SO3的還原性最強,說明其中的+4價的S元素易被氧化,KMnO4的氧化性最強,說明發生還原反應,故被氧化的元素是+4價的S,發生還原反應的過程是KMnO4 → MnSO4。
(2) H2SO3的還原性最強,反應中做為還原劑,KMnO4的氧化性最強,反應中做為氧化劑,離子方程式為2MnO4- +5H2SO3 =2Mn2+ +5SO42- +4H++3H2O。
(3) H2SO4是H2SO3被氧化后生成的產物,故反應中H2SO4是氧化產物,故錯BC。
(4)根據離子方程式分析,2molMnO4-轉移電子數為10 NA電子,故20mL 0.1mol/L,即0.002mol的氧化劑參加反應時,電子轉移數目是0.01NA(或6.02×1021)。
(5)反應過程中,紫紅色的KMnO4生成為無色的MnSO4,故用標準KMnO4溶液滴定H2SO3時,滴定終點時顏色變化是溶液由無色變為紫紅色,且半分鐘內不變色。
(6) 滴定過程中,有酸生成,故pH減小,故(a)正確;反應物H2SO3是弱電解質,部分電離,生成的H2SO4是強電解質,全部電離,離子難度增大,導電性增強,故(b)錯誤,(c)正確。故選(a)(c)。
考點:氧化還原反應的應用 酸堿中和滴定
點評:本題考查氧化反應的應用和酸堿中和滴定,題目難度中等,注意把握滴定原理以及實驗的誤差分析,為該題的易錯點。


科目:高中化學 來源: 題型:閱讀理解
| 滴定次數 | 待測液體積 (mL) |
標準KMnO4溶液體積(mL) | |
| 滴定前讀數 | 滴定后讀數 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
| 難溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 顏色 | 白 | 淺黃 | 白 | 磚紅 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
查看答案和解析>>
科目:高中化學 來源:2013屆新疆烏魯木齊地區高三第一次診斷性測驗化學試卷(帶解析) 題型:填空題
氧化還原滴定與酸堿中和滴定一樣是化學實驗室常用的定量測定方法。某氧化還 原滴定的反應體系中有反應物和生成物共六種,
 ,其中H2SO3的還原性最強,KMnO4的氧化性最強。對此反應體系:
,其中H2SO3的還原性最強,KMnO4的氧化性最強。對此反應體系:
(1) 被氧化的元素是_______;發生還原反應的過程是________→______。
(2) 請用這六種物質組織一個合理的化學反應,寫出它的離子方程式:_______
(3) 反應中H2SO4是_______ (填編號)
A,氧化劑 B.氧化產物 C.生成物 D.反應物
(4) 當有20mL 0.1mol/L的氧化劑參加反應時,電子轉移數目是_______ 。
(5) 用標準KMnO4溶液滴定H2SO3時,滴定終點時顏色變化是_______。
(6) 滴定過程中.下列圖像所表示的關系正確的是_______(填編號)。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年陜西省西安市高三第四次質量檢測化學試卷(解析版) 題型:實驗題
滴定實驗是化學學科中重要的定量實驗。
請回答下列問題:
(1)酸堿中和滴定——用標準鹽酸滴定未知濃度的NaOH溶液。
①下列操作造成測定結果偏高的是 (填選項字母)
A.滴定終點讀數時,俯視滴定管刻度,其他操作正確。
B.盛裝未知液的錐形瓶用蒸餾水洗過,未用未知液潤洗
C.酸式滴定管用蒸餾水洗凈后,未用標準鹽酸潤洗
D.滴定前,滴定管尖嘴有氣泡,滴定后氣泡消失
②該學生的實驗操作如下:
A、用堿式滴定管取稀NaOH 25.00mL,注入錐形瓶中,加入甲基橙做指示劑。
B、用待測定的溶液潤洗堿式滴定管。
C、用蒸餾水洗干凈滴定管。
D、取下酸式滴定管用標準的HCl溶液潤洗后,將標準液注入滴定管刻度“0”以上2~3cm處,再把滴定管固定好,調節液面至刻度“0”或“0”刻度以下。
E、檢查滴定管是否漏水。
F、另取錐形瓶,再重復操作一次。
G、把錐形瓶放在滴定管下面,瓶下墊一張白紙,邊滴邊搖動錐形瓶直至滴定終點,記下滴定管液面所在刻度。
a. 滴定操作的正確順序是(用序號填寫)___________________________ 。
b. 在G操作中如何確定終點? __________________________ ____ 。
c. 若換酚酞做指示劑,如何確定終點? _________________________ ____ 。
(2)氧化還原滴定—取草酸溶液置于錐形瓶中,加入適量稀硫酸,用濃度為0.1mol·L-1的高錳酸鉀溶液滴定,發生的反應為:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中記錄了實驗數據:
|
滴定次數 |
待測液體積 (mL)[來 |
標準KMnO4溶液體積(mL) |
|
|
滴定前讀數 |
滴定后讀數 |
||
|
第一次 |
25.00 |
0.50 |
20.40 |
|
第二次 |
25.00 |
3.00 |
23.00 |
|
第三次 |
25.00 |
4.00 |
24.10 |
①滴定時,KMnO4溶液應裝在 (“酸”或“堿”)式滴定管中,滴定終點時滴定現象是 。
②該草酸溶液的物質的量濃度為_____________。
(3)沉淀滴定――滴定劑和被滴定物的生成物比滴定劑與指示劑的生成物更難溶。
參考下表中的數據,若用AgNO3滴定NaSCN溶液,可選用的指示劑是 (填選項字母)。
|
難溶物 |
AgCl |
AgBr |
AgCN |
Ag2CrO4 |
AgSCN |
|
顏色 |
白 |
淺黃 |
白 |
磚紅 |
白 |
|
Ksp |
1.77×10-10 |
5.35×10-13 |
1.21×10-16 |
1.12×10-12 |
1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
查看答案和解析>>
科目:高中化學 來源:2014屆河南省平頂山市高二上學期期末考試化學試卷(解析版) 題型:實驗題
滴定實驗是化學學科中重要的定量實驗。
請回答下列問題:
(1)酸堿中和滴定——用標準鹽酸滴定未知濃度的NaOH溶液,下列操作造成測定結果偏高的是 (填選項字母)
A.滴定終點讀數時,俯視滴定管刻度,其他操作正確。
B.盛裝未知液的錐形瓶用蒸餾水洗過,未用未知液潤洗
C.酸式滴定管用蒸餾水洗凈后,未用標準鹽酸潤洗
D.滴定前,滴定管尖嘴有氣泡,滴定后氣泡消失
(2)氧化還原滴定——取草酸溶液置于錐形瓶中,加入適量稀硫酸,用濃度為0.1mol·L-1的高錳酸鉀溶液滴定,發生的反應為:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中記錄了實驗數據:
|
滴定次數 |
待測液體積 (mL) |
標準KMnO4溶液體積(mL) |
|
|
滴定前讀數 |
滴定后讀數 |
||
|
第一次 |
25.00 |
0.50 |
20.40 |
|
第二次 |
25.00 |
3.00 |
23.00 |
|
第三次 |
25.00 |
4.00 |
24.10 |
①滴定時,KMnO4溶液應裝在 (填“酸”或“堿”)式滴定管中,滴定終點時滴定現象是
②該草酸溶液的物質的量濃度為_____________。
(3)沉淀滴定――滴定劑和被滴定物的生成物比滴定劑與指示劑的生成物更難溶。
參考下表中的數據,若用AgNO3滴定NaSCN溶液,可選用的指示劑是 (填選項字母)。
|
難溶物 |
AgCl |
AgBr |
AgCN |
Ag2CrO4 |
AgSCN |
|
顏色 |
白 |
淺黃 |
白 |
磚紅 |
白 |
|
Ksp |
1.77×10-10 |
5.35×10-13 |
1.21×10-16 |
1.12×10-12 |
1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com