(2009?江門一模)氯化亞銅是一種重要的化工產(chǎn)品,常用作有機合成催化劑,還可用于顏料,防腐等工業(yè).該物質(zhì)是微溶于水的白色固體,露置于空氣中易被氧化為綠色的堿式氯化銅(Cu
2(0H)
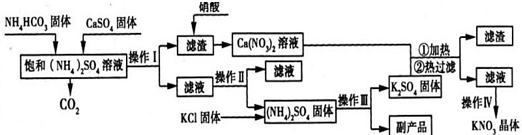
3Cl),在熱水中易水解生成氧化銅水合物而呈紅色.以下是一種采用亞硫酸鹽還原法,從含銅電鍍廢水中制備氯化亞銅的工藝流程如圖1.

已知Ksp:CuCl:1.2×10
-4 CuOH:1.4×10
-15 Cu (OH)
2:1.6×10
-10請回答以下問題:
(1)寫出反應(yīng)①制備氯化亞銅的離子反應(yīng)方程式:
2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+
2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+
.
(2)為提高CuCl的產(chǎn)率,常在反應(yīng)①的體系中加入稀堿溶液,調(diào)節(jié)pH至3.5.這樣做的目的是
OH-中和了反應(yīng)中的H+,有利于平衡向右進行,提高CuCl的產(chǎn)率.但當OH-濃度過大時,Cu+能與OH-結(jié)合,生成氫氧化亞銅,從而降減了CuCl的產(chǎn)率
OH-中和了反應(yīng)中的H+,有利于平衡向右進行,提高CuCl的產(chǎn)率.但當OH-濃度過大時,Cu+能與OH-結(jié)合,生成氫氧化亞銅,從而降減了CuCl的產(chǎn)率
.
(3)圖2是各反應(yīng)物在最佳配比條件下,反應(yīng)溫度對CuCl產(chǎn)率影響.由圖2可知,溶液溫度控制在
60℃
60℃
時,CuCl產(chǎn)率能達到94%,隨后隨溫度升高CuCl產(chǎn)率會下降,其原因是
溫度過高,一是促進了CuCl的水解,二是促進了CuCl與空氣中氧氣發(fā)生反應(yīng)
溫度過高,一是促進了CuCl的水解,二是促進了CuCl與空氣中氧氣發(fā)生反應(yīng)
.
(4)若要提高Cucl的產(chǎn)率你認為還可采取的措施有
反應(yīng)①在隔絕空氣條件下進行
反應(yīng)①在隔絕空氣條件下進行
.
(5)寫出氯化亞銅在空氣中被氧化的化學方程式
4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl
4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl
.
(6)反應(yīng)①也可用鐵代替亞硫酸鈉,寫出該反應(yīng)的化學方程式
2CuSO4+2NaCl+Fe=2CuCl+FeSO4+Na2SO4
2CuSO4+2NaCl+Fe=2CuCl+FeSO4+Na2SO4
.



 天天向上口算本系列答案
天天向上口算本系列答案
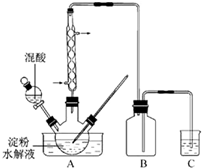 (2011?江蘇)草酸是一種重要的化工產(chǎn)品.實驗室用硝酸氧化淀粉水解液制備草酸的裝置如圖14所示(加熱、攪拌和儀器固定裝置均已略去)
(2011?江蘇)草酸是一種重要的化工產(chǎn)品.實驗室用硝酸氧化淀粉水解液制備草酸的裝置如圖14所示(加熱、攪拌和儀器固定裝置均已略去)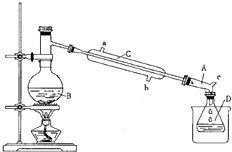 溴乙烷是一種重要的化工合成原料.實驗室合成溴乙烷的反應(yīng)和實驗裝置如下:
溴乙烷是一種重要的化工合成原料.實驗室合成溴乙烷的反應(yīng)和實驗裝置如下: