
分析 (1)根據物質與水的反應物與生成物來書寫化學反應方程式,再利用氧化還原反應中電子轉移計算,然后來計算標準狀況下氣體的體積;
(2)利用蓋斯定律來計算反應熱;
(3)①滴加適量的淀粉KI溶液,呈藍色,說明有NO3-,SO32-與NO3-不能共存;滴加用鹽酸酸化的BaCl2溶液,有白色沉淀析出,故一定含有SO42-;滴加NaOH溶液,加熱,產生的氣體能使濕潤的紅色石蕊試紙變藍,則有氨氣生成,故一定含有NH4+;加入足量硝酸酸化的AgNO3溶液,有沉淀產生,靜置,在上層清液中滴加酸性KMnO4溶液,不褪色,一定不含NO2-,若有NO2-,能使酸性KMnO4褪色,而氯離子的存在與否不能判斷,因為硫酸根已經存在;
②根據單質碘能使淀粉KI溶液呈藍色來分析;
(4)根據物質的性質來書寫方程式,根據一氧化氮在反應中的特點來判斷所起到的作用;
解答 解:(1)NO2與H2O反應的方程式為:3NO2+H2O═2HNO3+NO;6NO2+8NH3═7N2+12H2O,當反應中有1 mol NO2參加反應時,共轉移了4 mol電子,故轉移1.2mol電子時,消耗的NO2為1.2÷4×22.4L=6.72L.
故答案為:3NO2+H2O=2HNO3+NO;6.72;
(2)根據蓋斯定律,將第二個方程式反寫,與第一個方程式相加得:2NO2+2SO2═2SO3+2NO,△H=-83.6 kJ•mol-1,故NO2+SO2?SO3+NO,△H=-41.8 kJ•mol-1;
故答案為:-41.8;
(3)①滴加適量的淀粉KI溶液,呈藍色,說明在該酸性溶液中有一種能將碘離子氧化為碘單質的離子存在,而這樣的離子只有NO3-,故一定含有NO3-,就一定不會含有SO32-,因為SO32-具有較強的還原性,酸性條件下,與NO3-不能共存;滴加用鹽酸酸化的BaCl2溶液,有白色沉淀析出,故一定含有SO42-;滴加NaOH溶液,加熱,產生的氣體能使濕潤的紅色石蕊試紙變藍,則有氨氣生成,故一定含有NH4+;加入足量硝酸酸化的AgNO3溶液,有沉淀產生,靜置,在上層清液中滴加酸性KMnO4溶液,不褪色,一定不含NO2-,若有NO2-,能使酸性KMnO4褪色,而氯離子的存在與否不能判斷,因為硫酸根已經存在,
故答案為:SO42-、NO3-、NH4+;SO32-、NO2-;SO32-具有較強的還原性,酸性條件下,與NO3-不能共存;若有NO2-,能使酸性KMnO4溶液褪色;
②硝酸氧化碘離子的離子方程式為:6I-+2NO3-+8H+=3I2+2NO↑+4H2O,故答案為:6I-+2NO3-+8H+=3I2+2NO↑+4H2O;
(4)一氧化氮具有還原性,很容易被氧氣氧化,方程式為:2NO+O2=2NO2,二氧化氮能將二氧化硫氧化,方程式為NO2+SO2=SO3+NO,整個過程一氧化氮的質量沒有變化,故在反應中作催化劑,
故答案為:催化劑.
點評 本題考查了蓋斯定律的應用、方程式的書寫、離子共存和氧化還原反應、催化劑等,題目難度中等,側重于考查學生的分析能力和對基礎知識的綜合應用能力,注意把握常見離子的檢驗方法以及物質的性質.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 60.0g水晶晶體中,含有“Si-O”鍵的數目為NA | |
| B. | 7.8 g過氧化鈉晶體中含有陰離子的數目為0.2NA | |
| C. | 18.4 g甲苯中含有碳碳雙鍵的個數為0.6 NA | |
| D. | 12g石墨烯(單層石墨)中含有六元環的個數為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D | |
| 用品 |  |  |  聚乙烯盒 |  |
| 成分 | (NH4)2SO4 | Na2CO3 |  | Fe2O3 |
| 用途 | 化肥 | 制玻璃 | 盛放食品 | 涂料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
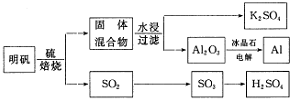
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
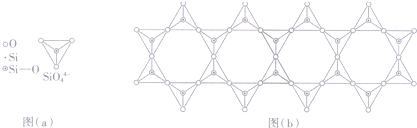
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
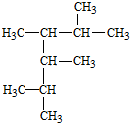 2,3,4,5-四甲基己烷
2,3,4,5-四甲基己烷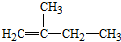 2-甲基-1-丁烯
2-甲基-1-丁烯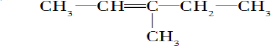 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 離子晶體中,一定不存在共價鍵 | B. | 原子晶體中,只存在共價鍵 | ||
| C. | 金屬晶體的熔沸點均很高 | D. | 稀有氣體的原子能形成分子晶體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com