
 .該物質遇水劇烈反應,產生有刺激性氣味的混合氣體X和Y,同時還有固體單質產生,X是一種能使品紅溶液褪色的氣體,Y在標準狀態下的密度為1.63g/L,該混合氣體相對于H2的密度為21,寫出上述過程對應的化學方程式2S2Cl2+2H2O=SO2↑+4HCl↑+3S↓.某研究性小組同學開動腦筋,為確定干燥的X 和Y混合氣體中Y的存在,設計方案如下:把干燥的X和Y與干燥的NH3混合,出現白煙,則證明有Y氣體.你認為此方案正確 (填正確,不正確),理由是SO2與干燥的NH3不反應,而HCl和干燥的NH3反應生成白煙.
.該物質遇水劇烈反應,產生有刺激性氣味的混合氣體X和Y,同時還有固體單質產生,X是一種能使品紅溶液褪色的氣體,Y在標準狀態下的密度為1.63g/L,該混合氣體相對于H2的密度為21,寫出上述過程對應的化學方程式2S2Cl2+2H2O=SO2↑+4HCl↑+3S↓.某研究性小組同學開動腦筋,為確定干燥的X 和Y混合氣體中Y的存在,設計方案如下:把干燥的X和Y與干燥的NH3混合,出現白煙,則證明有Y氣體.你認為此方案正確 (填正確,不正確),理由是SO2與干燥的NH3不反應,而HCl和干燥的NH3反應生成白煙. 分析 B既是蛋白質的重要組成成分,也是某種化肥的組成成分,則B為N元素;C為金屬元素,焰色反應呈黃色,則C為Na元素;A、B的原子序數之和是元素D的一半,且D的原子序數小于18,則A只能為H元素,D的原子序數為:2(1+7)=16,則D為S元素;E能夠形成化合物的短周期元素,其原子序數大于S,所以E為Cl元素,據此結合元素周期律知識進行解答.
解答 解:B既是蛋白質的重要組成成分,也是某種化肥的組成成分,則B為N元素;C為金屬元素,焰色反應呈黃色,則C為Na元素;A、B的原子序數之和是元素D的一半,且D的原子序數小于18,則A只能為H元素,D的原子序數為:2(1+7)=16,則D為S元素;E能夠形成化合物的短周期元素,其原子序數大于S,所以E為Cl元素,
(1)E為Cl元素,原子序數為17,位于周期表中第三周期第ⅤⅡA族,
故答案為:第三周期第ⅤⅡA族;
(2)B為N元素,D為S元素,形成的化合物中,S的質量分數約為70%,則N的質量分數為30%,則S和N原子個數比為:$\frac{70%}{32}$:$\frac{30%}{14}$=1:1,其相對分子質量在170~190之間,設化學式為(SN)x,則170<46x<190,則x只能為4,所以二者形成的化合物的分子式為:S4N4,
故答案為:S4N4;
(3)B4A4為N4H4,N4H4電離生成兩種離子,其中一種為10電子的NH4+,依據N元素與H元素守恒得知另外一種離子應為N3-,該電離方程式為:N4H4=NH4++N3-,
故答案為:N4H4=NH4++N3-;
(4)C2D為Na2S,Na2S溶液在空氣中長期放置,與氧氣反應會生成Na2S2,則Na2S溶液在空氣中變質過程的化學方程式為:4Na2S+O2+2H2O═4NaOH+2Na2S2,
故答案為:4Na2S+O2+2H2O═4NaOH+2Na2S2;
(5)D、E兩元素分別為S和Cl,按原子個數比1:1組成化合物丁且各原子均滿足8電子的穩定結構,其化學式為S2Cl2,其電子式為 ;S2Cl2遇水劇烈反應,產生有刺激性氣味的混合氣體X和Y,同時還有固體單質產生,X是一種能使品紅溶液褪色的氣體,則X為二氧化硫;Y在標準狀態下的密度為1.63g/L,Y的摩爾質量為:1.63g/L×22.4L/mol=36.5,則Y為HCl,根據化合價變化可知,單質為S,
;S2Cl2遇水劇烈反應,產生有刺激性氣味的混合氣體X和Y,同時還有固體單質產生,X是一種能使品紅溶液褪色的氣體,則X為二氧化硫;Y在標準狀態下的密度為1.63g/L,Y的摩爾質量為:1.63g/L×22.4L/mol=36.5,則Y為HCl,根據化合價變化可知,單質為S,
該混合氣體相對于H2的密度為21,混合氣體的平均相對分子質量為:2×21=42,
設混合氣體中二氧化硫的物質的量為x,HCl為的物質的量為y,則:$\frac{64x+36.5y}{x+y}$=42,整理可得:x:y=1:4,根據質量守恒定律可知則該反應的化學方程式為:2S2Cl2+2H2O=SO2↑+4HCl↑+3S↓;
為確定干燥的SO2和HCl混合氣體中HCl的存在,由于SO2與干燥的NH3不反應,而HCl和干燥的NH3反應生成白煙,所以可把干燥的SO2和HCl與干燥的NH3混合,出現白煙,則證明有HCl氣體,故該檢驗方法正確,
故答案為: ;2S2Cl2+2H2O=SO2↑+4HCl↑+3S↓;正確;SO2與干燥的NH3不反應,而HCl和干燥的NH3反應生成白煙.
;2S2Cl2+2H2O=SO2↑+4HCl↑+3S↓;正確;SO2與干燥的NH3不反應,而HCl和干燥的NH3反應生成白煙.
點評 本題考查了位置、結構與性質關系的綜合應用,題目難度中等,特點各元素為解答關鍵,試題知識點較多、綜合性較強,充分考查了學生的分析、理解能力及綜合應用所學知識的能力,(5)為難點、易錯點,需要根據X、Y的性質推斷二者組成,然后結合質量守恒定律寫出反應的方程式.


 學練快車道快樂假期暑假作業新疆人民出版社系列答案
學練快車道快樂假期暑假作業新疆人民出版社系列答案 浙大優學小學年級銜接導與練浙江大學出版社系列答案
浙大優學小學年級銜接導與練浙江大學出版社系列答案 小學暑假作業東南大學出版社系列答案
小學暑假作業東南大學出版社系列答案 津橋教育暑假拔高銜接廣東人民出版社系列答案
津橋教育暑假拔高銜接廣東人民出版社系列答案 波波熊暑假作業江西人民出版社系列答案
波波熊暑假作業江西人民出版社系列答案科目:高中化學 來源: 題型:解答題
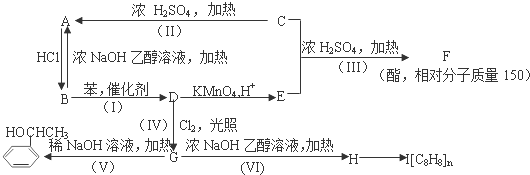
 ;I
;I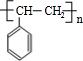 .
. .
. .
.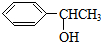 的同分異構體甚多,其中屬于酚的同分異構體共有9種,這些同分異構體中,在核磁共振氫譜中有四個吸收峰的同分異構體的結構簡式為:
的同分異構體甚多,其中屬于酚的同分異構體共有9種,這些同分異構體中,在核磁共振氫譜中有四個吸收峰的同分異構體的結構簡式為: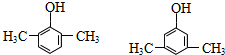 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (1)某同學做如下實驗,以檢驗反應中的能量變化.
(1)某同學做如下實驗,以檢驗反應中的能量變化.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
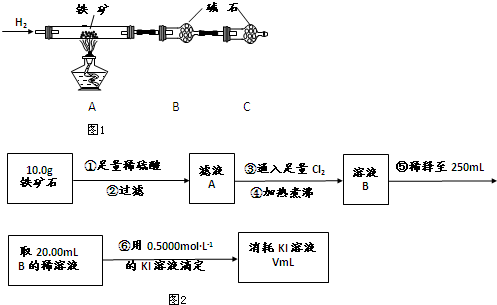
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 200 | B. | 770 | C. | 290 | D. | 292 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 稀HNO3 | B. | CO | C. | CH3CH2CH2OH | D. | 稀H2SO4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com