
【題目】Ⅰ、目前已開發出用電解法制取ClO2的新工藝。
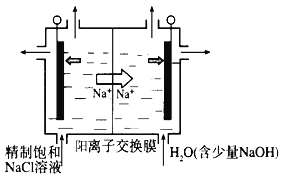
(1)圖中用石墨做電極,在一定條件下電解飽和食鹽水制取ClO2。則陽極產生ClO2的電極反應式為___________________________________________。
(2)電解一段時間,當陰極產生的氣體體積為112 mL(標準狀況)時,停止電解。通過陽離子交換膜的陽離子的物質的量為________mol。
Ⅱ、某研究性學習小組根據反應:2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4 + 8H2O設計如下原電池,其中甲、乙兩燒杯中各物質的物質的量濃度均為 1 mol·L-1,溶液的體積均為200 mL,鹽橋中裝有飽和K2SO4溶液。

回答下列問題:
(3)此原電池的正極是石墨________(填“a”或“b”)。
(4)電池工作時,鹽橋中的SO![]() 移向________(填“甲”或“乙”)燒杯。
移向________(填“甲”或“乙”)燒杯。
(5)甲燒杯中的電極反應式為_______________________。
(6)若不考慮溶液的體積變化,MnSO4濃度變為1.5 mol·L-1,則反應中轉移的電子為____mol。
【答案】 Cl--5e-+2H2O===ClO2↑+4H+ 0.01 a 乙 MnO![]() +5e-+8H+===Mn2++4H2O 0.5
+5e-+8H+===Mn2++4H2O 0.5
【解析】試題分析:Ⅰ、(1)陽極Cl-失去電子發生氧化反應生成ClO2。(2)水電離產生的H+在陰極上放電產生氫氣,轉移電子的物質的量n=2n(H2)=2×(0.112 L÷22.4 L·mol-1)=0.01 mol,根據電荷守恒分析轉移陽離子的物質的量。Ⅱ、(3)原電池中發生氧化反應的一極是負極,發生還原反應的一極是正極;(4)原電池中陽離子移向正極、陰離子移向負極;(5)甲燒杯中MnO![]() 得電子被還原為Mn2+; (6) MnSO4濃度由1 mol·L-1變為1.5 mol·L-1,則生成MnSO4的物質的量是0.2L×(1.5 mol·L-1-1 mol·L-1)=0.1mol,根據電極反應式計算轉移電子的物質的量。
得電子被還原為Mn2+; (6) MnSO4濃度由1 mol·L-1變為1.5 mol·L-1,則生成MnSO4的物質的量是0.2L×(1.5 mol·L-1-1 mol·L-1)=0.1mol,根據電極反應式計算轉移電子的物質的量。
解析:Ⅰ、(1)陽極Cl-失去電子發生氧化反應生成ClO2,電極反應是Cl--5e-+2H2O===ClO2↑+4H+。(2)水電離產生的H+在陰極上放電產生氫氣,轉移電子的物質的量n=2n(H2)=2×(0.112 L÷22.4 L·mol-1)=0.01 mol,溶液中陽離子全是+1價離子,根據電荷守恒,通過陽離子交換膜的陽離子的物質的量為0.01mol。Ⅱ、(3)原電池中發生氧化反應的一極是負極,發生還原反應的一極是正極;根據電池總反應方程式,KMnO4得電子發生還原反應,FeSO4失電子發生氧化反應;所以原電池的正極是石墨a; (4)原電池中陽離子移向正極、陰離子移向負極,所以鹽橋中的SO![]() 移向乙燒杯;(5)甲燒杯中MnO
移向乙燒杯;(5)甲燒杯中MnO![]() 得電子被還原為Mn2+,電極反應是MnO
得電子被還原為Mn2+,電極反應是MnO![]() +5e-+8H+===Mn2++4H2O; (6) MnSO4濃度由1 mol·L-1變為1.5 mol·L-1,則生成MnSO4的物質的量是0.2L×(1.5 mol·L-1-1 mol·L-1)=0.1mol,根據電極反應MnO
+5e-+8H+===Mn2++4H2O; (6) MnSO4濃度由1 mol·L-1變為1.5 mol·L-1,則生成MnSO4的物質的量是0.2L×(1.5 mol·L-1-1 mol·L-1)=0.1mol,根據電極反應MnO![]() +5e-+8H+===Mn2++4H2O,生成0.1mol MnSO4轉移電子的物質的量是0.5mol。
+5e-+8H+===Mn2++4H2O,生成0.1mol MnSO4轉移電子的物質的量是0.5mol。


科目:高中化學 來源: 題型:
【題目】用圖中所示裝置進行實驗,實驗現象與預測不一致的是( )
①中的物質 | ②中的物質 | 預測現象 | |
A | 飽和亞硫酸 | 藍色石蕊試液 | ②中溶液先變紅色又褪色 |
B | 飽和氯水 | 濕潤紅紙條 | ②中紅紙條褪色 |
C | 濃雙氧水 | H2S溶液 | ②中有淡黃色沉淀 |
D | 濃氨水 | 濃鹽酸 | ③中有白煙 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向某密閉容器中充入1 mol CO和2 mol H2O(g),發生反應:CO+H2O(g)![]() CO2+H2。當反應達到平衡時,CO的體積分數為x。若維持容器的體積和溫度不變,起始物質按下列四種配比充入該容器中,達到平衡時CO的體積分數大于x的是( )
CO2+H2。當反應達到平衡時,CO的體積分數為x。若維持容器的體積和溫度不變,起始物質按下列四種配比充入該容器中,達到平衡時CO的體積分數大于x的是( )
A. 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2
B. 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2
C. 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2
D. 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】FeCl3可通過反應 3FeCl2+HNO3+3HCl→3FeC13+NO↑+2H2O 制得。
完成下列填空:
(1)上述反應式中由三原子組成的極性分子,其電子式為____________。
(2)限于上述反應式,原子最外層有3個未成對電子的主族元素是__________(填寫名稱);與它同周期、非金屬性比它強的元素有_________(填寫元素符號),非金屬性較強的理由是___________________________________(請運用原子結構的知識解釋)。
(3)上述反應中若有0.12mol電子發生轉移,則可生成NO氣體__________L(標準狀況)。
(4)FeCl3濃溶液可用于蝕刻金屬銅制作電路板。寫出該反應的化學反應方程式。_____________________,實驗室里,某同學將FeCl3(s)置于燒杯中,加水溶解配制溶液,為了加速固體溶解,邊攪拌邊加熱,發現燒杯中出現渾濁。請用平衡移動原理解釋出現渾濁的原因。_______________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.已知某純堿試樣中含有雜質NaCl,為了確定試樣中純堿的質量分數,可測定其在化學反應中生成CO2的質量,實驗裝置如下(鐵架臺及夾持儀器均已省略)。
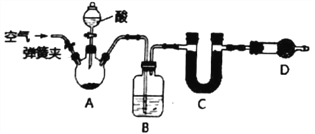
完成下列填空:
(1)B裝置中的試劑是_____________,作用是_____________________________。
(2)D裝置的作用是___________________________________。
II.測定試樣中純堿質量分數的某次實驗步驟如下:①將10.000g純堿試樣放入A中 ②稱量C(U型管+堿石灰,下同),質量為l05.160g ③使用分液漏斗滴加足量的酸,使充分反應 ④打開A的彈簧夾,緩緩鼓入一定量的空氣 ⑤再次稱量C ⑥重復步驟④和⑤,最后得到C的質量為109.l66g。
(3)步驟③中,滴加的酸最好選用________。
a、濃硝酸 b、稀鹽酸 c、濃硫酸 d、稀硫酸
當看到____________________現象時即可進行第④步操作。
(4)步驟⑥的目的是_______________________________________________。
(5)由實驗數據可知,試樣中純堿的質量分數為_________________(保留3位小數)。
(6)甲同學用上述裝置測定某試樣中純堿的質量分數,結果偏高,請幫助他找出造成實驗誤差的原因。_______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦酸鋇粉體是電子陶瓷元器件的重要基礎原料,其制備工藝流程圖如下:
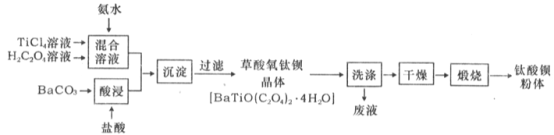
(l)草酸中碳元素的化合價為_____。
(2)為提高BaCO3的酸浸速率,可采取的措施為_____ (寫出一條)。
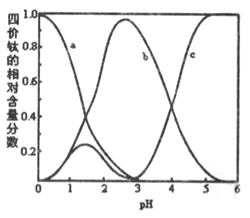
(3)“混合溶液”環節,鈦元素在不同pH下主要以TiOC2O4、TiO(C2O4)22-、和TiO(OH)+三種形式存在,如圖所示。實際制備工藝中,先用氨水調節混合溶液的pH于2.5~3之間,再進行“沉淀”,則上圖中曲線a對應鈦的形式為________(填化學式):寫出“沉淀”時的離子方程式:__________。
(4)草酸氧鈦鋇晶體經蒸餾水數次洗滌后,證明它已被洗滌干凈的實驗方案____________。
(5)工業上TiCl4和BaCO3通常用如下方法制備:
①先將金紅石(TiO2)與過量焦炭混合,再通人Cl2并加熱到900℃制取TiCl4。請寫出該法制取TiCl4的化學方程式:__________________________________。
②BaCO3是將重晶石(主要成分為BaSO4)浸泡在Na2CO3溶液中足夠長時間來制備。請問Na2CO3溶液的濃度至少要大于______ mol·L-1才能開始轉化。(已知常溫下:Ksp(BaSO4)=1.0×10-10(mol·L-1)2,Ksp(BaCO3) =2.58×10-9(mol·L-1)2,忽略CO32-的水解)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下的密閉容器中發生反應:C(s)+CO2(g)=2CO(g).下列說法不正確的是( )
A.將碳塊磨成粉末可加快反應速率
B.增加碳的質量可加快反應速率
C.升高溫度可加快反應速率
D.容器體積不變時,向容器中充入氦氣,反應速率不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列描述中正確的是( )
A. CS2為空間構型為V形的極性分子
B. 雙原子或多原子形成的氣體單質中,一定有σ鍵,可能有π鍵
C. 氫原子電子云的一個小黑點表示一個電子
D. HCN、SiF4和SO32-的中心原子均為sp3雜化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】環氧氯丙烷是制備環氧樹脂的主要原料,工業上有不同的合成路線,以下是其中的一種(有些反應未注明條件)。
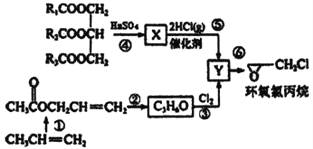
完成下列填空:
(1)X的結構簡式_________Y中的不含氧官能團的名稱為____________________
(2)反應①中的合成原料還有O2和醋酸及催化劑,寫出該反應的化學方程式______________________。
(3)下列說法不正確的是__________
A.如R1、R2、R3不完全相同,則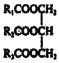 是混合物
是混合物
B.Y的結構簡式是不能確定的,可能有兩種不同的結構
C.反應②④⑤⑥都是取代反應
D.X與乙醇不是同系物,兩者都能使酸性KMnO4溶液褪色
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com