
部分弱酸的電離平衡常數如下表:
弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
電離平衡常數(25 ℃) | Ka=1.77 ×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(1)在溫度相同時,各弱酸的Ka值與酸性的相對強弱的關系為________________。
(2)室溫下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3溶液的pH由大到小的關系為______________________。
(3)濃度均為0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO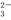 、CO
、CO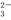 、HSO
、HSO 、HCO
、HCO 濃度從大到小的順序為____________________________。
濃度從大到小的順序為____________________________。
(4)下列離子方程式正確的是________(填字母)。
a.2ClO-+H2O+CO2=2HClO+CO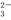
b.2HCOOH+CO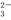 =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-=2HCOOH+SO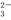
d.Cl2+H2O+2CO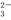 =2HCO
=2HCO +Cl-+ClO-
+Cl-+ClO-
(5)常溫下,pH=3的HCOOH溶液與pH=11的NaOH溶液等體積混合后,溶液中離子濃度由大到小的順序為________________________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2017屆福建省高三上學期第二次月考化學試卷(解析版) 題型:實驗題
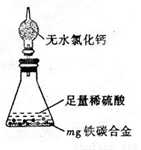
有某鐵碳合金,某化學興趣小組為了測定鐵碳合金中鐵的質量分數,并探究濃硫酸的某些性質,設計了下圖所示的實驗裝置和實驗方案(夾持儀器已省略),請你參與此項活動并回答相應問題。

Ⅰ 探究濃硫酸的某些性質
(1)按圖示的 連接裝置,檢查裝置的氣密性,稱量E的質量。
連接裝置,檢查裝置的氣密性,稱量E的質量。
(2)將m g鐵碳合金樣品放入A中,再加入適量的濃硫酸。儀器A的名稱為________。
未點燃酒精燈前,A、B均無明顯現象,其原因是: _。
(3)點燃酒精燈一段時間后,A、B中可觀察到明顯的現象。
寫出A中發生反應的化學方程式_______________________(任寫一個)。B中的現象是______________,由此可得到濃硫酸具有____________性。
(4)隨著反應的進行,A中還可能發生某些離子反應。寫出相應的離子方程式____________(任寫一個)。
(5)反應一段時間后,從A中逸出氣體的速率仍然較快,除因溫度較高,反應放熱外,還可能的原因是______________________。
Ⅱ 測定鐵的質量分數
(6)待A中不再逸出氣體時,停止加熱,拆下E并稱重。E增重b g。
鐵碳合金中鐵的質量分數為_____________________(寫表達式)。
(7)某同學認為上述方法較復雜,使用下圖所示的裝置和其它常用實驗儀器測定某些數據即可。為了快速和準確的計算出鐵的質量分數,最簡便的實驗操作是___________(填寫代號)。
A. 用排水法測定H2的體積
B. 反應 結束后,過濾、洗滌、干燥、稱量殘渣的質量
結束后,過濾、洗滌、干燥、稱量殘渣的質量
C. 測定反應前后裝置和藥品的總質量
查看答案和解析>>
科目:高中化學 來源:2016-2017陜西西安長安區一中重點班高一12月考化學卷(解析版) 題型:選擇題
實驗室中需要配制2mol/L的NaCl溶液480mL,配制時應選用的容量瓶的規格和稱取的NaCl質量分別是 ( )
)
A.480mL,56.2g B.500mL,56.2g
C.500mL,58.5g D.任意規格,56.2g
查看答案和解析>>
科目:高中化學 來源:2016-2017陜西西安長安區一中實驗班高一12月考化學卷(解析版) 題型:選擇題
在Al2(SO4)3 和MgSO4 的混合溶液中,滴加NaOH 溶液,生成沉淀的量與滴入NaOH溶液的體積關系如圖所示,則原混合液中 Al2(SO4)3 與MgSO4 的物質的量濃度之比為( )
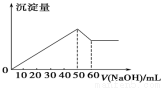
A. 1∶2 B. 2∶1 C. 6∶1 D. 3∶1
查看答案和解析>>
科目:高中化學 來源:2016-2017陜西西安長安區一中實驗班高一12月考化學卷(解析版) 題型:選擇題
NA 為阿伏加德羅常數,下列說法不正確的是( )
A. 58.5 克 NaCl 中,Na+最外層電子數為 8NA
B. Na2O、Na2O2 中陰陽離子個數均為 1:2
C. 標準狀況下11.2升Cl2 與足量Fe充分反應轉移NA個電子
D. 2.7克Al分別與足量稀鹽酸和足量NaOH溶液反應,生成氫氣質量不相等
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省高二上期中化學試卷(解析版) 題型:選擇題
將等物質的量濃度的CuSO4溶液和NaCl溶液等體積混合后,用石墨電極進行電解,電解過程中,溶液pH隨時間t變化的曲線如圖,則下列說法正確的是( )

A.陽極產物一定是Cl2,陰極產物一定是Cu
B.BC段表示在陰極上是H+放電產生了H2
C.AB、BC段陰極反應都為Cu2+ + 2e-= Cu
D.CD段表示陽極上OH一放電破壞了水的電離平衡,產生了H+
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省高二上期中化學試卷(解析版) 題型:選擇題
根據下圖海水綜合利用的工業流程圖,判斷下列說法正確的是( )
已知:MgCl2·6H2O受熱生成Mg(OH)Cl和HCl氣體等。
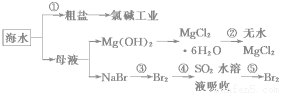
A.除去粗鹽中雜質(Mg2+、SO42-、Ca2+),加入的藥品順序為:NaOH溶液→Na2CO3溶液→BaCl2溶液→過濾后加鹽酸
B.在過程②中將MgCl2·6H2O灼燒即可制得無水MgCl2
C.從能量轉換角度來看,氯堿工業中的電解飽和食鹽水是一個將化學能轉化為電能的過程
D.從第③步到第⑤步的目的是為了制取并提純Br2
查看答案和解析>>
科目:高中化學 來源:2017屆安徽馬鞍山二中安師大附中高三12月聯考化學卷(解析版) 題型:填空題
鐵觸媒是重要的催化劑,CO易與鐵觸媒作用導致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化學反應方程式為:[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3。
請回答下列問題:
(1)基態Fe原子的價電子排布圖為 。
(2)Fe(CO)5又名羰基鐵,常溫下為黃色油狀液體,則Fe(CO)5的晶體類型是 ,與CO互為等電子體的分子的分子式為 。
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的雜化類型是 ,配體中提供孤對電子的原子是 。
(4)用[Cu(NH3)2]OOCCH3除去CO的反應中,肯定有 形成。
a.離子鍵 b.配位鍵 c.非極性鍵 d.σ鍵
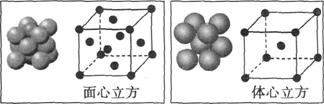
(5)單質鐵的晶體在不同溫度下有兩種堆積方式,晶胞分別如圖所示,面心立方晶胞和體心立方晶胞中實際含有的鐵原子個數之比為 ,面心立方堆積與體心立方堆積的兩種鐵晶體的晶胞單位分別為a pm和b pm,則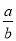 = 。
= 。
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省淮安市高三12月考試化學試卷(解析版) 題型:選擇題
下列裝置或操作能達到實驗目的的是
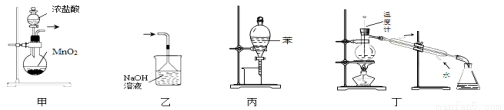
A.用裝置甲制取氯氣 B.用乙裝置除去氯氣中的HCl氣體
C.用丙裝置萃取溴水中的溴單質 D.用丁裝置分離乙酸與乙醇
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com