
【題目】微型化學實驗能有效減少污染,節約藥品。下圖中,某學生在襯有一張白紙的玻璃片上放置表面皿,在表面皿上的不同位置分別滴加濃度為0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,在表面皿中心處放置2小粒KMnO4晶體,并滴加一滴濃鹽酸,立即將表面皿蓋好。可見KMnO4晶體很快溶解,并產生氣體
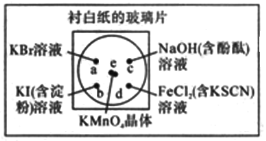
(1)①寫出化學實驗室中用MnO2制取Cl2的化學方程式______________________________。
②完成本實驗中制取Cl2的化學方程式:
___________KMnO4+__________HCl(濃)——______KCl+________MnCl2+____Cl2↑+______ _______
如該反應中消耗還原劑的物質的量為8mol,則電子轉移數目為_________________。
(2)b處的實驗現象為____________________________________________________。
c處的實驗現象為____________________________________________________。
(3)d處反應的離子方程式為____________________、____________________。
(4)通過該實驗能比較Cl2、FeCl3、KMnO4三種物質氧化性的強弱,其氧化性由強到弱的順序是_________________________________________。
【答案】MnO2+4HCl(濃) ![]() MnCl2+Cl2↑+2H2O 2 16 2 2 5 8 H2O 8NA b處溶液變藍色 c處溶液紅色褪去 2Fe2++ Cl2=2Fe3++ Cl- Fe3++3SCN-= Fe(SCN)3 KMnO4>Cl2>FeCl3
MnCl2+Cl2↑+2H2O 2 16 2 2 5 8 H2O 8NA b處溶液變藍色 c處溶液紅色褪去 2Fe2++ Cl2=2Fe3++ Cl- Fe3++3SCN-= Fe(SCN)3 KMnO4>Cl2>FeCl3
【解析】
(1)高錳酸鉀具有強氧化性,能把鹽酸氧化生成氯氣,自身被還原生成氯化錳,據此寫出反應方程式;高錳酸鉀是氧化劑鹽酸是還原劑,根據高錳酸鉀和參加氧化還原反應的鹽酸的計量數判斷氧化劑和還原劑的物質的量之比;
(2)b處氯氣能置換出碘,碘遇淀粉變藍色,c處氯氣和氫氧化鈉反應使酚酞紅色褪去;
(3)氯氣通入FeCl2溶液(含KSCN)中,會把亞鐵離子氧化成鐵離子,鐵離子和硫氰化鉀反應生成紅色的絡合物;
(4)依據氧化還原反應中氧化劑氧化性強于氧化產物的氧化性判斷解答
(1) 化學實驗室中用MnO2和濃鹽酸在加熱的條件下制備Cl2,方程式為MnO2+4HCl(濃) ![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2) 反應中KMnO4所含Mn元素化合價由+7價降低為MnCl2中+2價,共降低5價,HCl所含Cl元素化合價由-1價升高為氯氣中0價,共升高2價,化合價最小公倍數為10,故KMnO4的系數為2、Cl2的系數為5,根據Mn原子守恒可知MnCl2的系數為2,由K原子守恒可知KCl系數為2,根據Cl原子守恒HCl的系數為16,再由H原子守恒可知水的系數為8,故配平后為2KMnO4+16HCl(濃)![]() 2KCl+2MnCl2+5Cl2↑+8H2O;反應中KMnO4所含Mn元素化合價降低,KMnO4是氧化劑,HCl所含Cl元素化合價升高,HCl為還原劑,消耗HCl的物質的量為8mol時生成4molCl2,轉移4×2mol=8mol電子,個數為8NA;
2KCl+2MnCl2+5Cl2↑+8H2O;反應中KMnO4所含Mn元素化合價降低,KMnO4是氧化劑,HCl所含Cl元素化合價升高,HCl為還原劑,消耗HCl的物質的量為8mol時生成4molCl2,轉移4×2mol=8mol電子,個數為8NA;
(3)氯氣通入KI溶液(含淀粉)中,I-會被氧化成碘單質,碘單質遇淀粉變藍,故b處溶液變藍色;將 氯氣通入到滴有酚酞的氫氧化鈉溶液中,會發生反應 Cl2+2NaOH=NaCl+NaClO+H2O ,會消耗NaOH,紅色消失,故c處溶液紅色褪去;
(4) 氯氣通入FeCl2溶液(含KSCN)中,會把亞鐵離子氧化成鐵離子,鐵離子和硫氰化鉀反應生成紅色的絡合物,離子方程式為:2Fe2++ Cl2=2Fe3++ Cl-、Fe3++3SCN-= Fe(SCN)3;
(5)氧化還原反應中氧化劑氧化性強于氧化產物的氧化性,2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O中,高錳酸鉀為氧化劑,氯氣為氧化產物,所以氧化性:KMnO4>Cl2;氯氣與二價鐵離子反應生成三價鐵離子,則氧化性:Cl2>FeCl3;所以氧化性順序為:KMnO4>Cl2>FeCl3;


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】影響化學反應速率的因素很多,某化學小組用實驗的方法進行探究。
I.探究活動一:
備選藥品:鐵片、鋅片、0.5mol/LH2SO4、1.5mol/LH2SO4、18.4mol/LH2SO4
甲同學研究的實驗報告
實驗步驟 | 現象 | 結論 |
①分別取等體積的1.5mol/L的硫酸于兩支試管中; ②_____________________。 | 反應速率: 鋅>鐵 | 金屬的性質越活潑,反應速率越快 |
(1)甲同學實驗報告中的實驗步驟②為__________________________________。
(2)甲同學的實驗目的是_______________________________;要得出正確的實驗結論,還需控制的實驗條件是__________________。
乙同學為了定量研究濃度對化學反應速率的影響,利用如圖所示裝置進行實驗:

(3)乙同學在實驗中需要測定的數據是_________________________。
(4)乙同學不會選用___________mol/L硫酸完成該實驗,理由是_________________。
II.探究活動二:
備選藥品:0.1mol/LNa2S2O3溶液、0.2mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、0.2mol/LH2SO4溶液。
已知:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O
實驗 編號 | Na2S2O3用量 | H2SO4用量 | 溫度(℃) |
① | 0.1mol/L5mL | 0.1mol/L5mL | 10 |
② | 0.2mol/L5mL | 0.2mol/L5mL | 25 |
③ | 0.1mol/L5mL | 0.1mol/L5mL | 25 |
④ | 0.1mol/L5mL | 0.1mol/L5mL | 40 |
(1)若想探究溫度對化學反應速率的影響,可選的實驗編號有___________。
(2)若想探究濃度對化學反應速率的影響,可選的實驗編號有___________。
(3)在該實驗過程中,需要觀察和記錄________________,來比較化學反應速率的快慢。
(4)Na2S2O3在堿性溶液中可被I2氧化為Na2SO4,寫出該反應的離子方程式___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】藥物中間體Q、醫用材料PVA的合成路線如圖。
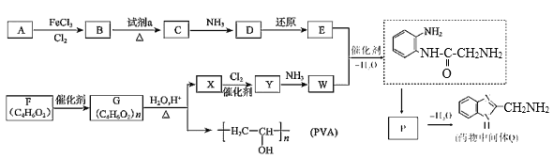
已知:①R-Cl+2NH3→R-NH2+NH4Cl
②R-NO2![]() R-NH2
R-NH2
③-NH2+![]()
(1)A的分子式是________。
(2)B→C是硝化反應,試劑a是________(填名稱)。
(3)C→D轉化的化學方程式是________。
(4)E的結構簡式是________。
(5)F含有的官能團是________(填名稱),與其含有相同官能團的同分異構體還有________種。
(6)G→X的化學方程式是________。
(7)W能發生縮聚反應,形成的高分子結構簡式是________。
(8)P的結構簡式是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下是工業上制取純硅的一種方法。

請回答下列問題(各元素用相應的元素符號表示):
(1)在上述生產過程中,屬于置換反應的有____(填反應代號);
(2)寫出反應③的化學方程式____;
(3)化合物W的用途很廣,通常可用作建筑工業和造紙工業的黏合劑,可作肥皂的填充劑,是天然水的軟化劑。將石英砂和純堿按一定比例混合加熱至1 373~1 623 K反應,生成化合物W,其化學方程式是____;
(4)A、B、C三種氣體在“節能減排”中作為減排目標的一種氣體是___(填化學式);分別通入W溶液中能得到白色沉淀的氣體是___(填化學式);
(5)工業上合成氨的原料H2的制法是先把焦炭與水蒸氣反應生成水煤氣,再提純水煤氣得到純凈的H2,提純水煤氣得到純凈的H2的化學方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用石油裂化和裂解過程得到的乙烯、丙烯來合成丙烯酸乙酯的路線如圖:
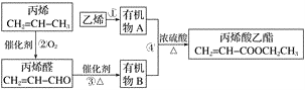
根據以上材料和你所學的化學知識,回答下列問題:
(1)乙烯的電子式是_____,官能團的名稱是______。
(2)除去甲烷中的乙烯所用的試劑是____(填序號)。
A.稀硫酸
B.溴的四氯化碳溶液
C.水
D.酸性高錳酸鉀溶液
(3)反應①的化學方程式是______,反應類型是_____。
(4)反應④的化學方程式是______,反應類型是_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學方程式中,不能正確表達反應顏色變化的原因的是
A. 銅久置空氣中表面出現綠色固體:2Cu+O2+CO2+H2O═Cu2(OH)2CO3
B. 某種火箭發射階段有少量N2O4,逸出,產生紅色氣體:N2O4![]() 2NO2
2NO2
C. FeSO4·7H2O在空氣中久置變黃:2FeSO4·7H2O![]() Fe2O3+SO2↑+SO3↑+14H2O
Fe2O3+SO2↑+SO3↑+14H2O
D. SO2通入KMnO4溶液中,溶液紫色逐漸褪去:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4十2H2SO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】次磷酸(H3PO2)是一種精細磷化工產品,有強還原性。已知:①2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑,②H3PO2+NaOH(足量)=NaH2PO2+H2O。下列推斷不正確的是
A. H3PO2的結構式為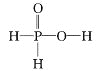
B. H3PO2具有強還原性,在空氣中可能被氧化成磷酸
C. NaH2PO2是酸式鹽
D. 每消耗1mol P4,反應①中轉移6mol電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組的同學設計實驗制備CuBr(白色結晶性粉末,微溶于水,不溶于乙醇等有機溶劑),實驗裝置(夾持、加熱儀器略)如圖所示。
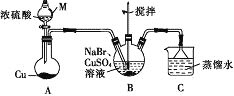
(1)儀器M的名稱是________。
(2)若將M中的濃硫酸換成70%的H2SO4,則圓底燒瓶中的固體試劑為______(填化學式)。
(3)B中發生反應的化學方程式為_______,能說明B中反應已完成的依據是_____。若B中Cu2+仍未完全被還原,適宜加入的試劑是_______(填標號)。
a.液溴 b.Na2SO4 c.鐵粉 d.Na2S2O3
(4)下列關于過濾的敘述不正確的是_______ (填標號)。
a.漏斗末端頸尖可以不緊靠燒杯壁
b.將濾紙潤濕,使其緊貼漏斗內壁
c.濾紙邊緣可以高出漏斗口
d.用玻璃棒在漏斗中輕輕攪動以加快過濾速率
(5)洗滌時,先用裝置C中的吸收液清洗,其目的是_______,再依次用溶解SO2的乙醇、乙醚洗滌的目的是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Fe2O3和Cu2O都是紅色粉末,常用作顏料.實驗小組通過實驗來探究某一紅色粉末中Fe2O3和Cu2O的含量(不含其他物質)。
已知:Cu2O+H2SO4=Cu+Cu SO4+H2O
探究過程如下:
取少量該粉末放入 足量稀硫酸中,粉末完全溶解。
(1)①若滴加KSCN試劑后溶液不變為紅色,則Fe2O3和Cu2O的物質的量之比為________。
②實驗小組發現可通過對反應后溶液的稱量來獲得綠礬晶體(FeSO4·7H2O),設計了簡單的流程來完成綠礬的制備:
混合液![]() 過濾
過濾![]() 一系列操作
一系列操作![]() 綠礬晶體(FeSO4·7H2O)
綠礬晶體(FeSO4·7H2O)
試劑a為_____________(填化學式),“一系列操作”為__________、__________、過濾、洗滌、干燥。
(2)測定Cu2O的質量分數:另取一種由Fe2O3和Cu2O組成的固體混合物9.28g,將其放在空氣中充分加熱(只發生Cu2O→CuO的反應),待質量不再變化時,測得質量為9.60g,則固體混合物中Cu2O的質量分數為_________________(保留三位有效數字)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com