
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ②③ |
分析 標況下2.24LNO的物質的量為:$\frac{2.24L}{22.4L/mol}$=0.1mol,生成0.1molNO轉移電子的物質的量為:0.1mol×(5-2)=0.3mol;銅和鎂都是2價金屬,根據電子守恒可知金屬的物質的量為:$\frac{0.3mol}{2}$=0.15mol,固體和硝酸恰好完全反應,反應生成硝酸銅、硝酸鎂,根據N原子守恒,200mL該硝酸溶液中含有硝酸的物質的量為:0.15mol×2+0.1mol=0.4mol,根據c=$\frac{n}{V}$計算出硝酸的物質的量濃度;
銅與鎂在空氣中加熱生成CuO、MgO,得到固體中含有氧元素的物質的量與金屬的物質的量相等,則得到固體的質量=金屬質量+氧元素質量.
解答 解:標況下2.24LNO的物質的量為:$\frac{2.24L}{22.4L/mol}$=0.1mol,生成0.1molNO轉移電子的物質的量為:0.1mol×(5-2)=0.3mol;銅和鎂都是2價金屬,根據電子守恒可知金屬的物質的量為:$\frac{0.3mol}{2}$=0.15mol,固體和硝酸恰好完全反應,反應生成硝酸銅、硝酸鎂,根據N原子守恒,200mL該硝酸溶液中含有硝酸的物質的量為:0.15mol×2+0.1mol=0.4mol,該硝酸溶液的濃度為:$\frac{0.4mol}{0.2L}$=2mol/L,故①正確、②錯誤;
銅與鎂在空氣中加熱生成CuO、MgO,得到固體中含有氧元素的物質的量與金屬的物質的量相等,則得到固體的質量為:$\frac{11.2g}{2}$+16g/mol×0.15mol=8g,故③正確、④錯誤;
根據分析可知,正確的為①③,
故選B.
點評 本題考查了混合物反應的計算,題目難度中等,明確發生反應實質為解答關鍵,注意掌握質量守恒定律、電子守恒在化學計算中的應用,試題培養了學生的分析能力及化學計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | 1000mL,106g | B. | 1000mL,286g | C. | 950mL,100.7g | D. | 950mL,271.7g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵制品銹蝕時主要發生析氫腐蝕 | |
| B. | 施用適量石膏可以降低鹽堿地(含較多NaCl、Na2CO3)的堿性 | |
| C. | 電鍍廠未經處理的廢水可以直接用來灌溉農田 | |
| D. | 將水壩的鋼鐵閘門與直流電的正極相連可以防閘門腐蝕 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
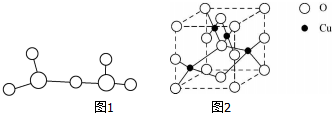
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 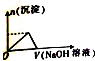 | B. | 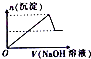 | C. | 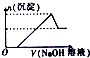 | D. |  |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.4 g乙烯與丙烯的混合氣體含有NA個碳原子 | |
| B. | 精煉銅,若陽極失去2NA個電子,則陰極增重64 g | |
| C. | 在1 L 0.1mol/L 的Na2CO3溶液中,陰離子總數小于0.1NA | |
| D. | 將1 L 2 mol/L 的FeCl3溶液加入到沸水中,加熱使之完全反應,所得氫氧化鐵膠體粒子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO+H2O(g)═CO2+H2 | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | 2Na2O2+2H2O═4NaOH+O2↑ | D. | 2F2+2H2O═4HF+O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3:2 | B. | 2:3 | C. | 4:1 | D. | 1:4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com