
已知A、B、C、D、E、F、G七種元素,它們的原子序數依次增大,A在所有元素中原子半徑最小,B原子核外電子有6種不同運動狀態;D與C、E均相鄰;A、D、E三種元素的原子序數之和為25;E
2-和F
+有相同的核外電子排布;G的質子數是25.請回答下列問題:
(1)寫出元素C的基態原子外圍電子排布式
;B,C,D三種元素分別形成的最簡單氫化物的沸點最高的是
(用化學式表示).
(2)由上述元素中的兩種元素組成的一種陰離子與D的一種同素異形體分子互為等電子體.該陰離子化學式
.
(3)由上述元素組成的屬于非極性分子且VSEPR為直線形的微粒的電子式
(任寫一種).
(4)M是由4個C元素的原子組成的一種不穩定的多原子單質分子.M分子中C原子雜化方式為sp
3,M分子的空間構型為
.
(5)某一次性電池的比能量和可儲存時間均比普通干電池優良,通用于大電流和連續放電,是民用電池的升級換代產品之一.它的負極材料是Zn.正極材料是G的一種常見氧化物,電解質是KOH.該電池的正極反應式為
.
(6)由上述元素中電負性最大的元素和第一電離能最小的元素形成的某化合物N的晶胞如圖所示.化合物N與氧化鈣相比.晶格能較小的是
(填化學式).已知該化合物的晶胞邊長為a pm,則該化合物的密度為
g?cm
-3(只要求列出算式.不必汁算出數值.阿伏加德羅常數的數值為N
A,1pm=10
-10cm).

 已知A、B、C、D、E、F、G七種元素,它們的原子序數依次增大,A在所有元素中原子半徑最小,B原子核外電子有6種不同運動狀態;D與C、E均相鄰;A、D、E三種元素的原子序數之和為25;E2-和F+有相同的核外電子排布;G的質子數是25.請回答下列問題:
已知A、B、C、D、E、F、G七種元素,它們的原子序數依次增大,A在所有元素中原子半徑最小,B原子核外電子有6種不同運動狀態;D與C、E均相鄰;A、D、E三種元素的原子序數之和為25;E2-和F+有相同的核外電子排布;G的質子數是25.請回答下列問題: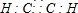 、
、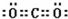 ,故答案為:
,故答案為: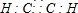 、
、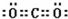 ;
;

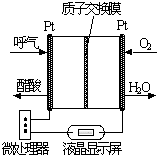 研究NO2、SO2、CO等大氣污染氣體的測量及處理具有重要意義.
研究NO2、SO2、CO等大氣污染氣體的測量及處理具有重要意義.