
【題目】(4)+6價鉻的化合物毒性較大,常用NaHSO3將廢液中的Cr2O72還原成Cr3+,該反應的離子方程式為______________。
科目:高中化學 來源: 題型:
【題目】在下列有機物中,經催化加氫后不能生成2-甲基戊烷的是
A.CH3C(CH3)=CHCH2CH3 B.CH2=C(CH3)CH2CH2CH3
C.CH3CH=CHCH(CH3)CH3 D.CH2=CHCH(CH3)CH2CH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)把0.2mol X氣體和0.4mol Y氣體混合于2L密閉容器中,使它們發生如下反應:![]() 末生成0.3mol W。若測知Z的濃度變化表示的反應速率為0.05mol
末生成0.3mol W。若測知Z的濃度變化表示的反應速率為0.05mol ![]() 。計算:
。計算:
①前2min內用Y 的濃度變化表示的反應速率為 ![]()
②化學方程式中n的值是 。
(2)在一定溫度下,將4mol SO2與2mol O2放入4L的密閉容器中,在一定條件下反應,2SO2+O2![]() 2SO3。10min 時達到平衡狀態。此時容器內壓強比反應前減少20%,計算SO2的轉化率為 。
2SO3。10min 時達到平衡狀態。此時容器內壓強比反應前減少20%,計算SO2的轉化率為 。
(3)某溫度時在2L容器中A、B、C 三種氣態物質的物質的量(n)隨時間(l)變化的曲線如圖所示,由圖中數據分析:

①該反應的化學方程式為
②下列敘述能說明上述反應達到平衡狀態的是 。
A、混合氣體的總物質的量不隨時間的變化而變化
B、相同時間內消耗2n mol 的A的同時生成4nmol 的C
C、混合氣體的總質量不隨時間的變化而變化
D、容器內壓強不再發生變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】焦亞硫酸鈉(Na2S2O5)是常用的食品抗氧化劑之一。某研究小組進行如下實驗:
實驗一 焦亞硫酸鈉的制取
采用下圖裝置(實驗前已除盡裝置內的空氣)制取Na2S2O5。裝置Ⅱ中有Na2S2O5晶體析出,發生的反應為Na2SO3+SO2=Na2S2O5
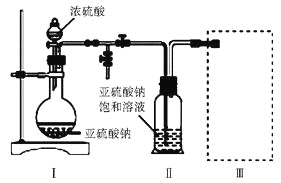
(1)裝置Ⅰ中產生氣體的化學方程式為____________________________。
(2)要從裝置Ⅱ中獲得已析出的晶體,可采取的分離方法是____________。
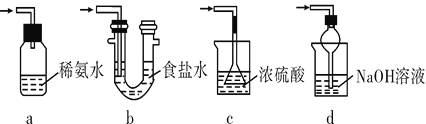
(3)裝置Ⅲ用于處理尾氣,可選用的最合理裝置(夾持儀器已略去)為______(填字母)。
實驗二 焦亞硫酸鈉的性質
Na2S2O5溶于水即生成NaHSO3。
(4)證明NaHSO3溶液中HSO![]() 的電離程度大于水解程度,可采用的實驗方法是________(填字母)。
的電離程度大于水解程度,可采用的實驗方法是________(填字母)。
a.測定溶液的pH
b.加入Ba(OH)2溶液
c.加入鹽酸
d.加入品紅溶液
e.用藍色石蕊試紙檢測
(5)檢驗Na2S2O5晶體在空氣中已被氧化的實驗,是檢驗__________的存在(填離子符號)。
實驗三 葡萄酒中抗氧化劑殘留量的測定
(6)葡萄酒常用Na2S2O5作抗氧化劑。測定某葡萄酒中抗氧化劑的殘留量(以游離SO2計算)的方案如下:
(已知:滴定時反應的化學方程式為SO2+I2+2H2O=H2SO4+2HI)

①按上述方案實驗,消耗標準I2溶液25.00 mL,該次實驗測得樣品中抗氧化劑的殘留量(以游離SO2計算)為____________g·L-1。
②在上述實驗過程中,若有部分HI被空氣中氧化氧化,則測得結果________(填“偏高”“偏低”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 配置一定物質的量濃度的溶液時,需要用到玻璃棒、膠頭滴管
B. 用濕潤的pH試紙測量稀氫氧化鈉溶液的pH,測量值偏大
C. 可用焰色反應鑒別氯化鈉和碳酸鈉
D. 用分液的方法從含有少量氯化鈉的硝酸鉀溶液中提取硝酸鉀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(11分)請回答下列問題:
(1)已知:N2、O2分子中化學鍵的鍵能分別是946kJ·mol-1、497 kJ·mol-1.N2(g)+O2(g)=2NO(g)△H=+180.0kJ·mol-1。則相同條件下破壞化學鍵需要吸收的能量為_______kJ。
(2)25℃時,pH=5的CH3COOH溶液中.由水電離出的氫離子濃度c(H+)=________ kJ·mol-1;往溶液中加入少量NaOH固體,則溶液中![]() _______(填“增大”、“減小”或“不變”),寫出表示該混合溶液中所有離子濃度之間的一個等式:_______。
_______(填“增大”、“減小”或“不變”),寫出表示該混合溶液中所有離子濃度之間的一個等式:_______。
(3)25℃下,向某Na2CO3溶液中加入稀鹽酸,其中含碳元素的各種微粒物質的量分數(φ)隨溶液pH變化的部分情況如圖所示。

①在同一溶液中,H2CO3、HCO3-、CO32-______(填“能”或“不能”)大量共存。
②當pH =7時,溶液中含碳元素的微粒主要為________。溶液中各種離子的物質的量濃度大小關系為______________。
③反應的CO32-+H2O![]() HCO3-+OH-的平衡常數Kh=______________________。
HCO3-+OH-的平衡常數Kh=______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】FeCl3在現代工業生產中應用廣泛。經查閱資料得知:無水FeCl3在空氣中易潮解,加熱易升華。工業上,向500—600℃的鐵屑中通入氯氣可生產無水氯化鐵;向熾熱鐵屑中通入氯化氫可以生產無水氯化亞鐵。某化學研究性學習小組模擬工業生產流程制備無水FeCl3并對產物做了如下探究實驗,請回答下列問題:
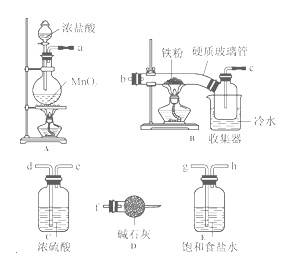
(1)裝置的連接順序為a → (用b、c…h表示)。
(2)i.A中裝置氣密性檢驗方法 。
ii.D中堿石灰的作用是 。
(3)反應結束后,生成的煙狀FeCl3大部分進入收集器,少量沉積在反應管B中硬質玻璃管的右端。要使沉積得FeCl3進入收集器,需進行的操作是 。
(4)反應一段時間后熄滅酒精燈,冷卻后將硬質玻璃管及收集器中的物質一并快速轉移至錐形瓶中,加入過量的稀鹽酸和少許植物油(反應過程中不振蕩),充分反應后,進行如下實驗:
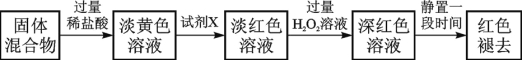
已知紅色褪去的同時有氣體生成,經檢驗為O2。該小組同學對紅色褪去的原因進行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液無明顯變化;第二份滴加試劑X,溶液出現紅色;第三份滴加稀鹽酸和BaCl2溶液,產生白色沉淀。
②另取同物質的量濃度的 FeCl3溶液滴加2滴試劑X,溶液變紅,再通入O2,無明顯變化。
實驗①說明 ;
實驗②的目的是 ;
得出結論: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com