

| 0.012mol×8 |
| 3 |
| 0.032mol×3 |
| 4mol/L |


科目:高中化學 來源: 題型:
 硝酸發生氧化還原反應的時候,一般硝酸濃度越稀,對應還原產物中氮的化合物越低.現有一定量的鋁粉和鐵粉的混合物與一定量很稀的HNO3充分反應,反應過程中無任何氣體放出.在反應結束后的溶液中,逐滴加入4mol?L-1NaOH溶液.所加NaOH溶液的體積(mL)與產生沉淀的物質的量(mol)關系如圖所示:
硝酸發生氧化還原反應的時候,一般硝酸濃度越稀,對應還原產物中氮的化合物越低.現有一定量的鋁粉和鐵粉的混合物與一定量很稀的HNO3充分反應,反應過程中無任何氣體放出.在反應結束后的溶液中,逐滴加入4mol?L-1NaOH溶液.所加NaOH溶液的體積(mL)與產生沉淀的物質的量(mol)關系如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:
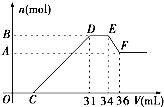 硝酸發生氧化還原反應的時候,一般硝酸越稀,對應的還原產物中氮的化合價越低.現有一定量的鋁、鐵合金與一定量稀HNO3充分反應,反應過程中無任何氣體放出.在反應結束后的溶液中,逐滴加入4mol/L NaOH溶液,所加NaOH溶液的體積(V)與產生沉淀的物質的量(n)關系如圖所示.下列說法中不正確的是( )
硝酸發生氧化還原反應的時候,一般硝酸越稀,對應的還原產物中氮的化合價越低.現有一定量的鋁、鐵合金與一定量稀HNO3充分反應,反應過程中無任何氣體放出.在反應結束后的溶液中,逐滴加入4mol/L NaOH溶液,所加NaOH溶液的體積(V)與產生沉淀的物質的量(n)關系如圖所示.下列說法中不正確的是( )| A、合金與硝酸反應時硝酸過量 | B、合金中鋁的物質的量為0.008mol | C、合金中金屬的物質的量共為0.032mol | D、無法求出C點的值 |
查看答案和解析>>
科目:高中化學 來源: 題型:
(10分) 硝酸發生氧化還原反應的時候,一般硝酸濃度越稀,對應的還原產物中氮的化合價越低。現有一定量的鐵粉和鋁粉混合物與一定量很稀的硝酸充分反應,反應過程中無任何氣體放出。在反應結束后的溶液中,逐滴加入1 mol/L的NaOH溶液,所加NaOH溶液的體積(mL)與產生沉淀的物質的量(mol)關系如下圖所示。(提示:氫氧化鋁不溶于弱酸弱堿,只溶于強酸強堿)
(1) 鐵與極稀的硝酸發生反應時得還原產物可能是____________;該反應的化學方程式為______________________________________________________________。
(2) B的數值是:______________mol。
(3) C的數值是:______________mL。
查看答案和解析>>
科目:高中化學 來源:2013屆江西省豐城中學高三階段測試化學試卷(帶解析) 題型:計算題
(10分)硝酸發生氧化還原反應的時候,一般硝酸濃度越稀,對應還原產物中氮的化合價越低。若硝酸現有一定量的鋁粉和鐵粉的混合物與一定量很稀的HNO3充分反應,反應過程中無任何氣體放出。在反應結束后的溶液中,逐滴加入4mol /LNaOH溶液,所加NaOH溶液的體積(mL)與產生沉淀的物質的量(mol)關系如圖所示。求:
(1)B與A的差值: mol;
(2)B的數值: mol;
(3)C的數值: mL。(要求有計算過程)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com