
【題目】某科研人員設計出將硫酸渣(主要成分Fe2O3,含有少量的SiO2等雜質)再利用的流程(如下圖),流程中的濾液經過多次循環后用來后續制備氧化鐵粉末。

(1)為了加快反應①的反應速率,除了攪拌、適當升高溫度、將硫酸渣粉碎外還可采用的措施是____________________________(寫出一點即可)。
(2)反應②主要作用是“還原”,即將Fe3+轉化為Fe2+。在溫度T1、T2(T1>T2)下進行該反應,通過檢測相同時間內溶液的pH,繪制pH隨時間的變化曲線如下圖所示.得出結論:該反應的溫度不宜過高。

①已知信息:pH= -lgc(H+),如0.1mol/L的鹽酸的pH= -lg0.1=1。在上述流程中通入SO2氣體“還原”時,試用離子方程式和適當文字來解釋pH下降的原因是__________________________;
②相同時間內,T1溫度下,溶液的pH更高的原因是____________________________________。
(3)該流程中循環使用的物質是 _____________。
(4)現有一包固體FeO和Fe2O3,欲要化學方法確定其中含有氧化亞鐵,應選擇的試劑是________。(填選號字母)
A. 鹽酸、硫氰化鉀溶液 B. 稀硫酸、酸性高錳酸鉀溶液
C. 稀硫酸、硫氰化鉀溶液 D. 稀硝酸、硫氰化鉀溶液
(5)為測定反應①后溶液中Fe3+的濃度以控制加入SO2的量。實驗步驟為:準確量取20.00ml的反應后溶液,稀釋成100mL溶液,取10.00 mL溶液,加入足量的KI晶體和2~3滴淀粉溶液,用0.50mol/L的Na2S2O3溶液與碘反應,當反應恰好完全進行時,共消耗Na2S2O3溶液20.00 mL。已知:2Na2S2O3 + I2 = Na2S4O6 + 2NaI,試計算原溶液中Fe3+的物質的量濃度(寫出計算過程)。______________
【答案】 適當增大硫酸濃度 SO2+2Fe3++2H2O=SO42- +2Fe2++4H+ ,生成了H+,H+濃度大,酸性強,pH下降 由已知知,T1>T2,溫度高,氣體溶解度下降,參與反應的SO2少,溶液中的H+濃度小,pH高 H2SO4 B 5.00mol/L
【解析】(1)為了加快反應①的反應速率,除了攪拌、適當升高溫度、將硫酸渣粉碎外還可采用的措施是適當增大硫酸濃度,正確答案:適當增大硫酸濃度。
(2)①氧化鐵與硫酸反應生成硫酸鐵,Fe3+具有氧化性,把二氧化硫氧化硫酸根離子,并生產生硫酸,酸性增強,pH下降,正確答案:SO2+2Fe3++2H2O=SO42- +2Fe2++4H+ ,生成了H+,H+濃度大,酸性強,pH下降。
②由已知可知,T1>T2,溫度高,氣體溶解度下降,參與反應的SO2少,溶液中的H+濃度小,pH高;正確答案: 由已知可知,T1>T2,溫度高,氣體溶解度下降,參與反應的SO2少,溶液中的H+濃度小,pH高。
(3)溶解硫酸渣時,加入硫酸;反應生成的鐵離子把二氧化硫又氧化為硫酸,所以該流程中循環使用的物質是H2SO4 ;正確答案: H2SO4。
(4)固體FeO和Fe2O3的混合物,先加入稀硫酸溶液,反應生成硫酸亞鐵和硫酸鐵,再加入酸性高錳酸鉀溶液,溶液褪色,證明溶液中有亞鐵離子,原固體中含有FeO;不能用硝酸來溶解固體,因為FeO能夠被硝酸氧化為鐵離子,影響亞鐵離子的檢驗;正確選項B。
(5)根據反應2Na2S2O3 + I2 = Na2S4O6 + 2NaI可以計算出碘的量:2Na2S2O3 --I2,碘單質的量=0.5×20×10-3/2=5×10-3 mol,有根據反應:2Fe3++2I-= I2+ 2Fe2+可知,2Fe3+--I2,Fe3+的量為10-2mol,又知10.00 mL溶液含Fe3+的量為10-2mol,則100mL溶液中含有Fe3+的量為10-1mol;則20.00ml溶液中Fe3+的物質的量濃度為10-1/0.02=5mol/L;正確答案:5.00mol/L。


科目:高中化學 來源: 題型:
【題目】經檢測某工廠的酸性廢水中所含離子及其濃度如下表所示:
離子 | Fe3+ | Cu2+ | SO42- | Na+ | H+ |
濃度/(mol/L) | 2×10-3 | 1×10-3 | 1×10-2 | 2×10-3 |
(1)c(H+)= mol/L。
(2)為了減少污染并變廢為寶,工程師們設計了如下流程,回收銅和綠礬(FeSO4·7H2O)。

① 工業廢水中加入鐵粉后,反應的離子方程式為:
Fe + Cu2+ == Fe2+ + Cu、 、 。
② 試劑B是 。
③ 操作③是蒸發濃縮、冷卻結晶、 ,最后用少量冷水洗滌晶體,在低溫下干燥。
④ 通過檢驗溶液D中Fe3+來判斷廢水中Fe3+是否除盡,實驗方法是 。
⑤ 獲得的FeSO4·7H2O需密閉保存,原因是 。
⑥ 上述1000 L廢水經處理,可獲得 FeSO4·7H2O的物質的量是 mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知五種元素的原子序數的大小順序為C>A>B>D>E;其中,A、C同周期,B、C同主族;A與B 形成離子化合物A2B,A2B中所有離子的電子數相同,其電子總數為30;D和E可形成4核10電子分子。試回答下列問題:
(1)畫出元素C的原子結構示意圖:________。
(2)寫出元素D在元素周期表中的位置:第____周期,第____族;該元素形成的單質的結構式為______。
(3)寫出下列物質的電子式:A、B、E形成的化合物______;D、E形成的化合物______。
(4)D、E形成的化合物受熱蒸發,吸收的熱量用于克服________。
(5)A、B兩元素組成的化合物A2B2屬于______(填“離子”或“共價”)化合物,其存在的化學鍵有______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃時,在“H2A—HA-—A2-”的水溶液體系中,H2A、HA-和A2- 三者中各自所占的物質的量分數(α)隨溶液pH變化的關系如圖所示。下列說法正確的是
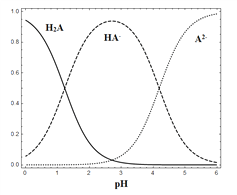
A. 在含H2A、HA-和A2- 的溶液中,加入少量NaOH固體,α(HA-)一定增大
B. 將等物質的量的NaHA和Na2A混合物溶于水,所得的溶液中α(HA-)=α(A2-)
C. NaHA溶液中,HA-的水解能力小于HA-的電離能力
D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+),則α(H2A)和α(HA-)一定相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了探究鐵、銅及其化合物的性質,某同學設計并進行了下列實驗。
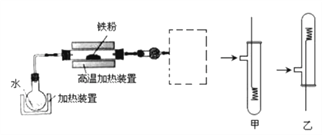
已知: 3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)
Fe3O4(s)+4H2(g)
請回答:
(1) 虛線框處宜選擇的裝置是_____ (填“甲”或“乙”); 實驗時應將螺旋狀銅絲加熱,變黑后再趁熱迅速伸入所制得的純凈氫氣中,觀察到的實驗現象是_________。
(2)實驗后,取硬質玻璃管中適量的固體,用一定濃度的鹽酸溶解,滴加KSCN溶液,沒有出現血紅色,說明該固體中沒有+3價的鐵,判斷結論是否正確并說明理由_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用電解法可提純含有某些含氧酸根雜質的粗氫氧化鉀溶液,其工作原理如圖所示。下列說法錯誤的是

A. 電解過程中,陰極區溶液的pH增大
B. 電解過程中,K+通過陽離子交換膜從陰極區移向陽極區
C. 電解過程中,陽極可發生反應:4OH--4e-==2H2O+O2↑
D. 純氫氧化鉀溶液從b出口導出
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】請根據要求填空:
(1)水的電離與溶液的酸堿性密切相關。
①常溫下,某檸檬水溶液的pH=3,其中的c(OH-)=__________。
②常溫下,濃度均為0.1 molL-1的CH3COOH溶液和CH3COONa溶液中,水的電離程度大小關系是:前者_____________后者(填“>”“<”或“=”);
③常溫下,濃度均為0.1 molL-1的NaX和NaY兩種鹽溶液,其pH分別為8 和10,則HX 和HY的酸性強弱關系是:HX_________HY(填“>”或“<”)。
(2)研究化學能與電能相互轉化的裝置、過程和效率的科學,叫做電化學。
①某原電池裝置如右圖,則:

該原電池的負極是__________(填“Zn”或“Cu”),正極的電極反應式為_______________________;
②用鉑電極電解某金屬氯化物(XCl2)的溶液,當收集到2.24 LCl2(標準狀況)時,陰極增重6.4 g,則該金屬的相對原子質量為_______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一密閉容器中,充入一定量的反應物A,反應![]() 達平衡后,保持溫度不變,將容器體積縮到一半,當達到新的平衡時,B的濃度是原來的1.6倍,則下列判斷正確的是( )
達平衡后,保持溫度不變,將容器體積縮到一半,當達到新的平衡時,B的濃度是原來的1.6倍,則下列判斷正確的是( )
A. ![]() B. 物質A的轉化率降低
B. 物質A的轉化率降低
C. 物質B的質量增加 D. 平衡向正反應方向移動了
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖的圖解表示構成細胞的元素、化合物,a、b、c、d代表不同的小分子物質,A、B、C代表不同的大分子物質,請分析回答下列問題:
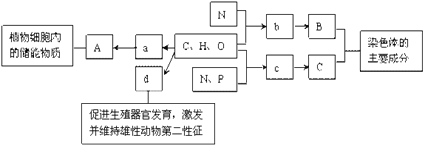
(1)在動物細胞內,與物質A作用最相近的物質是_______。
(2)A、B、C中能在細胞核內合成的是[ ]____,a、b、c、d中種類最多的是[ ]____,其結構簡式是____。
(3)物質c在人體細胞中共有____種,分子中的____不同決定了c的種類不同。
(4)細胞內的B和C都可與某些試劑發生特定的顏色反應。能與B反應產生紫色物質的試劑是____。
(5)若B、C構成了細胞膜的基本結構,則C是____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com