
【題目】三氯化磷(PCl3)是一種用于有機合成的重要催化劑。實驗室常用紅磷與干燥的Cl2制取PCl3,裝置如圖所示。
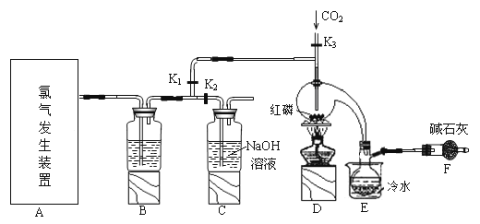
已知:紅磷與少量Cl2反應生成PCl3,與過量Cl2反應生成PCl5。PCl3遇O2會生成POCl3(三氯氧磷), POCl3溶于PCl3,PCl3遇水會強烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸點見下表。
物質 | 相對分子質量 | 熔點/℃ | 沸點/℃ |
PCl3 | 137.5 | -112 | 75.5 |
POCl3 | 153.5 | 2 | 105.3 |
請回答下列問題:
(1)請從下圖中選擇制備氯氣的發生裝置
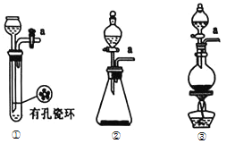
你選用的裝置是____(填序號),反應的離子方程式為____。
(2)B中所盛試劑是_____。
(3)E中冷水的作用是____。
(4)儀器F的名稱是____;F中堿石灰的作用是___。
(5)實驗制得的粗產品中常含有POCl3、PCl5等,加入紅磷加熱除去PCl5后,再通過__(填操作名稱)即可得到較純凈的PCl3。
(6)通過下面方法可測定產品中PCl3的質量分數:
①迅速稱取1.00g產品,加水反應后配成250mL溶液:
②取以上溶液25.00mL,向其中加入10.00mL0.1000mol/L碘水(足量),充分反應;
③向②所得溶液中加入幾滴淀粉溶液,用0.1000 mol/L的Na2S2O3溶液滴定;
④重復②、③操作,平均消耗0.1000 mol/LNa2S2O3溶液8.00mL。
己知:H3PO3+I2+H2O=H3PO4+2HI,I2+2Na2S2O3=2NaI+Na2S4O6,根據上述數據,假設測定過程中沒有其他反應,該產品中PCl3的質量分數為___(保留3位有效數字)。
【答案】②或③ 2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O或MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 濃硫酸 冷卻PCl3,防止揮發 球形干燥管 吸收多余的Cl2,防止空氣中的水蒸氣進入燒瓶與PCl3反應 蒸餾 82.5%
Mn2++Cl2↑+2H2O 濃硫酸 冷卻PCl3,防止揮發 球形干燥管 吸收多余的Cl2,防止空氣中的水蒸氣進入燒瓶與PCl3反應 蒸餾 82.5%
【解析】
實驗室要用紅磷與干燥的氯氣模擬工業生產制取PCl3流程為:利用②或③裝置制得氯氣,因PCl3遇水會強烈水解,所以氯氣需干燥,B裝置利用濃硫酸干燥氯氣,利用二氧化碳排盡裝置中的空氣,PCl3沸點為75.5℃,利用E裝置防止PCl3揮發(冷凝),因尾氣中含有有毒氣體氯氣,且空氣中水蒸氣可能進入裝置,所以用F裝置利用堿石灰吸收多余的氯氣,防止空氣中的水蒸氣進入燒瓶和PCl3反應。
(1)實驗室制備氯氣時,用二氧化錳與濃鹽酸共熱或高錳酸鉀與濃鹽酸反應,選擇制備氯氣的發生裝置為②、③;反應的離子方程式為2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O或MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)PCl3遇水會強烈水解,需要干燥的氯氣,則B裝置中試劑為濃硫酸;
(3)PCl3沸點為75.5℃,利用E裝置防止PCl3揮發(冷凝);
(4)根據裝置特點,F裝置為球形干燥管,尾氣中含有有毒氣體氯氣,且空氣中水蒸氣可能進入裝置,堿石灰可吸收多余的氯氣,防止空氣中的水蒸氣進入燒瓶和PCl3反應;
(5)POCl3的沸點為105.3℃,PCl3的沸點為75.5℃,且互相溶解,可利用蒸餾方式分離;
(6)根據題給信息可知:滴定實驗涉及關系式為PCl3—H3PO3—I2和2Na2S2O3--I2,設混合物中PCl3的物質的量為nmol,水解生成的H3PO3反應掉的I2的物質的量為nmol;滴定多余I2的消耗的Na2S2O3的物質的量為0.1×8.40×10-3=8.4×10-4mol,多余的I2的物質的量為0.0008/2=0.0004mol,提供I2的總物質的量0.1×10×10-3mol,H3PO3反應掉的I2的物質的量: 1×10-3-0.0004=0.0006 mol,25.00mL溶液里含有PCl3的質量為0.0006×137.5=0.0825g,則250mL溶液中,含有PCl3的質量為0.825 g,產品中PCl3的質量分數為0.825/1×100%=82.5%。


科目:高中化學 來源: 題型:
【題目】下列依據熱化學方程式得出的結論正確的是
A. 已知![]()
![]() ,則
,則![]() 固體與稀鹽酸完全反應,放出的熱量即為
固體與稀鹽酸完全反應,放出的熱量即為![]()
B. 已知![]()
![]()
![]()
![]() 則
則![]()
C. 已知![]() ,則反應物總能量小于生成物總能量
,則反應物總能量小于生成物總能量
D. 已知![]() (白磷,s)=
(白磷,s)=![]() (紅磷,s)
(紅磷,s)![]() ,則白磷比紅磷穩定
,則白磷比紅磷穩定
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(題文)[化學——選修5:有機化學基礎]
近來有報道,碘代化合物E與化合物H在Cr-Ni催化下可以發生偶聯反應,合成一種多官能團的化合物Y,其合成路線如下:

已知:![]()
回答下列問題:
(1)A的化學名稱是________________。
(2)B為單氯代烴,由B生成C的化學方程式為________________。
(3)由A生成B、G生成H的反應類型分別是________________、________________。
(4)D的結構簡式為________________。
(5)Y中含氧官能團的名稱為________________。
(6)E與F在Cr-Ni催化下也可以發生偶聯反應,產物的結構簡式為________________。
(7)X與D互為同分異構體,且具有完全相同官能團。X的核磁共振氫譜顯示三種不同化學環境的氫,其峰面積之比為3∶3∶2。寫出3種符合上述條件的X的結構簡式________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業尾氣中的氮氧化物常用氨催化吸收法,原理是NH3與NOx反應生成無毒物質。某同學采用以下裝置和步驟模擬工業上氮氧化物的處理過程。
(一)提供的裝置
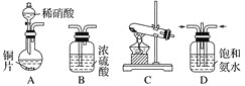

(二)NH3的制取
(1)下列有關實驗室制備氣體的說法正確的是__________(填序號)。
①可以用排飽和食鹽水的方法收集氯氣 ②用赤熱的炭與水蒸氣反應制取氫氣 ③實驗室制氧氣有時需要加熱,有時不需要加熱 ④用無水氯化鈣干燥氨氣 ⑤用濃鹽酸洗滌高錳酸鉀分解制氧氣的試管
(2)從所提供的裝置中選取一個能制取氨氣的裝置:________________(填序號)。
(3)當采用你所選用的裝置制取氨氣時,相應反應的化學方程式是___________。
(三)模擬尾氣的處理
選用上述部分裝置,按下列順序連接成模擬尾氣處理裝置,回答有關問題:
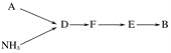
(4)A中反應的離子方程式為___________。
(5)D裝置中的液體可換成________(填序號)。
a CuSO4 b H2O c CCl4 d 濃硫酸
(6)該同學所設計的模擬尾氣處理實驗還存在的明顯缺陷是________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從海水中提取一些重要的化工產品的工藝流程如圖所示。
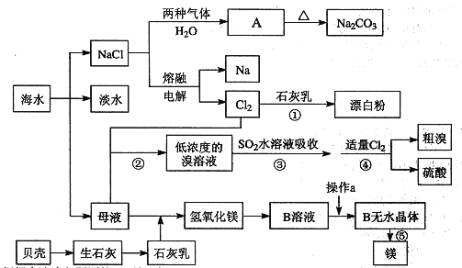
根據上述流程圖回答下列問題:
(1)圖中A的化學式為 ___________,在制取A的過程中需向飽和NaCl溶液中先后通入兩種氣體,后通入氣體的化學式為________________。
(2)海水淡化處理的方法有_____________________。(寫出2種即可)
(3)過程⑤的化學方程式為 _________________________________。
(4)過程③用SO2水溶液吸收溴單質,吸收率可達93%,生成兩種強酸,寫出反應的離子方程式________________________________。
(5)過程②到過程④的變化為“Br→Br2→Br→Br2”,其目的是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數值。下列有關敘述正確的是( )
A.1molN2與3molH2反應生成的NH3分子數為2NA
B.14g乙烯(C2H4)和丙烯(C3H6)混合氣體中的原子總數為3NA
C.1molFe溶于過量硝酸,電子轉移數為2NA
D.標準狀況下,2.24LCCl4含有的共價鍵數為0.4NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在常溫下,用0.1000 mol/L的鹽酸滴定25 mL 0.1000 mol/L Na2CO3溶液,所得滴定曲線如下圖所示。下列有關滴定過程中溶液相關微粒濃度間的關系不正確的是
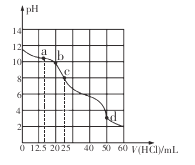
A. a點:c( HCO3-)>c(Cl-)>c(C032-)
B. b點:c(Na+)+c(H+)=c(Cl一)+c(HCO3-)+c(CO32-)+c(OH-)
C. c點:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
D. d點:c(Cl-)=c(Na+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四溴化碳是一種灰白色粉末,熔點為94~95℃,廣泛用于有機化合物的溴代、農藥的制備等。某合作學習小組的同學擬用丙酮和液溴制備四溴化碳,其原理為CH3COCH3+4Br2+5NaOH→CBr4+CH3COONa+4NaBr+4H2O。回答下列問題:
Ⅰ.制取Br2
(1)甲組同學擬用溴化鈉、二氧化錳及濃硫酸制備液溴,其實驗裝置如圖1所示:
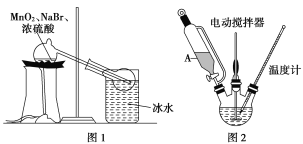
①該裝置不用橡皮塞及橡皮管,其原因是___________________;
②冰水的作用是__________________________。
Ⅱ.制取CBr4
(2)乙組同學擬利用甲組同學制得的液溴與CH3COCH3(沸點56.5℃)等試劑制取四溴化碳。實驗步驟如下:
步驟1:向圖2中三頸燒瓶中加入11.4 g NaOH和46 mL水,攪拌。
步驟2:冰水浴冷卻至2℃時,開始不斷滴加液溴20 g,滴加完畢后在5℃下保持20 min。
步驟3:加入少量相轉移試劑,在不斷攪拌下滴入1.6 g丙酮,維持溫度在5~10℃,連續攪拌4 h。
步驟4:過濾、冷水洗滌、減壓烘干,得產品8.3 g。
①步驟2滴入Br2之前,冷卻至2℃的目的是__________________________
②步驟4洗滌時,如何證明已洗滌干凈: ___________________________。
③本次實驗中產品的產率為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應原理是研究和學習化學的重要依據。回答下列問題:
(1)已知氫氣的燃燒熱△H=﹣285.5kJmol﹣1,則電解水的熱化學方程式為_____
(2)在298K、101kPa下,2SO2(g)+O2(g)2SO3(g)△H=﹣198kJmol﹣1,則相同條件下,2mol SO2和 1 mol O2充分反應,最終放出的熱量_____198kJ(填“大于”“小于或“等于”);該反應的平衡常數表達式K=_____。
(3)25℃時,下表為一些難溶電解質的相關數據:
物質 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
開始沉淀時的pH | 5.8 | 4.1 | 2.0 |
完全沉淀時的pH | 8.3 | 6.4 | 3.2 |
常溫下,除去酸性CuCl2溶液中含有的少量FeCl2,其操作步驟為:
①應先加入_____(填試劑名稱),發生的離子反應方程式為_____
②再加入CuO,調節溶液的pH在_____范圍內,使溶液中的Fe3+轉化為Fe(OH)3沉淀,過濾。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com