
| A. | 純堿屬于堿 | B. | 鋼屬于純凈物 | ||
| C. | 冰醋酸屬于混合物 | D. | 水屬于氧化物 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
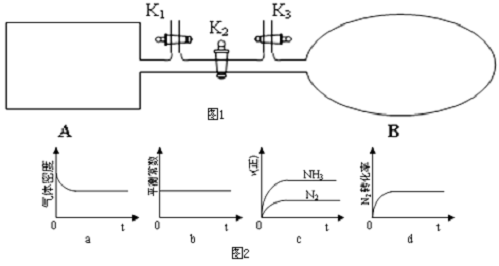
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二者均可作為水果催熟劑 | |
| B. | 二者均可使酸性高錳酸鉀溶液褪色 | |
| C. | 常溫常壓下二者均為難溶于水的氣體 | |
| D. | 在一定條件下二者均能與氫氣發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
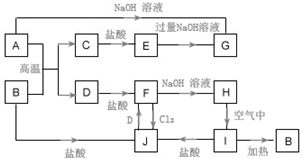 A~J為中學化學的常見物質,它們之間有如圖所示的轉化關系(部分產物已略去).已知A、D為金屬單質,B為紅棕色粉末,I為紅褐色固體.
A~J為中學化學的常見物質,它們之間有如圖所示的轉化關系(部分產物已略去).已知A、D為金屬單質,B為紅棕色粉末,I為紅褐色固體.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 雷瑣苯乙酮所有碳原子不可能共平面 | |
| B. | 雷瑣苯乙酮、傘形酮能用酸性KmnO4鑒別 | |
| C. | 1mol雷瑣苯乙酮跟足量H2反應,最多消耗3molH2 | |
| D. | 1mol傘形酮與足量NaOH溶液反應,最多消耗3molNaOH |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com