
已知
(l)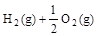 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·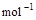
(2)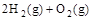 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·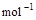
(3)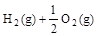 =H2O(l) △H3=c kJ·
=H2O(l) △H3=c kJ·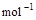
(4)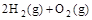 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·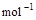
下列關系式中正確的是( )
A.a<c <0 B.b>d>0 C.2a=b<0 D.2c=d>0
科目:高中化學 來源:2013-2014學年湖北省荊門市高三元月調考理綜化學試卷(解析版) 題型:填空題
Ⅰ.沿海地區有著豐富的海水資源,海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等離子。合理利用資源和保護環境是可持續發展的重要保證。
 (1)海水經過處理后可以得到無水氯化鎂,無水氯化鎂是工業制取鎂的原料。試寫出電解熔融氯化鎂制取金屬鎂的化學反應方程式???????????????????????????????? 。
(1)海水經過處理后可以得到無水氯化鎂,無水氯化鎂是工業制取鎂的原料。試寫出電解熔融氯化鎂制取金屬鎂的化學反應方程式???????????????????????????????? 。
(2)某化工廠生產過程中會產生含有Cu2+和Pb2+的污水。排放前擬用沉淀法除去這兩種離子,根據下列數據,你認為投入?????????? (選填“Na2S”或“NaOH”)效果更好。
難溶電解質 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |
(3)火力發電在我國的能源利用中占較大比重,但是排放出的SO2會造成一系列環境和生態問題。利用海水脫硫是一種有效的方法,其工藝流程如下圖所示:

①天然海水的pH≈8,試用離子方程式解釋天然海水呈弱堿性的原因????????? (任寫一個)。
②某研究小組為探究提高含硫煙氣中SO2吸收效率的措施,進行了天然海水吸收含硫煙氣的模擬實驗,實驗結果如圖所示。

請你根據圖示實驗結果,就如何提高一定濃度含硫煙氣中SO2的吸收效率,提出一條合理化建議:??? 。
③天然海水吸收了含硫煙氣后會溶有H2SO3、HSO3-等分子或離子,使用氧氣將其氧化的化學原理是?????????????????? (任寫一個化學方程式或離子方程式)。氧化后的“海水”需要引入大量的天然海水與之混合后才能排放,該操作的主要目的是???????????????????????? 。
Ⅱ.能源是人類生存和發展的重要支柱。研究化學反應過程中的能量變化在能源緊缺的今天具有重要的理論意義。已知下列熱化學方程式
①2H2(g)+O2(g)=2H2O(l)????  H=-570kJ/mol;
H=-570kJ/mol;
②H2(g)+1/2O2(g)=H2O(g)???  H=-242kJ/mol;
H=-242kJ/mol;
③C(s)+1/2O2(g)=CO(g)????  H=—110.5kJ/moL;
H=—110.5kJ/moL;
④C(s)+O2(g)=CO2(g)???????  H=—393.5kJ/moL;
H=—393.5kJ/moL;
⑤CO2(g)+2H2O(g)=2CH4(g)+2 O2(g)?  H=+890kJ/moL
H=+890kJ/moL
回答下列問題
(1)上述反應中屬于吸熱反應的是??????????????? 。
(2)H2的燃燒熱為△H=??????????????? 。
(3)蓋斯定律在生產和科學研究中有很重要的意義。有些反應的反應熱雖然難直接測定,但可通過間接的方法求得。已知C(s) + H2O(g)=H2(g)+ CO(g)????  H=akJ/moL;則a=???????? ;該反應的熵
H=akJ/moL;則a=???????? ;該反應的熵 S???????? 0(選填“>”、“=”、“<”);已知自由能
S???????? 0(選填“>”、“=”、“<”);已知自由能 G=
G= H—T
H—T S,當
S,當 G<0時可自發進行。則該反應在什么條件下可自發進行__________________。
G<0時可自發進行。則該反應在什么條件下可自發進行__________________。
(4)CO分析儀以燃料電池為工作原理,其裝置如圖所示,該電池中電解質為氧化釔-氧化鈉,其中O2-可以在固體介質NASICON中自由移動。下列說法錯誤的是????? 。

A.負極的電極反應式為:CO+O2—―2e-=CO2
B.工作時電極b作正極,O2—由電極a流向電極b
C.工作時電子由電極a通過傳感器流向電極b
D.傳感器中通過的電流越大,尾氣中CO的含量越高
查看答案和解析>>
科目:高中化學 來源:2013屆山東臨清三中高二上學期學分認定測試化學試卷 題型:填空題
(6分)(1)某溫度下,純水中c(H+) = 5×10-7 mol·L-1,則此時純水中的c(OH-) = ____ mol·L-1;若溫度不變,滴入稀硫酸使c(H+) = 5.0×10-3 mol·L-1,則c(OH-) = ____ mol·L-1。
(2)已知室溫下pH=2的高碘酸(H5IO6)溶液與pH=12的NaOH溶液等體積混合,所得混合溶液呈酸性,則高碘酸的電離方程式是__________________________。
查看答案和解析>>
科目:高中化學 來源:同步題 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:
(6分)火箭推進器中盛有強還原劑液態肼(N2H4)和強氧化劑液態雙氧水。當它們混合反應時,即產生大量氮氣和水蒸氣,并放出大量熱。已知:0.4mol液態肼與足量的液態雙氧水反應,生成氮氣和水蒸氣,放出256.652kJ的熱量。
⑴ 反應的熱化學方程式為 ;
⑵ 又已知H2O(l) = H2O(g); △H=+44kJ/mol,則16g液態肼和液態雙氧水反應生成液態水時放出的熱量是 ;
⑶ 此反應用于火箭推進,除釋放大量的熱和快速產生大量氣體外還有一個很大的優點是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
氮元素有多種氫化物,如氨(NH3)、肼(N2H4)等。
(1)肼(N2H4)又稱聯氨,是一種可燃性的液體,可用作火箭燃料。已知在25℃,101kPa時,N2H4的燃燒熱為624KJ/mol,又已知H2O(l)=H2O(g) △H=+44KJ/mol。則N2H4完全燃燒生成氮氣和水蒸汽的熱化學方程式是________________。
(2)肼—空氣燃料電池是一種堿性燃料電池,電解質溶液是20%~30%的KOH溶液。 該電池放電時,負極的電極反應式是 。如果此燃料電池的能量轉化率為50%,當消耗標準狀況下的空氣2.24L(假設空氣中氧氣體積含量為20%)時,此電池產生的電能為 (假設肼此時生成液態水)。
(3)1998年希臘亞里斯多德大學的Marnellos和Stoukides采用高質子導電性的SCY陶瓷(能傳遞H+),實現了高溫常壓下高轉化率的電化學合成氨,其實驗裝置如圖,正極的電極反應式為______________。電池工作時,H+移向 極(填“正”、“負”)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com