
【題目】在一定溫度下,發生如下反應:2SO2(g)+O2(g) ![]() 2SO3(g)ΔH<0。改變起始時n(SO2)對反應的影響如圖所示。下列說法正確的是
2SO3(g)ΔH<0。改變起始時n(SO2)對反應的影響如圖所示。下列說法正確的是
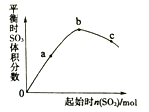
A. SO2的起始量越大,混合氣體中SO2的體積分數越大
B. a、b、c三點中,a點時SO2的轉化率最高
C. a、b、c三點的平衡常數:Kb>Kc>Ka
D. b、c點均為化學平衡點,a點未達平衡且反應正向進行
科目:高中化學 來源: 題型:
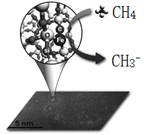
【題目】中科院一項最新成果實現了甲烷高效生產乙烯,甲烷在催化作用下脫氫,在氣相中經自由基偶聯反應生成乙烯,如圖所示。
物質 | 燃燒熱(kJ/mol) |
氫氣 | 285.8 |
甲烷 | 890.3 |
乙烯 | 1411.5 |
(1)已知相關物質的燃燒熱如上表,寫出甲烷制備乙烯的熱化學方程式_________。
(2)在400℃時,向1L的恒容反應器中充入1molCH4,發生上述反應,測得平衡混合氣體中C2H4的體積分數為20.0 %。則在該溫度下,其平衡常數K=_______。按化學平衡移動原理,在圖(a)中畫出該反應的平衡轉化率與溫度及壓強(p1>p2)的關系曲線。_______________________
(3)在制備C2H4時,通常存在副反應:2CH4(g)![]() C2H6(g)+H2(g)。在常溫下,向體積為1L的恒容反應器中充入1molCH4,然后不斷升高溫度,得到圖(b)。
C2H6(g)+H2(g)。在常溫下,向體積為1L的恒容反應器中充入1molCH4,然后不斷升高溫度,得到圖(b)。
①在200℃時,測出乙烷的量比乙烯多的主要原因是_________________________。
②在600℃后,乙烯的體積分數減少的主要原因是__________________________。

(4)工業上常采用除雜效率高的吸收-電解聯合法,除去天然氣中的雜質氣體H2S,并轉化為可回收利用的單質硫,其裝置如下圖所示。

通電前,先通入一段時間含H2S的甲烷氣,使部分NaOH吸收H2S轉化為Na2S,再接通電源,繼續通入含雜質的甲烷氣,并控制好通氣速率。裝置中右端碳棒為_________極,左端碳棒上的電極反應為_________________________,右池中的c(NaOH):c(Na2S)______________(填“增大”、“基本不變”或“減小)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知相同溫度下CH3COOH和NH3H2O的電離常數相等,現向10mL濃度為0.1molL﹣1的CH3COOH溶液中滴加相同濃度的氨水,在滴加過程中( )
A.水的電離程度始終增大
B.c(NH4+):c(NH3H2O)始終減小
C.c(CH3COOH)與c(CH3COO)之和始終保持不變
D.當加入氨水的體積為10mL時,c(NH4+)=c(CH3COO﹣)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.氫能是重要的新能源。他的開發、儲存和應用,是當前人們關注的熱點之一。
(1)開發氫能的方法之一是分解水。開發特殊物質做催化劑,_______(填“能”或“不能”)降低水分解過程中所需能量。
(2)用高壓氫氣、氧氣制作的氫氧燃料電池是氫能源利用的一種重要方式。某氫氧燃料電池的兩個電極的極性標志模糊不清,小明利用如圖所示裝置進行實驗判斷。

①根據觀察到的現象判斷電極a(或b)極性:若石墨1表面覆蓋一層紅色固體,則a電極是_____極。,
②寫出U型管中陽極的電極反應式:______________,發生________反應(填“氧化”、“還原”)。電解一段時間后發現陰極增重6.4g,則外電路中通過的電子的物質的量是________mol。若該電解反應所需的電子全部由氫氧燃料電池提供,則至少需要消耗__________ L氫氣(標準狀況下)才能滿足需要。
Ⅱ.汽車行駛、某些化工廠生產過程,會向空氣中排放出NOx、CO、SO2等有害氣體。
(1)NOx對環境的主要影響有___________(填字母標號)。
A.硝酸型酸雨 B.溫室效應 C. 破壞臭氧層 D. 光化學煙霧
(2)為了減少重型柴油車排放NOx,向尾氣處理裝置內自動噴入的尿素溶液在一定條件下先轉化為NH3,NH3再與NOx反應生成兩種無污染的物質。其中NH3與NO2在一定條件下反應的化學方程式為_________。
(3)通過CO傳感器可監測CO的含量,其工作原理為2CO+O2=2CO2,示意圖如下:

①通入CO的一極為_______極(填“正”或“負”、“陰”、“陽”),溶液中H+移向_____極(填“A”或“B”)。
②寫出B電極的電極反應式:_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗方法錯誤的是( )
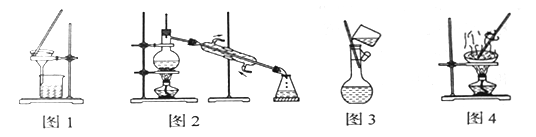
A. 圖1所示為除去少量泥水中泥沙的方法
B. 圖2所示為制取蒸餾水的方法
C. 圖3所示為稀釋濃硫酸的方法
D. 圖4所示為蒸發氯化鈉溶液制氯化鈉晶體的方法
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生物大分子在生物體的生命活動中具有重要的作用。碳原子本身的化學性質,使它能夠通過化學鍵連接成鏈或環,從而形成各種生物大分子。可以說,地球上的生命是在碳元素的基礎上建立起來的。以上事實可以說明
A. C元素組成所有的的化合物
B. C元素是組成生物體的最基本的元素
C. C元素是各種大分子中含量最多的元素
D. C元素比其他元素重要
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】C、H、N三種元素在人體的化學成分中,質量分數共占73%左右(占細胞干重的百分比),而在巖石圈的化學成分中,質量分數不到1%,這一事實說明( )
A. 生物界與非生物界具有相似性
B. 生物界與非生物界具有統一性
C. 生物界與非生物界具有差異性
D. 生物界與非生物界的本質完全相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
A. 化學鍵的斷裂和形成是化學反應中能量變化的主要原因
B. 已知常溫下Ksp[Mg(OH)2]=1.8×10-11,則Mg(OH)2在pH=12的NaOH溶液中的溶解度約為1.044×10-6g
C. 水能,風能、生物質能是可再生能源,煤、石油、天然氣是不可再生能源
D. 用酚醛樹脂制成的塑料可反復加熱熔融加工
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com