
決定物質(zhì)性質(zhì)的重要因素是物質(zhì)的結(jié)構(gòu)。請回答下列問題:
(1)N、O、S三種元素的第一電離能從大到小的順序為 ????????? 。
(2)甲醛(H2C=O)分子碳原子的雜化方式為 ?????????? 用價層電子對互斥理論推斷甲醛中H—C—H的鍵角?????? 120o(填“>”“<”或“=”)。
(3)科學家通過X射線探明,KCl、MgO、CaO的晶體結(jié)構(gòu)與NaCl的晶體結(jié)構(gòu)相似(圖a所示)。KCl、CaO、MgO三種離子晶體熔點從高到低的順序是?????? 。
(4)設MgO晶胞的邊長為acm,則MgO的密度是??? g·cm-3(只要求列算式。阿伏加德羅常數(shù)為NA)。
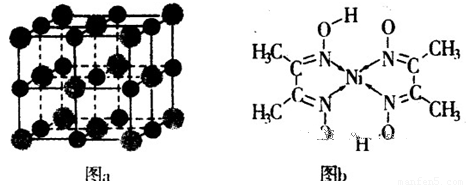
(5)某配合物的分子結(jié)構(gòu)如圖b所示,其分子內(nèi)不含有????? (填字母)。
A.離子鍵? B.共價鍵? C.金屬鍵? D.配位鍵? E.氫鍵? F.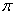 鍵
鍵
(1)N>O>S;(2)sp2;<;(3)MgO>CaO>KCl;(4)160/a3NA;(5)AC。
【解析】
試題分析:(1)根據(jù)同周期同主族元素性質(zhì)遞變規(guī)律判斷,同一周期由左向右元素原子的第一電離能呈遞增趨勢,但氮原子2p軌道為半充滿狀態(tài),第一電離能比相鄰的元素都大;同主族由上到下元素原子的第一電離能逐漸減小,N、O、S三種元素的第一電離能從大到小的順序為N>O>S;(2)甲醛(H2C=O)分子碳原子的雜化方式為sp2;甲醛(H2C=O)分子中氧原子上含有兩對孤對電子,對成鍵電子對有排斥作用,甲醛中H—C—H的鍵角<120o;(3)對于結(jié)構(gòu)相似的離子晶體,晶格能越大晶體的熔點越高;晶格能的高低取決于離子半徑和離子所帶的電荷,離子半徑越小,所帶電荷越多,晶格能越大,熔點越高;則KCl、CaO、MgO三種離子晶體熔點從高到低的順序是MgO>CaO>KCl;(4)根據(jù)MgO晶胞結(jié)構(gòu)利用切割法分析知,1mol晶胞中含有4molMgO,質(zhì)量為160g,晶胞的邊長為acm,則1mol晶胞的體積為a3NAcm3則MgO的密度是160/a3NAg·cm-3;(5)根據(jù)配合物的分子結(jié)構(gòu)判斷,其分子內(nèi)不含有離子鍵和金屬鍵,選AC。
考點:考查物質(zhì)結(jié)構(gòu)與性質(zhì),涉及第一電離能的比較、雜化方式的判斷、晶胞計算及化學鍵的識別。


科目:高中化學 來源: 題型:閱讀理解
| 電離能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 共價鍵 | C-C | C-N | C-S |
| 鍵能/kJ?mol-1 | 347 | 305 | 259 |
 (3)科學家通過X射線探明,KCl、MgO、CaO、TiN的晶體結(jié)構(gòu)與NaCl的晶體結(jié)構(gòu)相似(如圖一所示),其中3種離子晶體的晶格能數(shù)據(jù)如下表:
(3)科學家通過X射線探明,KCl、MgO、CaO、TiN的晶體結(jié)構(gòu)與NaCl的晶體結(jié)構(gòu)相似(如圖一所示),其中3種離子晶體的晶格能數(shù)據(jù)如下表:| 離子晶體 | NaCl | KCl | CaO |
| 晶格能/kJ?mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 (2013?渭南二模)決定物質(zhì)性質(zhì)的重要因素是物質(zhì)結(jié)構(gòu).請回答下列問題.
(2013?渭南二模)決定物質(zhì)性質(zhì)的重要因素是物質(zhì)結(jié)構(gòu).請回答下列問題.| 電離能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 共價鍵 | C-C | C-N | C-S |
| 鍵能/kJ?mol-1 | 347 | 305 | 259 |
| 離子晶體 | NaCl | KCl | CaO |
| 晶格能/kJ?mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 (2011?姜堰市二模)決定物質(zhì)性質(zhì)的重要因素是物質(zhì)結(jié)構(gòu).請回答下列問題.
(2011?姜堰市二模)決定物質(zhì)性質(zhì)的重要因素是物質(zhì)結(jié)構(gòu).請回答下列問題.| 電離能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 離子晶體 | NaCl | KCl | CaO |
| 晶格能/kJ?mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化學 來源: 題型:
決定物質(zhì)性質(zhì)的重要因素是物質(zhì)結(jié)構(gòu)。請回答下列問題。
(1)已知A和B為第三周期元素,其原子的第一至第四電離能如下表所示:
| 電離能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
A的化合價 B的化合價(填“>”、“<”或“=”)。
(2)實驗證明:KCl、MgO、CaO、TiN這4種晶體的結(jié)構(gòu)與NaCl晶體結(jié)構(gòu)相似(如上圖所示),其中3種離子晶體的晶格能數(shù)據(jù)如下表:
| 離子晶體 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
則該 4種離子晶體(不包括NaCl)熔點從高到低的順序是: 。其中MgO晶體中一個Mg2+周圍和它最鄰近且等距離的Mg2+有 個。
(3)金屬陽離子含未成對電子越多,則磁性越大,磁記錄性能越好。離子型氧化物V2O5和CrO2中,適合作錄音帶磁粉原料的是 。
(4)某配合物的分子結(jié)構(gòu)如上圖所示,則N原子的雜化方式為 ;基態(tài)Ni原子的電子排布式 。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江蘇省高三上學期10月份月考化學試卷 題型:填空題
(12分)決定物質(zhì)性質(zhì)的重要因素是物質(zhì)結(jié)構(gòu)。請回答下列問題。
(1)已知A和B為第三周期元素,其原子的第一至第四電離能如下表所示:
|
電離能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
|
A |
578 |
1817 |
2745 |
11578 |
|
B |
738 |
1451 |
7733 |
10540 |
則,A的化合價 ▲ B的化合價(填“>”、“<”或“=”)。
(2)實驗證明:KCl、MgO、CaO、TiN這4種晶體的結(jié)構(gòu)與NaCl晶體結(jié)構(gòu)相似(如右圖所示),

其中3種離子晶體的晶格能數(shù)據(jù)如下表:
|
離子晶體 |
NaCl |
KCl |
CaO |
|
晶格能/kJ·mol-1 |
786 |
715 |
3401 |
則該 4種離子晶體(不包括NaCl)熔點從高到低的順序是: ▲ ,原因是: ▲ 。
(3)金屬陽離子含未成對電子越多,則磁性越大,磁記錄性能越好。離子型氧化物V2O5和CrO2中,適合作錄音帶磁粉原料的是 ▲ 。
(4)某配合物的分子結(jié)構(gòu)如右圖所示,

則N原子的雜化方式為 ▲ ;基態(tài)Ni原子的電子排布式 ▲ 。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com