
| 試劑 | 離子反應方程式 | |
| ①NaHCO3溶液(Na2CO3) | CO2 | CO2+H2O+CO32-=2HCO3- |
| ②Fe2O3(Al2O3) | NaOH溶液 | Al2O3+2OH-=2AlO2-+H2O |
| ③FeCl3溶液(FeCl2) | Cl2 | 2Fe2++Cl2=2Fe3++2Cl- |
| ④CO2(HCl) | 飽和的NaHCO3溶液 | HCO3-+H+=H2O+CO2↑ |
分析 (1)A.配制一定物質的量濃度溶液,定容時俯視刻度線會導致所配溶液體積偏小;
B.氯水中含有次氯酸,次氯酸具有漂白性;
C.濃硫酸稀釋是將濃硫酸沿燒杯內壁倒入蒸餾水中,并不斷攪拌;
D.NaOH易潮解且具有強腐蝕性;
E.K元素的焰色反應必須透過藍色鈷玻璃觀察;
F.氫氧化亞鐵不穩定,易被空氣中氧氣氧化生成氫氧化鐵;
(2)①碳酸鈉和水、二氧化碳反應生成碳酸氫鈉,所以將足量二氧化碳通入混合溶液中即可除去碳酸鈉;
②氧化鋁和NaOH溶液反應生成可溶性的偏鋁酸鈉,氧化鐵和NaOH溶液不反應,所以可以用NaOH溶液除去氧化鋁;
③氯化亞鐵和氯氣發生氧化還原反應生成氯化鐵,所以用向溶液中通入足量氯氣除去氯化亞鐵;
④HCl和飽和的碳酸氫鈉反應生成二氧化碳,二氧化碳和碳酸氫鈉不反應,可以用飽和的碳酸氫鈉溶液除去HCl.
解答 解:(1)A.配制一定物質的量濃度溶液,定容時俯視刻度線會導致所配溶液體積偏小,則配制溶液濃度偏大,故錯誤;
B.氯水中含有次氯酸,次氯酸具有漂白性,所以導致測量不準確,應該用pH計測定氯水溶液的pH值,故錯誤;
C.濃硫酸稀釋是將濃硫酸沿燒杯內壁倒入蒸餾水中,并不斷攪拌,防止局部溫度過高而濺出液體,故正確;
D.NaOH易潮解且具有強腐蝕性,所以稱量NaOH固體時要放置在燒杯中稱量,故錯誤;
E.K元素的焰色反應必須透過藍色鈷玻璃觀察,濾去黃光的干擾,故錯誤;
F.氫氧化亞鐵不穩定,易被空氣中氧氣氧化生成氫氧化鐵,為防止氫氧化亞鐵被空氣氧化,則制備氫氧化亞鐵時,將盛有NaOH溶液的滴管,伸入硫酸亞鐵溶液中,故正確;
故選CF;
(2):①向Na2CO3中通入二氧化碳,會反應生成碳酸氫鈉溶液,達到除雜的目的,離子方程式:CO2+H2O+CO32-=2HCO3-;
②Al2O3與氫氧化鈉溶液反應生成偏鋁酸鈉和水,而三氧化二鐵不反應,離子方程式:Al2O3+2OH-=2AlO2-+H2O;
③氯氣能將二價鐵離子氧化為三價鐵離子,離子方程式:2Fe2++Cl2=2Fe3++2Cl-;
④飽和碳酸氫鈉溶液能和鹽酸反應生成二氧化碳氣體,實質是:HCO3-+H+=H2O+CO2↑,且碳酸氫鈉和二氧化碳不反應,
故答案為:
| 試劑 | 離子反應方程式 | |
| ① | CO2 | CO2+H2O+CO32-=2HCO3- |
| ② | NaOH溶液 | Al2O3+2OH-=2AlO2-+H2O |
| ③ | Cl2 | 2Fe2++Cl2=2Fe3++2Cl- |
| ④ | 飽和的NaHCO3溶液 | HCO3-+H+=H2O+CO2↑ |
點評 本題考查化學實驗方案評價及物質分離提純,為高頻考點,明確實驗原理、物質性質差異性是解本題關鍵,側重考查學生分析判斷及離子方程式書寫能力,注意除雜時不能引進新的雜質且操作方便.


 陽光同學一線名師全優好卷系列答案
陽光同學一線名師全優好卷系列答案科目:高中化學 來源: 題型:實驗題
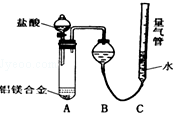 鋁鎂合金已成為輪船制造、化工生產等行業的重要材料.研究性學習小組的三位同學,為測定已知質量的鋁鎂合金(設不含其它元素)中鎂的質量分數,設計下列三種不同實驗方案(所加試劑均為足量)進行探究.填寫下列空白.
鋁鎂合金已成為輪船制造、化工生產等行業的重要材料.研究性學習小組的三位同學,為測定已知質量的鋁鎂合金(設不含其它元素)中鎂的質量分數,設計下列三種不同實驗方案(所加試劑均為足量)進行探究.填寫下列空白.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題

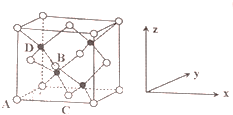
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水污染的程度是由其溶氧量來測定 | |
| B. | 污染水的金屬元素如汞、鎘、鉛等的含量極少時,不會對生物造成傷害 | |
| C. | 使用含磷洗衣粉會造成河水、湖水污染,使海藻瘋狂生長,魚類死亡 | |
| D. | 工業所排出的廢水危害水生生物 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 ,W的氣態氫化物穩定性比H2O(g)弱(填“強”或“弱”).
,W的氣態氫化物穩定性比H2O(g)弱(填“強”或“弱”).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
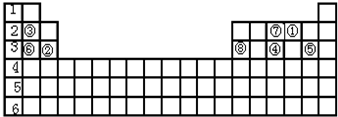
 ,與④的氫化物相比較,N的氫化物更穩定.
,與④的氫化物相比較,N的氫化物更穩定.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對農作物合理施用化肥 | B. | 對廢舊電池進行回收處理 | ||
| C. | 將塑料垃圾埋入地下或者傾倒入海 | D. | 使用沼氣、太陽能、風能等代替煤炭 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 實驗操作 | 實驗現象 |
| ①取10ml一定溶質質量分數的硫酸銅溶液,倒入50ml的燒杯里 ②取一塊鈉,用濾紙吸干表面煤油,再切取綠豆大小的一塊,投入溶液中 | 鈉浮在液面上,熔化成閃亮小球,鈉球游動,發出“嘶嘶”的聲響,析出藍色沉淀 |
| 實驗操作 | 實驗現象 | 結論 |
| 取燒杯中少許沉淀于試管中,再向其中加入過量的稀硫酸 | 沉淀全部溶解,溶液變藍色 | 說明沉淀中不含紅色的銅 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com