
【題目】下列生活中的做法不恰當的是( )
A.貯氯罐意外泄漏,應沿逆風方向疏散群眾
B.鋁制餐具不宜長期存放酸性、堿性或咸的食物
C.氫氧化鋁可作胃酸的中和劑
D.氯氣車間液氯泄漏時,應彎腰逃離氯氣泄漏區域
 活力課時同步練習冊系列答案
活力課時同步練習冊系列答案科目:高中化學 來源: 題型:
【題目】某實驗小組用下列裝置進行乙醇催化氧化的實驗。

(1)實驗過程中銅網出現紅色和黑色交替的現象,請寫出相應的化學反應方程式:______________________________________________。
在不斷鼓入空氣的情況下,熄滅酒精燈,反應仍能繼續進行,說明該乙醇氧化反應是________反應。
(2)甲和乙兩個水浴作用不相同。
甲的作用是__________________________;乙的作用是__________________________。
(3)反應進行一段時間后,干燥試管a中能收集到不同的物質,它們是________________。集氣瓶中收集到的氣體的主要成分是__________________________。
(4)若試管a中收集到的液體用紫色石蕊試紙檢驗,試紙顯紅色,說明液體中還含有__________。要除去該物質,可先在混合液中加入________________(填寫字母)。
a.氯化鈉溶液 b.苯
c.碳酸氫鈉溶液 d.四氯化碳
然后,再通過________________(填實驗操作名稱)即可除去。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配制一定物質的量濃度的NaCl溶液時,導致濃度偏高的原因可能是
A. 移液時,不慎將液體流到瓶外 B. 容量瓶盛過NaCl溶液,使用前未洗滌
C. 容量瓶中原有少量的蒸餾水 D. 定容時讀數仰視
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生用鋅片、銅片、發光二極管、濾紙、導線等在玻璃片制成如圖所示的原電池,當濾紙用醋酸溶液潤濕時,二極管發光.下列有關該電池的說法正確的是( )
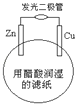
A. 銅片上的電極反應:Cu — 2e﹣ = Cu2+
B. 鋅片為電池的負極
C. 外電路中電子由銅片經導線流向鋅片
D. 電池工作時電能直接轉化為化學能
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】砷(As)及其化合物與生產、生活密切相關,廣泛應用在殺蟲劑以及藥物中。回答下列問題:
(1)砷是第四周期VA族元素。下列關于第VA族元素及其化合物的說法不正確的是_______(填序號)。
a.沸點:PH3<NH3
b.酸性:HNO3>H3AsO4
c.As的氧化物的水化物是強堿
d.形成的簡單離子半徑隨著原子序數遞增而增大
(2)工業生產中常用“古氏試砷法”檢驗微量砷,其反應原理為:
①將含砷化合物轉化為具有極強還原性的AsH3;
②AsH3與AgNO3溶液反應產生As2O3與另一種固體,該反應的離子方程式為_____________。
(3)砷及其化合物幾乎都有毒,通常+3價砷化合物毒性強于+5價砷化合物。海產品中含有微量+5價砷化合物,食用海鮮后不能馬上進食水果的原因是________________________________。
(4)砷酸(H3AsO4)可用于制造殺蟲劑、藥物。As2O3溶于稀硝酸中可得砷酸,此反應的化學方程式為________________________________。
(5)利用單質鐵處理水體砷污染的原理為:單質鐵在水體中被氧化腐蝕得到水合氧化鐵[Fe(OH)3和FeOOH],吸附沉降砷的化合物。在其它條件一定時,調節水樣的pH,得到除砷效率曲線如圖所示。
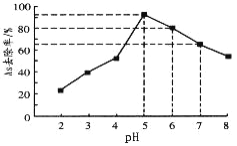
①請解釋水樣酸性較強時,除砷效率較低的原因是_____________________。
②國家飲用水標準規定水中砷的含量應低于0.05mg·L-1(1mg=1000μg)。某水樣中含砷總濃度為100μg·L-1,若控制水樣的pH=6,出水后的砷濃度_________________(填“能”或“否”)達到飲用水標準。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】F、Cl和Br都是VIIA族元素,關于這三種元素原子說法正確的是
A.原子半徑:F>C1>BrB.最外層電子數都相同
C.核外電子層數都相同D.最外層電子數都不相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】兩種氣態烴組成的混合氣體完全燃燒后所得到CO2和H2O的物質的量隨混合烴總物質的量的變化如圖所示,則下列對混合烴的判斷正確的是( )

①一定有乙烯 ②一定有甲烷 ③一定有丙烷
④一定沒有乙烷 ⑤可能有甲烷 ⑥可能有乙炔
A. ①②B. ②④C. ②⑥D. ②④⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I:運用化學反應原理知識研究如何利用CO、SO2等污染物有非常重要的意義。
(1)用CO可以合成甲醇。
已知: CH3OH(g)+3/2 O2(g)=CO2(g)+2H2O(l) △H1
CO(g)+1/2O2(g)=CO2(g) △H2
H2(g)+1/2O2(g)=H2O(l) △H3
請寫出由CO和H2形成CH3OH的熱化學方程式___________________________________________
(2)—定壓強下,在容積為2L的密閉容器中充入1mol CO與2mol H2,在催化劑作用下發生反應:
CO(g) +2H2(g)![]() CH3OH(g) △H,CO轉化率與溫度、壓強的關系如圖所示:
CH3OH(g) △H,CO轉化率與溫度、壓強的關系如圖所示:

①下列說法正確的是__________
A.若容器內氣體密度恒定,反應達到平衡狀態
B.若容器內各氣體平均相對分子質量恒定,反應達到平衡狀態
C.若v(CO)=v(CH3OH)時,反應達到平衡狀態
D.反應中,催化劑使平衡向正反應方向移動
②該反應的△H________0,p2_______________p1(填“大于”“小于”或“等于”)。
③100℃時,該反應的化學平衡常數K=__________.

II:甲醇是一種燃料,也可以作為燃料電池的原料
(3)甲醇直接燃燒會產生一定的污染,某實驗小組依據甲醇燃燒的反應原理,設計如圖所示的電池裝置,則電池正極的電極反應式:______,該電池工作時,溶液中的OH-向______極移動,該電池工作一段時間后,測得溶液的pH減小,則該電池總反應的離子方程式為_______________________________________;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com