
【題目】常溫下,將20.0g質量分數為14.0%的KHCO3溶液跟30.0g質量分數為24.0%的KHCO3溶液混合,得到密度為1.15g·cm-3的混合溶液。計算:
(1)混合后溶液的質量分數__________。
(2)混合后溶液的物質的量濃度________。
(3)在1000g水中需溶解___________摩爾KHCO3才能使其濃度恰好與上述混合后溶液的濃度相等?
【答案】 20% 2.3 mol·L-1 2.5mol
【解析】(1)20.0g質量分數為14.0%的KHCO3溶液中溶質的質量m1=20.0g×14.0%=2.8g;30.0g質量分數為24.0%的KHCO3溶液溶質的質量m2=30.0g×24.0%=7.2g,溶液混合前后溶質、溶液的質量都不變,所以混合液的質量分數為![]() ×100%=20%,答:混合后溶液的質量分數為20%;
×100%=20%,答:混合后溶液的質量分數為20%;
(2)混合液中溶質的質量為2.8g+7.2g=10g,溶質的物質的量為n=![]() =0.1mol,溶液的體積為V=
=0.1mol,溶液的體積為V=![]() =
=![]() L,所以溶液的物質的量濃度為c=
L,所以溶液的物質的量濃度為c=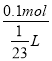 =2.3mol/L,答:混合后溶液的物質的量濃度為2.3mol/L;
=2.3mol/L,答:混合后溶液的物質的量濃度為2.3mol/L;
(3)設需要KHCO3的物質的量為xmol,KHCO3的質量為100x,根據(1)可知,KHCO3的質量分數為20%,則ω=20%=![]() =
=![]() ×100%,解得:x=2.5mol,答:在1 000g水中需溶解2.5mol KHCO3才能使其濃度恰好與上述混合后溶液的濃度相等。
×100%,解得:x=2.5mol,答:在1 000g水中需溶解2.5mol KHCO3才能使其濃度恰好與上述混合后溶液的濃度相等。


科目:高中化學 來源: 題型:
【題目】實驗室現有一瓶標簽右半部分已被腐蝕的固體M,剩余部分只看到“Na2S”字樣(如圖所示)。已知固體M只可能是Na2SO3、Na2SiO3、Na2SO4中的一種。若取少量固體M配成稀溶液進行下列有關實驗,其中說法正確的是( )

A. 往溶液中通入二氧化碳,若有白色沉淀,則固體M為Na2SiO3
B. 往溶液中加入稀鹽酸酸化的BaCl2,若有白色沉淀,則固體M為Na2SO4
C. 用pH試紙檢驗,若pH=7,則固體M不一定是Na2SO4
D. 只用鹽酸一種試劑不能確定該固體M的具體成分
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子能大量共存的是( )
A. Na+ H+ NO3- Fe2+ B. Ca2+ H+ ClO- NO3-
C. K+ H+ Cl- SO42- D. Fe3+ Cl- H+ CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有A、B、C、D、E五種可溶性強電解質,它們在水中可電離產生下列離子(各離子不重復):
陽離子:H+、Na+、Al3+、Ag+、Ba2+
陰離子:OH-、Cl-、CO32-、NO3-、SO42-
已知:①A、B兩溶液呈堿性,C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至過量,沉淀量先增加后減少但不消失。
③D溶液與另外四種溶液反應都能產生沉淀。
請回答下列問題:
(1)寫出A與D的化學式: A________,D________。
(2)寫出A與E溶液反應的離子方程式:_______ 。
(3)已知:NaOH(aq)+HNO3(aq) = NaNO3(aq)+H2O(l) ΔH=-a kJ·mol-1。請寫出表示相同條件下B與C的稀溶液反應的中和熱的熱化學方程式: ________
(4)若25 ℃時,C、E及醋酸三種溶液的pH=4,則E和C溶液中由水電離出的c(H+)的比是________;將C與醋酸混合,醋酸的電離程度將________ (填“增大”“不變”或“減小”)(水的濃度視為常數)。
(5)用惰性電極電解0.1 mol·L-1 D與0.1 mol·L-1C各100 mL混合后的溶液,電解一段時間后,陰極質量________ (填“增大”“不變”或“減小”,下同);溶液的pH ________。
(6)向(5)中所得溶液中加入足量鐵粉,則所能溶解的鐵粉質量為________g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)AgNO3的水溶液呈________(填“酸”、“中”或“堿”)性,原因是(用離子方程式表示):______________;實驗室在配制AgNO3的溶液時,常將AgNO3固體先溶于_______中,然后再用蒸餾水稀釋到所需的濃度,以________(填“促進”或“抑制”)其水解。
(2)明礬可用于凈水,原因是(用離子方程式表示)______________。把FeCl3溶液蒸干、灼燒,最后得到的主要固體產物是________。
(3)用熱的純堿溶液洗滌餐具,原因是(用離子方程式表示)_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是中學化學中常用于混合物的分離和提純的裝置,請根據裝置回答問題:

(1)除去自來水中的Ca2+、Mg2+、Cl—、SO42—等雜質,選擇裝置_____________(填代表裝置圖的字母)。
(2)用CCl4萃取碘水中的I2,有機層的顏色為___________________。
(3)裝置A中①的名稱是_____________,進水的方向是_____________。裝置B在分液時為使液體順利滴下,應進行的具體操作是_____________。
(4)海水中蘊藏著豐富的資源,在實驗室中取少量海水,進行如下流程的實驗:

問題1:粗鹽中含Ca2+、Mg2+、Fe3+、SO42-等雜質,需要提純后才能綜合利用。粗鹽提純的步驟有:①加入過量的Na2CO3溶液;②加入過量的BaCl2溶液;③加入過量的NaOH溶液;④調節溶液的pH等于7;⑤溶解;⑥過濾;⑦蒸發。
正確的操作順序是_____________(填寫字母)。
a.⑤②③①⑥④⑦b.⑤①②③⑥④⑦ c.⑤③②①⑥④⑦d.⑤②①③④⑥⑦
問題2:由海水到氯化鈉晶體的實驗過程中要用到的主要裝置是_____________(從給定的四種裝置中選擇,填字母)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】判斷下列鹽溶液的酸堿性,能發生水解的用離子方程式表示,不能發生水解的請寫上“不發生水解”字樣。
K2CO3溶液呈 性 ;
K2SO4溶液呈 性 ;
FeCl3溶液呈 性 ;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com