
【題目】常溫下,濃度均為0.1 mol·Lˉ1的NaOH溶液和氨水,下列說法正確的是
A. c(NH3H2O) + c(![]() ) = c(Na+)
) = c(Na+)
B. NH3·H2O的電離方程式:NH3H2O ===![]() + OH-
+ OH-
C. 氨水的pH大于NaOH溶液
D. 將濃度為0.1 mol·Lˉ1的鹽酸和氨水等體積混合后,所得溶液中:c(OH-) > c(H+)
 挑戰100單元檢測試卷系列答案
挑戰100單元檢測試卷系列答案 名題金卷系列答案
名題金卷系列答案科目:高中化學 來源: 題型:
【題目】下列有關金屬腐蝕與防護的說法正確的是( )

A. 圖1中,插入海水中的鐵棒,越靠近底端,腐蝕越嚴重
B. 鍍層破損后,鍍鋅鐵比鍍錫鐵更耐用
C. 純銀器表面在空氣中因電化學腐蝕漸漸變暗
D. 圖2中,金屬棒X若為Cu,可使埋在地下的鋼管免受腐蝕
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲、乙兩同學欲制取純凈的Fe(OH)2 ,根據如圖所示的裝置進行試驗。A管中是Fe+H2SO4 , B管中是NaOH溶液,請回答下列問題。
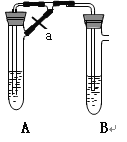
(1)同學甲:先夾緊止水夾a,使A管開始反應,在B管中觀察到的現象是 。
(2)同學乙:打開a,使A管中反應一段時間再 夾緊止水夾a,實驗中在B管中觀察到的現象是 ,B中發生反應的離子方程式為
(3)同學乙打開a的目的 ; (填甲或乙)同學可成功。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是某學校實驗室從化學試劑商店買回的硫酸試劑標簽上的部分內容。

(1)硫酸具有A-D所示的性質,以下過程主要表現了濃硫酸的那些性質?請將選項字母填在下列各小題的橫線上: A強酸性 B 吸水性 C 脫水性 D 強氧化性
①濃硫酸使木條變黑__________
②熱的濃硫酸與銅片反應__________
(2)現用該濃硫酸配制100mL 1mol/L的稀硫酸。可供選用的儀器有:①膠頭滴管;②燒瓶;③燒杯;④ 藥匙;⑤量筒;⑥托盤天平。請回答下列問題:
配制稀硫酸時,上述儀器中不需要使用的有__________(選填序號),還缺少的儀器有__________(寫儀器名稱);
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數值。下列有關敘述正確的是
A. 標準狀況下,11.2L14CO2含有的中子數為11NA
B. 5.6gFe粉與足量S粉加熱充分反應轉移的電子數為0.2NA,
C. 1molNa2O2固體中所含離子數目為4NA
D. 1LpH=6的純水中含有OHˉ的數目為10-8NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若定義pC是溶液中微粒物質的量濃度的負對數,則常溫下,一定濃度的某酸(H2A)水溶液中pC(H2A)、pC(HAˉ)、pC(A2-)隨著溶液pH的變化曲線如圖所示。下列說法一定正確的是

A. pH=4時,c(HAˉ)<c(A2-)
B. c(H2A)+c(HAˉ)+c(A2-)是定值
C. 該酸的電離常數Ka1=10-1.3
D. 常溫下,NaHA的水溶液呈堿性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳、氮、氧、氯、鈉、銅等元素的化合物廣泛存在于自然界,回答下列問題:
(1)基態氯原子的價電子排布圖是________________________;基態銅原子核外電子占有的空間運動狀態有____________種
(2)碳、氮、氧三種元素中第一電離能最大的是____________ (填元素符號)CO32-中碳原子的雜化軌道類型為____________。
(3)相同條件下,水的沸點高于液氨,原因是________________________。
(4)銅與CNˉ可形成絡合離子[Cu(CNˉ)4]2-,寫出一種與CNˉ互為等電子體的分子的化學式____________;1 mol[ Cu(CNˉ)4]2-中含有____________molσ鍵;若將[Cu(CNˉ)4]2-中二個CNˉ換為Clˉ,只有一種結構,則[Cu(CNˉ)4]2-中4個氮原子所處空間位置關系為_________。
(5)氯化鈉的晶胞如圖所示。晶體中氯離子以面心立方最密堆積排列,鈉離子嵌入在氯離子之間的空隙中。一個氯離子周圍離氯離子最近的氯離子數目為__________個。已知:半徑r(Clˉ)=apm,r(Na+)=bpm。摩爾質量M(NaCI)=cg·mol-1則氯化鈉晶體的密度為_________g·cm-3

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三鹽基硫酸鉛(3PbO·PbSO4·H2O) (相對分子質量為990)簡稱“三鹽”,白色或微黃色粉末,熱穩定性能優良,主要用作聚氯乙烯的熱穩定劑。“三鹽”是由可溶性鉛鹽中加入硫酸生成硫酸鉛,再加氫氧化鈉而制得。以100.0噸鉛泥(主要成分為PbO、Pb及PbSO4等)為原料制備三鹽的工藝流程如下圖所示。

已知:(1)Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13;(2)鉛與冷鹽酸、冷硫酸幾乎不起作用。
請回答下列問題:
(1)寫出步驟①“轉化”的化學方程式______________________________________。
(2)步驟③“酸溶”,最適合選用的酸為______________,為提高酸溶速率,可采取的措施是__________(任意寫出一條)。
(3)若步驟④沉鉛”后的濾液中c(Pb2+)=1.82×10-5mol/L,則此時c(SO42-)=______mol/L。
(4)從原子利用率的角度分析該流程的優點為_______________________。
(5)步驟⑥“合成”三鹽的化學方程式為____________________________。若得到純凈干燥的三鹽49.5t,假設鉛泥中的鉛元素有80%轉化為三鹽,則鉛泥中鉛元素的質量分數為__ % (結果保留一位小數)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上可用硫酸銀與硫黃培燒制備氧化鋁,再電解氧化鋁,發生反應如下:反應Ⅰ:2A12(SO4)3+3S![]() 2Al2O3+9SO2↑
2Al2O3+9SO2↑
反應Ⅱ:2Al2O3![]() 4Al+3O2↑
4Al+3O2↑
下列說法正確的是
A. 反應Ⅰ中S 單質是氧化劑
B. 反應Ⅱ中鋁元素被氧化
C. 當生成5.4gAl時,反應Ⅰ和Ⅱ共轉移1.2mole-
D. 反應Ⅰ中氧化產物與還原產物物質的量之比為2:9
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com