
 =
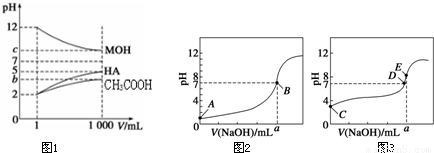
= ,平衡正移n(H+)增大,n(CH3COOH)減小,故比值增大,故B正確;
,平衡正移n(H+)增大,n(CH3COOH)減小,故比值增大,故B正確;

 桃李文化快樂暑假武漢出版社系列答案
桃李文化快樂暑假武漢出版社系列答案 優秀生快樂假期每一天全新寒假作業本系列答案
優秀生快樂假期每一天全新寒假作業本系列答案 暑假接力賽新疆青少年出版社系列答案
暑假接力賽新疆青少年出版社系列答案科目:高中化學 來源: 題型:

 CH3COOH+OH-
CH3COOH+OH- CH3COOH+OH-
CH3COOH+OH-查看答案和解析>>
科目:高中化學 來源: 題型:
| △ |

| KMnO4 |
| H+ |










 、
、
 、
、
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
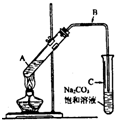 (2009?成都一模)某興趣小組利用如圖裝置,取不同濃度的硫酸與 3mL 無水乙醇和 2mL 冰醋酸分別進行制取乙酸乙酯的研究.
(2009?成都一模)某興趣小組利用如圖裝置,取不同濃度的硫酸與 3mL 無水乙醇和 2mL 冰醋酸分別進行制取乙酸乙酯的研究. CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O| 組序號 | 催化劑 | 反應現象 | C中飽和碳酸鈉溶液中酯層高度 |
| ① | 2mL98%濃硫酸 | 20秒時溶液出現棕色,隨反應進行,溶液顏色逐漸加深,最后成黑色;酯層無氣泡. | 2.10cm |
| ② | 2mL14mol?L-1硫酸 | 反應后溶液顏色呈棕色,酯層與飽和碳酸鈉溶液界面清晰,無氣泡. | 2.14cm |
| ③ | 2mL10mol?L-1硫酸 | 反應后溶液顏色呈無色,酯層與飽和碳酸鈉溶液界面清晰,無氣泡. | 2.16cm |
| ④ | 2mL7mol?L-1硫酸 | 反應后溶液顏色呈無色,酯層與飽和碳酸鈉溶液有氣泡. | 2.00cm |
| △ |
| △ |
查看答案和解析>>
科目:高中化學 來源:新課標2011屆度上學期高三一輪復習單元測試1(新人教) 題型:選擇題
在催化劑作用下乙酸可通過兩步反應得乙烷,反應原理如下:
①CH3COOH+2H2→CH3CH2OH+H2O
②CH3CH2OH+H2→CH3CH3+H2O
③CH3COOH+3H2→CH3CH3+2H2O
在反應過程中乙酸和乙醇會生成乙酸乙酯。為研究分別考查了加Mo(鉬)和不加Mo負載型Ni(鎳)催化劑催化效能,某文獻記載的數據如下:
|
|
乙酸轉化率 |
未反應的含氧化合物含量 |
||||
|
乙酸 |
乙醇 |
|||||
|
溫度/℃ |
Mo16Ni6 |
Ni6 |
Mo16Ni6 |
Ni6 |
Mo16Ni6 |
Ni6 |
|
240 |
87.2 |
21.8 |
0.53 |
3.24 |
1.03 |
0.14 |
|
260 |
89.1 |
27.2 |
0.45 |
3.02 |
0.99 |
0.19 |
下列說法不正確的是 ( )
A.上述①②③三反應均屬于加成反應
B.上述①②③三反應均屬于還原反應
C.乙酸加氫脫氧反應260℃比240℃下進行更有利
D.Mo16Ni6催化性能比Ni6好
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com