
| A. | 得到2.54g沉淀時,加入Na0H溶液的體積是600ml | |
| B. | 該濃硝酸稀釋至100mL時,HNO3的物質的量濃度是7mol•L-1 | |
| C. | 該合金中鎂與銅的質量之比是3:16 | |
| D. | NO2和N2O4的混合氣體中,N2O4的物質的量是0.01mol |
分析 金屬離子全部沉淀時,得到2.54g沉淀為氫氧化銅、氫氧化鎂,故沉淀中氫氧根的質量為:2.54g-1.52g=1.02g,氫氧根的物質的量為:$\frac{1.02g}{17g/mol}$=0.06mol,根據電荷守恒可知,金屬提供的電子物質的量等于氫氧根的物質的量,設銅、鎂合金中Cu、Mg的物質的量分別為xmol、ymol,則:$\left\{\begin{array}{l}{2x+2y=0.06}\\{64x+24y=1.52}\end{array}\right.$,解得:x=0.02,y=0.01,
A.反應后溶質為硝酸鈉,根據氮元素守恒計算硝酸鈉的物質的量,根據鈉離子守恒可知n(NaOH)=n(NaNO3),再根據V=$\frac{n}{c}$計算需要氫氧化鈉溶液的體積;
B.根據c=$\frac{1000ρω}{M}$計算該濃硝酸的物質的量濃度,然后根據稀釋過程中溶質的物質的量不變計算出稀釋后硝酸溶液濃度;
C.根據分析計算出該合金中鎂與銅的質量之比;
D.根據n=$\frac{V}{{V}_{m}}$計算NO2和N2O4混合氣體的物質的量,設二氧化氮的物質的量為amol,根據電子轉移列方程計算.
解答 解:金屬離子全部沉淀時,得到2.54g沉淀為氫氧化銅、氫氧化鎂,故沉淀中氫氧根的質量為:2.54g-1.52g=1.02g,氫氧根的物質的量為:$\frac{1.02g}{17g/mol}$=0.06mol,根據電荷守恒可知,金屬提供的電子物質的量等于氫氧根的物質的量,設銅、鎂合金中Cu、Mg的物質的量分別為xmol、ymol,則:$\left\{\begin{array}{l}{2x+2y=0.06}\\{64x+24y=1.52}\end{array}\right.$,解得:x=0.02,y=0.01,
A.反應后溶質為硝酸鈉,根據氮元素守恒可知,硝酸鈉的物質的量為0.05L×14mol/L-0.04mol-(0.05-0.04)×2=0.64mol,根據鈉離子守恒可知n(NaOH)=n(NaNO3)=0.64mol,故需要氫氧化鈉溶液的體積為:$\frac{0.64mol}{1mol/L}$=0.64L=640mL,故A錯誤;
B.該濃硝酸密度為1.40g/mL、質量分數為63%,故該濃硝酸的物質的量濃度為:$\frac{1000×1.4×63%}{63}$mol/L=14mol/L,將50mL該濃硝酸稀釋至100mL時,溶液濃度變為原先的一半,為7mol/L,故B正確
C.該合金中鎂與銅的物質的量之比=(24g/mol×0.01mol):(64g/mol×0.02mol)=3:16,故C正確;
D.NO2和N2O4混合氣體的物質的量為:$\frac{1.12L}{22.4L/mol}$=0.05mol,設二氧化氮的物質的量為amol,則四氧化二氮的物質的量為(0.05-a)mol,根據電子轉移守恒可知,a×1+(0.05-a)×2×1=0.06,解得a=0.04,則四氧化二氮的物質的量為:0.05mol-0.04mol=0.01mol,故D正確;
故選A.
點評 本題考查混合物的有關計算、氧化還原反應的計算,題目難度中等,理解反應發生的過程是關鍵,是對學生綜合能力的考查,注意根據守恒思想進行的解答,試題培養了學生的分析能力及化學計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | CO2和SiO2都能與堿及堿性氧化物反應 | |
| B. | CO2和SiO2都能與水反應生成相應的酸 | |
| C. | CO2和SiO2都能與焦炭反應生成CO | |
| D. | SiO2可用于制光導纖維,干冰可用于人工降雨 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Y和Z可以組成一種Y和Z的質量比為7:20的化合物 | |
| B. | X、Y、Z組成的一種離子化合物,其中X、Y、Z元素原子個數比可能為4:2:3 | |
| C. | X和Z可以形成X2Z和X2Z2型化合物,所含共價鍵類型不完全相同 | |
| D. | 由X、Y、Z三種元素中的任意兩種組成的具有10電子的微粒有2種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
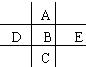 如圖為周期表前四周期的一小部分,A、B、C、D、E的位置關系如圖所示.其中B元素的最高價是負價絕對值的3倍,它的最高氧化物中含氧60%,回答下列問題:
如圖為周期表前四周期的一小部分,A、B、C、D、E的位置關系如圖所示.其中B元素的最高價是負價絕對值的3倍,它的最高氧化物中含氧60%,回答下列問題: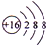 .A單質的電子式為
.A單質的電子式為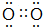 .
.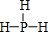 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe2O3 | B. | FeO | C. | Fe(OH)2 | D. | Fe(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用氨水洗滌試管內壁上的“銀鏡” | |
| B. | 只用溴水鑒別苯、CCH4、KI溶液、Na2SO4溶液 | |
| C. | 為加快過濾速度,用玻璃棒攪拌過濾器中的食鹽水 | |
| D. | 為迅速除去乙酸乙酯中的少量乙酸,加入足量NaOH溶液并加熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯水是指氯氣的水溶液 | |
| B. | 在pH試紙上滴新制氯水,試紙會先變紅后褪色 | |
| C. | 久置的氯水漂白作用更強 | |
| D. | 新制氯水應避光保存 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com