
(1)已知:① TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
②2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
寫出TiO2和焦炭、氯氣反應生成液態(tài)TiCl4和CO氣體的熱化學方程式:________________。
(2)有一類甲醇質子交換膜燃料電池,需將甲醇蒸氣轉化為氫氣,兩種反應原理是:
A.CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
B.CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-676.7 kJ·mol-1
由上述方程式可知,CH3OH的標準燃燒熱________(填“大于”“等于”“小于”或“不能確定”)-676.7 kJ·mol-1。已知水的氣化熱為44 kJ·mol-1,則氫氣燃燒的熱化學方程式為__________________________。
(1)TiO2(s)+2C(s)+2Cl2(g)=TiCl4(l)+2CO(g) ΔH=-81 kJ·mol-1
(2)不能確定 H2(g)+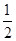 O2(g)=H2O(l) ΔH=-285.9
kJ·mol-1
O2(g)=H2O(l) ΔH=-285.9
kJ·mol-1
【解析】
試題分析:(1)將①+②可得:TiO2(s)+2C(s)+2Cl2(g)=TiCl4(l)+2CO(g) ΔH=-81 kJ·mol-1
(2)由于A產物是氫氣,不是化合物,B產物是氣態(tài)的水,不是穩(wěn)定的化合物的狀態(tài)。所以不能確定CH3OH的標準燃燒熱。將(A─B)÷3可得:H2(g)+1/2O2(g)=H2O(g)
ΔH= -241.9KJ/mol.由于水的氣化熱為44 kJ·mol-1,所以氫氣燃燒的熱化學方程式為:H2(g)+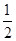 O2(g)=H2O(l) ΔH=-285.9
kJ·mol-1
O2(g)=H2O(l) ΔH=-285.9
kJ·mol-1
考點:考查蓋斯定律及應用。


 優(yōu)學名師名題系列答案
優(yōu)學名師名題系列答案科目:高中化學 來源: 題型:
| 電離能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 737 | 1451 | 7733 | 10540 |

查看答案和解析>>
科目:高中化學 來源: 題型:
 X、Y、Z三種元素,原子序數依次減小.X是第四周期主族元素,其部分電離能如圖1所示;X、Y元素具有相同的最高正化合價;Z元素是形成化合物種類最多的元素.回答下列問題:
X、Y、Z三種元素,原子序數依次減小.X是第四周期主族元素,其部分電離能如圖1所示;X、Y元素具有相同的最高正化合價;Z元素是形成化合物種類最多的元素.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
| 滴定 序號 |
待測液體積/mL | NH4Fe(SO4)2標準溶液 滴定管起點讀數/mL |
NH4Fe(SO4)2標準溶液 滴定管終點讀數/mL |
| 1 | 25.00 | 0.02 | 24.02 |
| 2 | 25.00 | 0.08 | 24.06 |
| 3 | 25.00 | 0.12 | 24.14 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||
| ||
查看答案和解析>>
科目:高中化學 來源:2011-2012學年遼寧省沈陽二中高二下學期期中考試化學試卷(帶解析) 題型:填空題
(6分)鈦(Ti)被譽為“21世紀的金屬”。工業(yè)上將TiO2與焦炭混合,通入Cl2高溫下制得TiCl4;再將TiCl4提純后,在氬氣保護下與鎂高溫反應制得Ti。其反應如下:
①TiO2+2Cl2+2C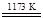 TiCl4+2CO ②TiCl4+2Mg
TiCl4+2CO ②TiCl4+2Mg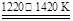 Ti+2MgCl2
Ti+2MgCl2
回答下列問題:
(1)已知TiCl4在通常情況下是無色液體,熔點為–37℃,沸點為136℃;TiCl4在潮濕空氣中易水解產生白霧,同時產生H2TiO3固體。
① TiCl4為______晶體(填“離子”、“原子”或“分子”)。
② TiCl4分子為正四面體形,則Ti為________雜化。
③ TiCl4在潮濕空氣中水解的化學方程式是_________________________________。
(2)配離子[TiCl(H2O)5]2+的中心離子化合價為 ,中心離子配位數為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com