
分析 A、B、C、D、E、F六種短周期主族元素,原子序數依次增大,E是地殼中含量最高的金屬元素,則E是Al元素;C、F同主族,C元素核電荷數只有F元素的一半,二者原子序數相差8,則C是O、F是S元素;1mol D單質跟水反應放出11.2L(標準狀況)A氣體單質,且原子序數小于E而大于O元素,則D是Na元素、A是H元素;
B元素原子的最外層電子數為電子層數的兩倍,且原子序數小于O元素,則B是C元素;
(1)主族元素原子核外電子層數等于其周期數,最外層電子數等于其族序數;
(2)C、D、F分別是O、Na、S元素,這三種元素形成的化合物是硫酸鈉、亞硫酸鈉,硫酸鈉和亞硫酸鈉都是由陰陽離子構成的;
(3)由H、O、Na、S四種元素形成的兩種化合物(均含四種元素)能發生化學反應生成一種氣體,這兩種化合物分別是亞硫酸氫鈉、硫酸氫鈉,二者反應生成二氧化硫和水.
解答 解:A、B、C、D、E、F六種短周期主族元素,原子序數依次增大,E是地殼中含量最高的金屬元素,則E是Al元素;C、F同主族,C元素核電荷數只有F元素的一半,二者原子序數相差8,則C是O、F是S元素;1mol D單質跟水反應放出11.2L(標準狀況)A氣體單質,且原子序數小于E而大于O元素,則D是Na元素、A是H元素;
B元素原子的最外層電子數為電子層數的兩倍,且原子序數小于O元素,則B是C元素;
(1)F是S元素,S原子核外有3個電子層、最外層電子數是6,所以位于第三周期第VIA族,
故答案為:3;Ⅵ;
(2)C、D、F分別是O、Na、S元素,這三種元素形成的化合物是硫酸鈉、亞硫酸鈉,硫酸鈉和亞硫酸鈉都是由陰陽離子構成的,所以屬于離子晶體,故答案為:離子晶體;
(3)由H、O、Na、S四種元素形成的兩種化合物(均含四種元素)能發生化學反應生成一種氣體,這兩種化合物分別是亞硫酸氫鈉、硫酸氫鈉,二者反應生成二氧化硫和水,離子方程式為HSO3-+H+=H2O+SO2↑,
故答案為:HSO3-+H+=H2O+SO2↑.
點評 本題考查位置結構性質相互關系及應用,涉及離子方程式的書寫、晶體類型判斷、元素在周期表中的位置等知識點,正確判斷元素是解本題關鍵,注意離子方程式書寫規則,為易錯點.


科目:高中化學 來源: 題型:選擇題
| A. | 5.4KJ | B. | 350KJ | C. | 3.5KJ | D. | 8.5KJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L辛烷的分子數為NA | |
| B. | 1 mol甲基(-CH3)所含的電子總數為9NA | |
| C. | 0.5 mol 1,3-丁二烯分子中含有C=C雙鍵數為 NA | |
| D. | 28gC2H4所含共用電子對數目為6NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl是取代反應 | |
| B. | CH2=CH2+Br2→CH2Br-CH2Br是加成反應 | |
| C. | 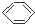 +HO-NO2$→_{60℃}^{濃硫酸}$ +HO-NO2$→_{60℃}^{濃硫酸}$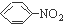 +H2O是取代反應 +H2O是取代反應 | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O是加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.6 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.6 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2H2+O2 $\frac{\underline{\;點燃\;}}{\;}$2H2O | |
| B. | CaO+H2O=Ca(OH)2 | |
| C. | CaCO3 $\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ | |
| D. | CH3CH2OH(酒精)+3O2 $\frac{\underline{\;點燃\;}}{\;}$2CO2+3 H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com