
【題目】氯化亞銅(CuCl)可用作催化劑、殺菌劑、媒染劑、脫色劑。CuCl是一種白色粉末,微溶于水、不溶于乙醇,在潮濕的空氣中易被氧化。實驗室采用如圖裝置和下列步驟制備氯化亞銅。
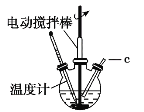
步驟1:在三頸燒瓶中加入20%鹽酸、食鹽、銅屑,加熱至60~70℃,開動攪拌器,同時從c口緩慢通入氧氣,制得Na[CuCl2]溶液。
步驟2:反應完全后,冷卻,過濾,濾液用適量的水稀釋,析出CuCl。
步驟3:過濾,分別用鹽酸、乙醇洗滌濾出的固體。
步驟4:在真空干燥器中60~70 ℃干燥2h,冷卻后得到產(chǎn)品。
回答下列問題:
(1)質(zhì)量分數(shù)為20%的鹽酸密度為1.1g/cm3,物質(zhì)的量濃度為___________;配制20%鹽酸需要的玻璃儀器有:__________、燒杯、玻璃棒、膠頭滴管。
(2)步驟1中制得Na[CuCl2]的化學方程式為________________________________。
(3)根據(jù)“步驟2中用水稀釋濾液能得到CuCl”推測,濾液中存在的平衡是____________。
(4)析出的CuCl晶體不用水而用鹽酸、乙醇分別洗滌的目的是__________________。
(5)測定產(chǎn)品中氯化亞銅的質(zhì)量分數(shù),實驗過程如下:
準確稱取制備的氯化亞銅產(chǎn)品0.25 g,將其置于足量的FeCl3溶液中,待樣品全部溶解后,加入適量稀硫酸,用0.10 mol/L的硫酸鈰[Ce(SO4)2]標準溶液滴定到終點,消耗硫酸鈰溶液24.50 mL,反應中Ce4+被還原為Ce3+。(已知:CuCl+FeCl3=CuCl2+FeCl2)
①硫酸鈰標準溶液應盛放在________(填“酸”或“堿”)式滴定管中。
②產(chǎn)品中氯化亞銅的質(zhì)量分數(shù)為________。
【答案】6.0mol/L 量筒 4HCl(濃)+4NaCl+4Cu+O2![]() 4Na[CuCl2]+2H2O [CuCl2]-(aq)
4Na[CuCl2]+2H2O [CuCl2]-(aq) ![]() CuCl(s)+Cl-(aq) 用鹽酸洗滌可以減小溶解導致的損失;用乙醇洗滌可以使晶體迅速干燥,避免CuCl被氧化 酸 97.51%
CuCl(s)+Cl-(aq) 用鹽酸洗滌可以減小溶解導致的損失;用乙醇洗滌可以使晶體迅速干燥,避免CuCl被氧化 酸 97.51%
【解析】
(1)根據(jù)物質(zhì)的量濃度與質(zhì)量分數(shù)換算關(guān)系可得該溶液的物質(zhì)的量濃度為c=![]() ;配制20%鹽酸,由于溶質(zhì)為液體,所以需要的玻璃儀器有:量筒、燒杯、玻璃棒、膠頭滴管;
;配制20%鹽酸,由于溶質(zhì)為液體,所以需要的玻璃儀器有:量筒、燒杯、玻璃棒、膠頭滴管;
(2)根據(jù)步驟I所述可知:NaCl、HCl、Cu、O2在加熱時服用產(chǎn)生Na[CuCl2],同時產(chǎn)生H2O,根據(jù)原子守恒、電子守恒,可得反應的化學方程式為:4HCl(濃)+4NaCl+4Cu+O2![]() 4Na[CuCl2]+2H2O;
4Na[CuCl2]+2H2O;
(3)步驟2操作是反應完全后,冷卻,過濾,濾液用適量的水稀釋,析出CuCl,說明[CuCl2]-在溶液中存在電離平衡:[CuCl2]-(aq)![]() CuCl(s)+Cl-(aq),加水稀釋,平衡正向移動,[CuCl2]-轉(zhuǎn)化為CuCl沉淀;
CuCl(s)+Cl-(aq),加水稀釋,平衡正向移動,[CuCl2]-轉(zhuǎn)化為CuCl沉淀;
(4)析出的CuCl晶體不用水而用鹽酸、乙醇洗滌,是因為用鹽酸洗滌可以減小溶解導致的損失;用乙醇洗滌是利用乙醇容易揮發(fā)的特性,可以使晶體迅速干燥,避免CuCl被氧化;
(5)硫酸鈰是強酸弱堿鹽,水解使溶液顯酸性,所以應該盛放在酸式滴定管中;
根據(jù)反應前后電子轉(zhuǎn)移數(shù)目相等,可得關(guān)系式:CuCl~FeCl2~Ce(SO4)2,n(CuCl)=n[Ce(SO4)2]= 0.10 mol/L×0.0245L=0.00245mol,m(CuCl)= 0.00245mol×99.5g/mol=0.244g,所以產(chǎn)品中氯化亞銅的質(zhì)量分數(shù)為(0.244g÷0.25 g) ×100%=97.51%。


 備戰(zhàn)中考寒假系列答案
備戰(zhàn)中考寒假系列答案科目:高中化學 來源: 題型:
【題目】氟磺胺草醚(結(jié)構(gòu)式為 ,化學式為C13H10ClF3N2O6S)為高效豆田芽后除草劑,在雜草萌生后施藥可有效防除一年生闊葉雜草。其合成方法如圖:
,化學式為C13H10ClF3N2O6S)為高效豆田芽后除草劑,在雜草萌生后施藥可有效防除一年生闊葉雜草。其合成方法如圖:
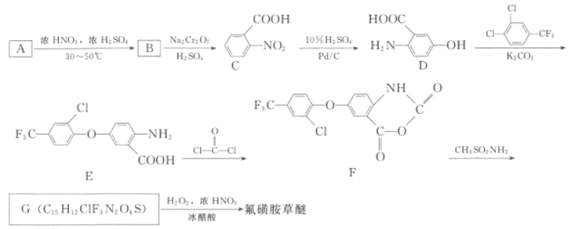
回答下列問題:
(1)已知A的分子式為C7H8,則其結(jié)構(gòu)簡式為_______________。
(2)寫出從A→B反應的化學方程式:______________________。與B具有相同官能團的B的同分異構(gòu)體有___________個,其中核磁共振氫譜吸收峰面積比值為2:2:2:1的是___________(寫結(jié)構(gòu)簡式)
(3)上述反應中,B→C屬于___________反應,E→F屬于___________反應。
(4)G的結(jié)構(gòu)簡式為___________。
(5)仿照題給價息,寫出以 和
和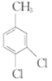 為原料合成
為原料合成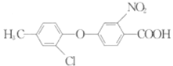 的流程圖(其他無機試劑自選)。_________________
的流程圖(其他無機試劑自選)。_________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列各組離子一定能在指定溶液中大量共存的是( )
A. 使酚酞變紅色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B. ![]() 的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C. ![]() 的溶液:NH4+、Cu2+、NO3-、Cl-
的溶液:NH4+、Cu2+、NO3-、Cl-
D. 水電離的c(H+)=1×10﹣13 mol·L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關(guān)系式錯誤的是( )
A. CO2的水溶液:c(H+)>c(HCO3-)>2c(CO32-)
B. 等濃度的HCN溶液與NaOH溶液等體積混合,所得溶液pH>7,則溶液中離子濃度:c(Na+)>c(CN-) >c(OH-)>c(H+)
C. NaHCO3溶液中存在水解平衡:HCO3-+H2OH2CO3+OH-
D. 兩種弱酸HX和HY混合后,溶液中的c(H+)為(Ka為電離平衡常數(shù)) ![]() +
+![]() + c(OH-)
+ c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含氮、磷化合物在生活和生產(chǎn)中有許多重要用途,如:(CH3)3N、磷化硼(BP)、磷青銅(Cu3SnP)等。
回答下列問題:
(1)錫(Sn)是第五周期ⅣA元素。基態(tài)錫原子的價電子排布式為_________,據(jù)此推測,錫的最高正價是_________ 。
(2)與P同周期的主族元素中,電負性比P小的元素有____種,第一電離能比P大有____種。
(3)PH3分子的空間構(gòu)型為___________。PH3的鍵角小于NH3的原因是__________。
(4)化合物(CH3)3N能溶于水,試解析其原因____________。

(5)磷化硼是一種耐磨涂料,它可用作金屬的表面保護層。磷化硼晶體晶胞如圖所示:
①在一個晶胞中磷原子空間堆積方式為________,磷原子的配位數(shù)為________。
②已知晶胞邊長a pm,阿伏加德羅常數(shù)為NA。則磷化硼晶體的密度為______ g/cm3。
③磷化硼晶胞沿著體對角線方向的投影如圖,請將表示B原子的圓圈涂黑________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質(zhì)的保存方法,與其化學性質(zhì)無關(guān)的是( )
A.金屬鈉保存在煤油中
B.濃鹽酸需密閉保存
C.新制氯水密閉存放于棕色瓶中
D.過氧化鈉需保持干燥密閉保存
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】汽車尾氣中CO、NO2在一定條件下可以發(fā)生反應:4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g)ΔH=-1 200 kJ·mol-1。在一定溫度下,向容積固定為2 L的密閉容器中充入一定量的CO和NO2,NO2的物質(zhì)的量濃度隨時間的變化曲線如圖所示:
4CO2(g)+N2(g)ΔH=-1 200 kJ·mol-1。在一定溫度下,向容積固定為2 L的密閉容器中充入一定量的CO和NO2,NO2的物質(zhì)的量濃度隨時間的變化曲線如圖所示:

(1)0~10 min內(nèi)該反應的平均速率v(CO)=________,從11 min起其他條件不變,壓縮容器的容積變?yōu)? L,則c(NO2)的變化曲線可能為圖中的________(填字母)。
(2)恒溫恒容條件下,不能說明該反應已達到平衡狀態(tài)的是________(填字母)。
A.容器內(nèi)混合氣體顏色不再變化
B.容器內(nèi)的壓強保持不變
C.2v逆(NO2)=v正(N2)
D.容器內(nèi)混合氣體密度保持不變
(3)寫出該反應平衡常數(shù)表達式:______,增大壓強平衡______(填“正向”“不”“逆向”)移動,平衡常數(shù)______(填“增大”“減小”“不變”)。
(4)對于該反應,溫度不同(T2>T1)、其他條件相同時,下列圖像表示正確的是_______(填序號)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究表明N2O與CO在Fe+作用下發(fā)生反應的能量變化及反應歷程如下圖所示,下列說法錯誤的是

A. 反應總過程ΔH<0
B. Fe+使反應的活化能減小
C. FeO+也是該反應的催化劑
D. Fe++N2O![]() FeO++N2、FeO++CO
FeO++N2、FeO++CO![]() Fe++CO2兩步反應均為放熱反應
Fe++CO2兩步反應均為放熱反應
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com