為了合理利用化學能,確保安全生產,化工設計需要充分考慮化學反應的焓變,并采取相應措施.化學反應的焓變通常用實驗進行測定,也可進行理論推算.
(1)實驗測得,1g甲醇在氧氣中充分燃燒生成二氧化碳和液態水釋放出22.7kJ的熱量,試寫出甲醇燃燒的熱化學方程式:
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)?H=-1452.8 kJ?mol-1
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)?H=-1452.8 kJ?mol-1
(2)自發現富勒烯C
60以來,其神奇的結構和性能引起了人們對碳原子團簇廣泛和深入的研究.C
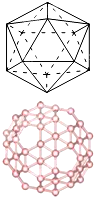
60分子是形如球狀的多面體,該結構的建立基于以下考慮:削去右圖多面體(含12個頂點,20個正三角形)的每一個頂角,得到由一定數目的正五邊形和正六邊形所組成的多面體,即為C
60分子,該多面體中含有90條棱,且每個碳原子都達到了8電子的穩定結構.已知幾種共價鍵的鍵能數據如下表:
利用下表數據估算得C
60分子的燃燒熱為
(120d-60a-30b-60e) kJ?mol-1
(120d-60a-30b-60e) kJ?mol-1
.
| 化學鍵 |
C-C |
C=C |
C≡C |
C=O |
O=O |
| 鍵能/(kJ?mol-1) |
a |
b |
c |
d |
e |
(3)最近美國Rice University的教授Boris Yakobson與其同事預測了一種硼巴基球(B
n,如圖所示)的存在,這種分子組成與C
60相似,但在它每個六邊形的中心有一個額外的原子,顯著提高了其穩定性.則n=
80
80
.

 為了合理利用化學能,確保安全生產,化工設計需要充分考慮化學反應的焓變,并采取相應措施.化學反應的焓變通常用實驗進行測定,也可進行理論推算.
為了合理利用化學能,確保安全生產,化工設計需要充分考慮化學反應的焓變,并采取相應措施.化學反應的焓變通常用實驗進行測定,也可進行理論推算.
