
下圖是某研究性學習小組設計的對一種廢舊合金各成分(含有Cu、Fe、Si 三種成分)進行分離、回收再利用的工業流程,通過該流程能得到常用的單質、聚鐵(堿式硫酸鐵的聚合物)、鐵紅(Fe2O3)和綠礬(FeSO4·7H2O)。
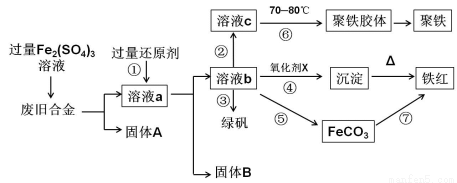
(1)加入過量Fe2(SO4)3溶液過程中與較活潑的金屬反應的離子方程式: 。
(2)①中過量的還原劑應是 ,固體B是 。
(3)向溶液b中加入酸性KMnO4溶液發生反應的離子方程式為
(4)②中加入H2O2,并調節pH值得到溶液c,在⑥中,將溶液c控制到70~80 ℃的目的是 。
(5)在③中,蒸發濃縮需要的硅酸鹽儀器除酒精燈外,還有 。
(6)在④中的氧化劑X是 。
(7)在⑤中,向溶液b加入了NH4HCO3溶液,得到FeCO3沉淀,寫出其離子反應方程式: 。
(8)在⑦中,寫出FeCO3煅燒的化學反應方程式: 。
科目:高中化學 來源:2016-2017學年浙江省高二上期中化學試卷(解析版) 題型:選擇題
工業上電解法處理含鎳酸性廢水并得到單質Ni的原理如圖所示。下列說法不正確的是( )

已知:①Ni2+在弱酸性溶液中發生水解
②氧化性:Ni2+(高濃度)>H+>Ni2+(低濃度)
A.碳棒上發生的電極反應:4OH— -4e—==O2↑+2H2O
B.電解過程中,B中NaCl溶液的物質的量濃度將不斷減少
C.為了提高Ni的產率,電解過程中需要控制廢水pH
D.若將圖中陽離子膜去掉,將A、B兩室合并,則電解反應總方程式發生改變
查看答案和解析>>
科目:高中化學 來源:2017屆重慶市西北狼教育聯盟高三12月月考化學試卷(解析版) 題型:選擇題
四種短周期元素W、R、P、Q的原子序數依次增大,W的一種核素沒有中子,R、Q同主族,R元素原子的最外層電子數是內層電子數的3倍,P元素與R元素形成的常見化合物中既含離子鍵又含非極性共價鍵。下列說法不正確的是( )
A. Q元素形成的酸一定是強酸
B. P與R形成化合物中,陰、陽離子個數比一定為1:2
C. 原子半徑:W<R<Q<P
D. 沸點:W2R>W2Q
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省淮安市高三12月考試化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.化學反應的焓變與反應的途 徑有關
徑有關
B.室溫下,稀釋0.1mol·L-1CH3COOH溶液,溶液的導電能力減弱
C.常溫常壓下,22.4L Cl2中含有的分子數為6.02×1023個
D.等質量的銅按a、b兩種途徑完全轉化為Cu(NO3)2,途徑a、b消耗的硝酸一樣多
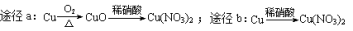
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省淮安市高三12月考試化學試卷(解析版) 題型:選擇題
下列有關化學用語表示正確的是
A.對硝基甲苯的結構簡式: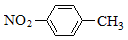
B.CH2F2的電子式: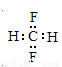
C.HClO的結構式:H -O-Cl
-O-Cl
D.CO2的比例模型:
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省七校聯合體高三上學期第二次聯考化學試卷(解析版) 題型:選擇題
下列實驗操作、現象與所得結論一致的是
實驗操作 | 現象 | 結論 | |
A | 向盛有25mL 沸水的燒杯中滴入5~6滴FeCl3飽和溶液,繼續煮沸。 | 溶液生成紅褐色沉淀 | 制得Fe(OH)3膠體 |
B | 向兩支盛有KI3溶液的試管中,分別滴加淀粉溶液和AgNO3溶液。 | 前者溶液變藍,后者有黃色沉淀。 | KI3溶液中存在平衡:I3- |
C | 將溴乙烷和NaOH乙醇溶液混合加熱,產生氣體通入酸性KMnO4溶液中。 | 酸性KMnO4溶液褪色。 | 一定產生了乙烯。 |
D | 在滴有酚酞的Na2CO3溶液中,加入CaCl2溶液。 | 溶液褪色。 | CaCl2溶液有酸性。 |
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省高三上12月月考化學卷(解析版) 題型:實驗題
直接氧化法制備混凝劑聚合硫酸鐵[Fe2(OH)n(SO4)3-n/2]m (n>2,m≤10)的實驗流程如下:

已知:鹽基度=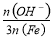 ×100%.式中n(OH-)、n(Fe)分別表示PFS中OH-和Fe3+的物質的量.所得產
×100%.式中n(OH-)、n(Fe)分別表示PFS中OH-和Fe3+的物質的量.所得產 品若要用于飲用水處理,需達到鹽基度指標為 8.0%~16.0%.
品若要用于飲用水處理,需達到鹽基度指標為 8.0%~16.0%.
(1)實驗加入硫酸的作用是____________,取樣分析Fe2+濃度,其目的是___________。
(2)用pH試紙測定溶液pH的操作方法為____________,若溶液的pH偏小,將導致聚合硫酸鐵中鐵的質量分數____________(填“偏高”、“偏低”、“無影響”)
(3)聚合反應的原理為m[Fe2(OH)n(SO4) 3-n/2]?[Fe2(OH)n(SO4)3-n/2]m,則水解反應的化學方程式為____________.
(4)產品鹽基度的測定方法:
Ⅰ稱取m g固體試樣,置于400mL聚乙烯燒杯中,加入25mL鹽酸標準溶液,再加20mL煮沸后冷卻的蒸餾水,搖勻,蓋上表面皿.
Ⅱ室溫下放置10min,再加入10mL氟化鉀溶液,搖勻,掩蔽Fe3+,形成白色沉淀.
Ⅲ加入5滴酚酞指示劑,立即用物質的量濃度為c mol•L-1的氫氧化鈉標準液滴定至終點,消耗體積為VmL.
Ⅳ向聚乙烯燒杯中,加入25mL鹽酸標準溶液,再加20mL煮沸后冷卻的蒸餾水,搖勻,蓋上表面皿.然后重復Ⅱ、Ⅲ做空白試驗,消耗氫氧化鈉標準液的體積為V0mL.
①達到滴定終點的現象為____________。
②已知試樣中Fe3+的質量分數為a,則該試樣的鹽基度的計算表達式為________。
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省高三上12月月考化學卷(解析版) 題型:選擇題
我國晉代《抱樸子》中描述了大量的化學反應,其中有:①“丹砂(HgS)燒之成水銀,積變又還成丹砂”; ②“以曾青涂鐵,鐵赤色如銅”。下列有關敘述正確的是
A.①中水銀“積變又還成丹砂”說明水銀發生了還原反應
B.②中反應的離子方程式為:2Fe+3Cu2+=2Fe3++3Cu
C.根據①可知溫度計打破后可以用硫粉覆蓋水銀,防止中毒
D.水銀能跟曾青發生置換反應生成單質銅
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上五調考試化學卷(解析版) 題型:選擇題
A、B、C、D、E是原子序數依次增大的五種短周期元素且B、C相鄰,A元索可以與B、C、E元素分別形成甲、乙、丙三種物質且甲、乙均為10電子化合物,丙為18電子化合物。D元索的最外層電子數與核外電子層數相等。已知:甲+E2=丙+ Br2,甲+丙=丁,下列說法中正確的是( )
A. 離子半徑:D>C>B
B. A與B兩種元素共同形成的10電子粒子有3種
C. D元素在周期表中的位置是第二周期第ⅡA族
D. 丁物質均由非金屬元索構成,只含共價鍵
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com