
【題目】I已知:還原性HSO![]() >I-,氧化性IO
>I-,氧化性IO![]() > I2 。
> I2 。
(1)在NaIO3溶液中滴加少量NaHSO3溶液,發生下列反應。配平反應方程式并用單線橋標出電子轉移的方向和數目_______。
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
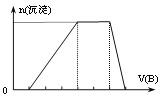
(2)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物質的量和析出I2單質的物質的量的關系曲線如圖所示。寫出反應過程中與AB段曲線對應的離子方程式_______;當溶液中I-與I2的物質的量之比為5:3時,加入的NaIO3為_______mol。

II 已知:KClO3可以和草酸(H2C2O4)、硫酸反應生成高效的消毒殺菌劑ClO2,還生成CO2、KHSO4等物質。寫出該反應的化學方程式________________。
【答案】 IO
IO![]() +5I-+6H+=3I2+3H2O
+5I-+6H+=3I2+3H2O ![]() 2KClO3+H2C2O4+2H2SO4=2KHSO4+2CO2↑+2ClO2↑+2H2O
2KClO3+H2C2O4+2H2SO4=2KHSO4+2CO2↑+2ClO2↑+2H2O
【解析】
根據還原性HSO3->I-,氧化性IO3->I2來判斷反應的產物,利用得失電子相等配平方程式,并利用化合價來分析轉移的電子數;根據圖象及物質的量的關系來分析反應的過程,寫出AB段的離子方程式,根據n(I-):n(I2)=5:3,由OA、AB二段離子方程式計算加入NaIO3的量;根據題給的反應物和生成物,由得失電子守恒和質量守恒書寫化學方程式。
I:(1)反應中碘元素由+5價降低為0價,硫元素由+4價升高為+6價,要使得失電子守恒,NaIO3系數為4,NaHSO3系數為10,依據原子個數守恒該反應的方程式為:4NaIO3 +10NaHSO3 =7Na2SO4 +3H2SO4 +2I2+2H2O,用單線橋表示為: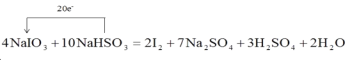 ,答案為
,答案為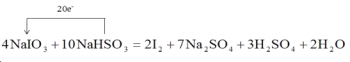 。
。
(2)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液,由圖可知,OA段,無I2生成,IO3-根的碘元素得電子,全部轉化為I-,NaHSO3中硫元素失電子,全部由+4價變為+6價,且從圖象可知IO3-與HSO3-的物質的量之比為n(IO3-):n(HSO3-)=1:3,離子方程式為IO3-+3HSO3-═3SO42-+I-+3H+,AB段,發生I-和IO3-反應,生成I2,離子方程式為IO3-+5I-+6H+═3H2O+3I2,當溶液中I-與I2的物質的量之比為5:3時,設I-與I2的物質的量分別為5n、3n,根據AB段反應 則產生I-總的物質的量為(5n+5n)mol=10nmol,根據OA段反應
則產生I-總的物質的量為(5n+5n)mol=10nmol,根據OA段反應 , 10nmolIO3-與5molHSO3-反應,由電子守恒可知,10n×6=5mol×2,解得n=
, 10nmolIO3-與5molHSO3-反應,由電子守恒可知,10n×6=5mol×2,解得n= ![]() mol,加入的NaIO3為(10n+n)mol=11nmol=11×
mol,加入的NaIO3為(10n+n)mol=11nmol=11×![]() mol=
mol=![]() mol;答案為IO3-+5I-+6H+═3H2O+3I2,
mol;答案為IO3-+5I-+6H+═3H2O+3I2,![]() 。
。
II:由KClO3和草酸(H2C2O4)在酸性條件下反應生成ClO2、CO2和KHSO4可知,KClO3中氯元素由+5價得電子變成+4價,草酸(H/span>2C2O4)中碳元素由+3價失電子變成+4價,由電子得失守恒和題中的反應物和生成物,反應的方程式為:2KClO3+H2C2O4+2H2SO4═2ClO2↑+2CO2↑+2KHSO4+2H2O;答案為2KClO3+H2C2O4+2H2SO4═2ClO2↑+2CO2↑+2KHSO4+2H2O。


科目:高中化學 來源: 題型:
【題目】下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6種元素的代號,其中J為0族元素。
X | Y | Z | |
R | |||
W | |||
J |
下列說法正確的是( )
A.R原子的核外電子排布圖為![]()
B.Y2-與Na+的半徑大小關系為Y2->Na+
C.X的第一電離能小于Y的第一電離能
D.表中電負性最大的元素為W
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D為前四周期元素.A元素的原子價電子排布為![]() ,B元素的最外層電子數是其電子層數的3倍,C元素原子的M電子層的P軌道中有3個未成對電子,D元素原子核外的M層中只有2對成對電子。
,B元素的最外層電子數是其電子層數的3倍,C元素原子的M電子層的P軌道中有3個未成對電子,D元素原子核外的M層中只有2對成對電子。
![]() 當
當![]() 時,
時,![]() 屬于 ______ 分子
屬于 ______ 分子![]() 填“極性”或“非極性”
填“極性”或“非極性”![]() .
.
![]() 當
當![]() 時,A與B形成的晶體屬于 ______ 晶體.
時,A與B形成的晶體屬于 ______ 晶體.
![]() 若A元素的原子價電子排布為
若A元素的原子價電子排布為![]() ,A、C、D三種元素的第一電離能由大到小的順序是 ______
,A、C、D三種元素的第一電離能由大到小的順序是 ______ ![]() 用元素符號表示
用元素符號表示![]() 。
。
![]() 已知某紅紫色配合物的組成為
已知某紅紫色配合物的組成為![]() 該配合物中的中心離子鈷離子在基態時核外電子排布式為 ______ ,又已知中心離子鈷離子的配位數是6,1mol該物質與足量的硝酸銀反應可生成3molAgCl,則該物質化學式是 ______ 。
該配合物中的中心離子鈷離子在基態時核外電子排布式為 ______ ,又已知中心離子鈷離子的配位數是6,1mol該物質與足量的硝酸銀反應可生成3molAgCl,則該物質化學式是 ______ 。
![]() 金屬鐵的晶體在不同溫度下有兩種堆積方式,晶胞分別如圖所示.體心立方晶胞和面心立方晶胞中實際含有的Fe原子個數之比為 ______ 。
金屬鐵的晶體在不同溫度下有兩種堆積方式,晶胞分別如圖所示.體心立方晶胞和面心立方晶胞中實際含有的Fe原子個數之比為 ______ 。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)某第三周期金屬元素R的部分電離能情況如圖Ⅰ所示,則R元素位于正確表第____族,其基態原子第二能層電子排布圖為_____________________。
圖Ⅱ中 A、B、C、D是四種不同主族元素的氣態氫化物,其中A比B分子沸點高的可能原因是_________。

圖Ⅱ中C物質能與第二周期中的另一種元素的氫化物通過配位鍵相互作用得到化合物X,X是一種儲氫材料,且X是乙烷的等電子體,加熱X會緩慢釋放H2同時生成化合物Y,Y又是乙烯的等電子體,則化合物C的VSEPR模型是__________,X的結構式為__________(標明配位鍵)。
(2)已知Ti3+可形成配位數為6的配合物。
現有鈦的兩種配合物,組成皆為TiCl3·6H2O,一種為紫色,另一種為綠色,現取等質量的兩種物質的樣品配成待測溶液,分別往待測溶液中滴入AgNO3溶液充分反應,產生白色沉淀;測得綠色物質得到的沉淀質量是紫色物質得到的沉淀質量的2/3。則原綠色配合物的化學式為_____________,原紫色配合物的化學式為_____________。
(3)由某原子構成的晶胞,己知晶胞密度為ρg/cm3,邊長為anm。若該原子半徑為(![]() )anm,則該晶胞類型為______________;該原子的摩爾質量表達式為______________。
)anm,則該晶胞類型為______________;該原子的摩爾質量表達式為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】普通干電池,是一種廣泛使用的可移動化學電源,其結構如圖甲所示,電池反應是:![]() 但這種一次性電池使用后的隨意丟棄,已經是不可忽視的環境問題.某中學的課外活動小組在老師指導下,用廢棄的電池進行處理回收.將電池剝離,得到石墨棒,清洗后作電化學實驗的電極.廢鋅皮和炭黑與錳的氧化物做以下處理
但這種一次性電池使用后的隨意丟棄,已經是不可忽視的環境問題.某中學的課外活動小組在老師指導下,用廢棄的電池進行處理回收.將電池剝離,得到石墨棒,清洗后作電化學實驗的電極.廢鋅皮和炭黑與錳的氧化物做以下處理
實驗一、用廢鋅制取防腐劑皓礬![]() 圖乙
圖乙![]()

![]() 操作一的名稱是:______。
操作一的名稱是:______。
![]() 鋅的化學性質與鋁相似,也可以與強堿反應而溶解,但生成的是配合物
鋅的化學性質與鋁相似,也可以與強堿反應而溶解,但生成的是配合物![]() 四羥基鋅酸鈉
四羥基鋅酸鈉![]() 和
和![]() ,該配合物中心離子是______,配位數是 ______。
,該配合物中心離子是______,配位數是 ______。
實驗二、經查相關資料:錳的氧化物都不溶于水,且都能與濃鹽酸反應生成氯氣.將分離得到的黑色粉末在空氣中充分灼燒,并做相關實驗,回答下列問題:
![]() 灼燒的目的是: ______ ,將灼燒后的固體冷卻,溶解、過濾、干燥得到的固體物質混合物
灼燒的目的是: ______ ,將灼燒后的固體冷卻,溶解、過濾、干燥得到的固體物質混合物![]() 和
和![]() 。
。
![]() 寫出
寫出![]() 與濃鹽酸反應的離子方程式: ______ 。
與濃鹽酸反應的離子方程式: ______ 。
![]() 取
取![]() 上述混合物,與足量的濃鹽酸充分反應,得到標況下的氯氣
上述混合物,與足量的濃鹽酸充分反應,得到標況下的氯氣![]() ,則混合物中
,則混合物中![]() 和
和![]() 質量之比是: ______ 。
質量之比是: ______ 。
實驗三、查詢資料得知,還可以通過電解的方式,將![]() 轉化為
轉化為![]() ,同學們設計了這樣的一個裝置
,同學們設計了這樣的一個裝置![]() 圖丙
圖丙![]() ,將混合物粉末調成糊狀,附在其中的 ______ 邊電極上
,將混合物粉末調成糊狀,附在其中的 ______ 邊電極上![]() 填左或者右
填左或者右![]() ,該電極上發生的電極反應式是: ______
,該電極上發生的電極反應式是: ______ ![]() 在電解過程中溶液的pH將 ______填變大、變小、不變
在電解過程中溶液的pH將 ______填變大、變小、不變![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外小組對金屬鈉進行研究。已知C、D都是單質,F的水溶液是一種常見的強酸。

(1)金屬Na在空氣中放置足夠長時間,最終的生成物是:_________________________。
(2)若A是一種常見金屬單質,且A與B溶液能夠反應,則將過量的F溶液逐滴加入E溶液,邊加邊振蕩,所看到的實驗現象是_________________________。
(3)若A是一種不穩定的鹽,A溶液與B溶液混合將產生白色絮狀沉淀且瞬間變為灰綠色,最后變成紅褐色的E,請寫出該過程中發生氧化還原反應的化學方程式:_________________________。
(4)若A是一種溶液,只可能含有H+、NH![]() 、Mg2+、Fe3+、Al3+、CO
、Mg2+、Fe3+、Al3+、CO![]() 、SO
、SO![]() 中的某些離子,當向該溶液中加入B溶液時發現生成沉淀的物質的量隨B溶液的體積發生變化如圖所示,由此可知,該溶液中肯定含有的離子及其物質的量濃度之比為_________。
中的某些離子,當向該溶液中加入B溶液時發現生成沉淀的物質的量隨B溶液的體積發生變化如圖所示,由此可知,該溶液中肯定含有的離子及其物質的量濃度之比為_________。
(5)將NaHCO3與M的混合物在密閉容器中充分加熱后排出氣體,經測定,所得固體為純凈物,則NaHCO3與M的質量比為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應:2A(g)+3B(g)![]() C(g)+4D(g),速率最快的是( )
C(g)+4D(g),速率最快的是( )
A. v(C)=0.1mol·L-1·s-1 B. v(B)=4.0 mol·L-1·min-1
C. v(A)=2.0mol·L-1·min-1 D. v(D)=0.3mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知CH4(g)+2O2(g)→CO2(g)+2H2O(g) ΔH== - Q1 ;
2H2(g)+O2(g) →2H2O(g) ΔH== - Q2;
H2O(g) →H2O(l) ΔH== - Q3
常溫下,取體積比為4:1的甲烷和H2的混合氣體112L(標準狀況下),經完全燃燒后恢復到常溫,則放出的熱量為
A.4Q1+0.5Q2B.4Q1+Q2+10Q3C.4Q1+2Q2D.4Q1+0.5Q2+9Q3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵的某種氧化物20 g,在加熱的條件下通入足量的CO完全反應,將生成的氣體用石灰水吸收,得到沉淀37.5 g,求該氧化物中鐵元素與氧元素的質量比。_________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com