
分析 根據n=$\frac{m}{M}$計算Na2SO4的物質的量,由化學式可知,鈉離子物質的量為硫酸鈉物質的量的2倍,硫酸根物質的量等于硫酸鈉的物質的量計算.
解答 解:14.2g Na2SO4的物質的量為$\frac{14.2g}{142g/mol}$=0.1mol,
所含的Na+的物質的量是0.1mol×2=0.2mol,其數目為0.2NA,
所含SO42-的物質的量等于硫酸鈉的物質的量是0.1mol,其質量為m=nM=0.1mol×96g/mol=9.6g;
答:含有Na+的數目是0.2NA;含有SO4-的質量是9.6g.
點評 本題考查物質的量有關計算,比較基礎,注意根據化學式判斷含有微粒與物質的物質的量關系.


 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源: 題型:解答題
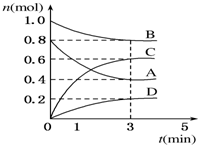 T℃時,在容積為0.5L的密閉容器中發生如 下反應.mA(g)+nB(g)?pC(g)+qD(s)△H<0(m、n、p、q為最簡整數比).A、B、C、D的物質的量變化如圖所示.
T℃時,在容積為0.5L的密閉容器中發生如 下反應.mA(g)+nB(g)?pC(g)+qD(s)△H<0(m、n、p、q為最簡整數比).A、B、C、D的物質的量變化如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含金屬元素的離子不一定是陽離子 | |
| B. | 金屬與鹽溶液反應都是置換反應 | |
| C. | 玻璃是氧化物,成分可表示成Na2O.CaO.6SiO2 | |
| D. | 與強酸、強堿都反應的物質只有兩性氧化物和兩性氫氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 已知:Fe(OH)3和Al(OH)3沉淀的生成與溶解的pH如表:
已知:Fe(OH)3和Al(OH)3沉淀的生成與溶解的pH如表:| 氫氧化物 | 溶液pH | |||
| 開始沉淀 | 沉淀完全 | 沉淀開始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | - | - |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| A. | AB段可能發生的反應是:2SO42-+2Ba2++Al3++30H-=2BaSO4↓+Al(OH)3↓ | |
| B. | C點對應的沉淀是:Fe(OH)3和BaSO4 | |
| C. | OA段可能發生的反應是:3Ba2++6OH-+3SO42-+Al3++Fe3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓ | |
| D. | 據圖計算原溶液中:c(Cl-)=c(SO42-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com