
【題目】用5 mol/L 的HNO3溶液配制500 mL 1 mol/L的HNO3溶液時,不需用到的儀器是
A. 分液漏斗B. 膠頭滴管C. 燒杯D. 500 mL容量瓶
 同步練習強化拓展系列答案
同步練習強化拓展系列答案科目:高中化學 來源: 題型:
【題目】織物漂白劑亞氯酸鈉(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒氣體。25℃時,各組分濃度隨pH變化情況如圖所示(Cl-沒有畫出)。下列說法不正確的是( )
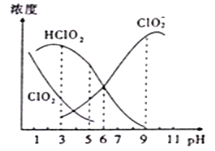
A.25℃時, ClO2-的水解平衡常數Ka=10-6
B.在pH約為4.0~4.5范圍內使用該漂白劑較好
C.25℃時,等濃度的HClO2溶液和NaClO2溶液等體積混合后,混合溶液中:
c(HClO2)+c(H+)+c(Na+)=c(ClO2-)+2c(OH-)
D.當pH=5時往NaClO2溶液中滴入稀氫氧化鈉溶液,溶液中主要反應的離子方程式是:HClO2+OH-=H2O+ClO2-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素X的某價態離子Xn+中所有電子正好充滿K、L、M三個電子層,它與N3-形成的晶體結構如下圖所示。下列說法錯誤的是

A. X元素的原子序數是19
B. Xn+中n=1
C. 該晶體中陽離子與陰離子個數比為3∶1
D. 晶體中每個N3-周圍有6個等距離且最近的Xn+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】MnO2是常見的氧化劑、催化劑和活性電極材料。
(1)工業上,以惰性材料為電極,電解MnSO4溶液(含少量稀硫酸)制備MnO2。寫出陽極的電極反應式:___________。
(2)已知如下熱化學方程式(K代表平衡常數):
①MnCO3(s)![]() MnO(s)+CO2(g) △H1 K1
MnO(s)+CO2(g) △H1 K1
②2MnO(s)+O2(g)![]() 2MnO2(s) △H2 K2
2MnO2(s) △H2 K2
③2MnCO3(s)+O2(g)![]() 2MnO2(s)+2CO2(g) △H3 K3
2MnO2(s)+2CO2(g) △H3 K3
△H3=______(用△H1、△H2表示) K3=_______(用K1、K2表示)。
(3)反應②在低溫條件下能自發進行,則△H2______0(填“>”“<”或“=”)。
(4)在密閉容器中投入足量的MnCO3,—定條件下發生反應:MnCO3(s)![]() MnO(s)+CO2(g)
MnO(s)+CO2(g)
△H>0。在一定溫度下,達到平衡狀態時p(CO2)=2a MPa。

① 溫度、壓強對MnCO3分解率的影響如圖所示:比較:L1____L2(填“>”“<”或“=”)。
② 保持溫度不變,將容器體積擴大至原來的2倍,則p(CO2)的變化范圍是______。
③ 保持溫度不變,將容器體積壓縮至原來的一半,達到新平衡時下列物理量-定不變的是__(填代號)。
A.平衡常數K B.c(CO2) C.n(CO2) D.m(MnCO3)
(5)—定溫度下,在容積為2L的恒容密閉容器中加人足量的MnCO3(s)和5molO2,發生反應:2MnCO(s)+O2(g)![]() 2MnO2(s)+2CO2(g),CO2以平均速率0.1mol L-1·min-1經過10min達到平衡狀態。該條件下該反應的平衡常數K為_______。
2MnO2(s)+2CO2(g),CO2以平均速率0.1mol L-1·min-1經過10min達到平衡狀態。該條件下該反應的平衡常數K為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】尿素/H2O2溶液可用于煙氣的脫硫脫硝。
(1)已知T℃時,2SO2(g)+O2(g) ![]() 2SO3(g) △H1
2SO3(g) △H1
2H2O2(I)=2H2O(I)+O2(g) △H2
SO3(g)+H2O(I))=H2SO4(I) △H3
則SO2(g)+H2O2(I))=H2SO4(I) △H4=__________ (用含△H1、△H2、△H3的代數式表示)
(2)尿素[CO(NH2)2]溶液對NOx及SO2有一定的脫除率。將SO2和NOx (N〇約占90%)通入氧氣的體積分數為7%、尿素濃度為5%的反應器中進行反應。
①煙氣中SO2最終轉化為一種正鹽,其化學式為______________;NO和NO2以物質的量之比1:1與CO(NH2)2反應生成無毒氣體的化學方程式為_________________________。
②氨基甲酸銨(H2NCOONH4)是尿素的水解產物,將一定量的氨基甲酸銨置于恒容密閉容器中,發生反應:NH2COONH4(s)![]() 2NH3(g)+CO2(g) △H,實驗測得不同溫度下平衡時氣體的總濃度如下表:
2NH3(g)+CO2(g) △H,實驗測得不同溫度下平衡時氣體的總濃度如下表:
溫度/K | 338 | 343 | 348 | 353 |
平衡時氣體的總濃度/mol L-1 | 0.36 | 0.48 | 0.60 | 0.72 |
該反應的△H__________(填“>”或“<”)0;348K時,該反應的平衡常數K__________________。
(3)其他條件不變,向尿素溶液中添加H2O2溶液,測得不同 pH下氮氧化物的脫除率與時間的關系如圖
所示。

①NO與H2O2發生反應生成亞硝酸時,氧化劑與還原劑的物質的量之比為____________。
②脫硝時,最佳pH為_________;在堿性較強時,NOx脫除率降低,其原因是_____________________
(任寫一點)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一氧化碳是一種用途相當廣泛的化工基礎原料。
⑴. 利用下列反應可以將粗鎳轉化為純度達99.9%的高純鎳。
Ni(s)+4CO(g)![]() Ni(CO)4(g) 該反應的ΔH_______0(選填“>”或“=”或“<”)。
Ni(CO)4(g) 該反應的ΔH_______0(選填“>”或“=”或“<”)。
⑵. 在高溫下一氧化碳可將二氧化硫還原為單質硫。已知:
C(s)+O2(g)=CO2(g);ΔH1=-393.5 kJ·mol-1
CO2(g)+C(s)=2CO(g);ΔH2=+172.5 kJ·mol-1
S(s)+O2(g)=SO2(g);ΔH3=-296.0 kJ·mol-1
則2CO(g)+SO2(g)=S(s)+2CO2(g) ΔH4=________。
⑶. 工業上一般采用CO與H2反應合成可再生能源甲醇,反應如下:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
某溫度下,將2molCO和6molH2充入2L的密閉容器中,充分反應達到平衡后,測
得c(CO)=0.2mol·L-1,則CO的轉化率為___________。
合成氣經壓縮升溫后進入10m3甲醇合成塔,在催化劑作用下,通過反應進行甲醇合成,T1℃下此反應的平衡常數為160。此溫度下,在密閉容器中加入一定量CO和H2,反應到某時刻測得各組分的濃度如下:
物質 | H2 | CO | CH3OH |
濃度/(mol·L-1) | 0.2 | 0.1 | 0.4 |
比較此時正、逆反應速率的大小:v正_______v逆 (填“>”、“<”或“=”);若其他條件不變,在T2℃反應10min后達到平衡,c(H2)=0.4 mol·L-1,則該時間內反應速率:
v(CH3OH) =__________;
(4)金屬氧化物被一氧化碳還原生成金屬單質和二氧化碳。下圖是四種金屬氧化物被一氧化碳還原時lg[c(CO)/c(CO2)]與溫度(t)的關系曲線圖。800℃時,其中最易被還原的金屬氧化物是____(填化學式),該反應的平衡常數數值(K)等于____________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知mmol某氣體的質量為a g,則b g該氣體在標準狀況下的體積(L)為
A.22.4bm/a B. 22.4b/am C.22.4am/b D.22.4a/bm
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】自來水是用氯氣殺菌消毒的,不法商販用自來水冒充純凈水銷售,為辨別純凈水真偽,可用下列哪種試劑鑒別( )
A.硝酸銀溶液 B.氯化鐵溶液
C.酚酞試液 D.氫氧化鈉溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com