
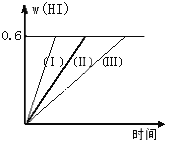
【題目】將1 mol I2(g)和2 mol H2置于2L密閉容器中,在一定溫度下發生反應:I2(g) + H2(g) ![]() 2HI(g);△H<0,并達平衡。HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示:
2HI(g);△H<0,并達平衡。HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示:
(1)達平衡時,I2(g)的物質的量濃度為____________________。
(2)若改變反應條件,在甲條件下w(HI)的變化如曲線(Ⅰ)所示,在乙條件下w(HI)的變化如曲線(Ⅲ) 所示。則甲條件可能是____________,則乙條件可能是_____________ 。(填入下列條件的序號)
①恒容條件下,升高溫度;②恒容條件下,降低溫度;③恒溫條件下,縮小反應容器體積;
④恒溫條件下,擴大反應容器體積;⑤恒溫恒容條件下,加入適當催化劑。
(3)若保持溫度不變,在另一個相同的2L密閉容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),發生反應,達平衡時,HI的體積分數仍為0.6,則a、b、c的關系是____________。
【答案】 0.05mol·L-1 ③⑤ ④ (a+c/2)/(b+c/2)=1/2
【解析】試題分析:(1)該反應是一個反應前后氣體體積不變的化學反應,所以反應后混合氣體的物質的量是3mol,同一容器中各種氣體的體積分數等其物質的量分數,所以平衡時碘化氫的物質的量=3mol×0.6=1.8mol,則參加反應的n(I2)=0.5n(HI)=0.5×1.8=0.9mol,剩余的n(H2)=1-0.9=0.1mol,所以平衡時c(H2)=![]() =0.05mol/L,故答案為:0.05mol/L;
=0.05mol/L,故答案為:0.05mol/L;
(2)在甲條件下w(HI)的變化如曲線(Ⅰ) 所示,反應時間縮短,碘化氫的含量不變,說明該條件只增大了反應速率不影響平衡,增大壓強(縮小反應容器體積)和加入催化劑對該反應平衡無影響,但都增大反應速率,縮短反應時間;在乙條件下w(HI)的變化如曲線(Ⅲ) 所示,反應時間變長,碘化氫的含量不變,說明反應速率減小,平衡不移動,所以是減小壓強(擴大容器體積),故答案為:③⑤;④;
(3)若保持溫度不變,在另一個相同的2L密閉容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),發生反應,達平衡時,HI的體積分數仍為0.6,與原來的平衡是等效平衡,恒溫恒容,前后氣體體積不變化,按化學計量數轉化到左邊,滿足與原來加入的反應物物質的量比例相等即可;
I2(g) + H2(g)![]() 2HI(g);
2HI(g);
開始(mol):a b c
變化(mol):0.5c 0.5c c
平衡(mol):a+0.5c b+0.5c 0
則(a+0.5c ):( b+0.5c)=1:2,所以4a+c=2b,故答案為:4a+c=2b。


 小天才課時作業系列答案
小天才課時作業系列答案 一課四練系列答案
一課四練系列答案 黃岡小狀元滿分沖刺微測驗系列答案
黃岡小狀元滿分沖刺微測驗系列答案 新輔教導學系列答案
新輔教導學系列答案 陽光同學一線名師全優好卷系列答案
陽光同學一線名師全優好卷系列答案科目:高中化學 來源: 題型:
【題目】向Fe 2 (SO 4 ) 3 和Al 2 (SO 4 ) 3 的混合溶液中,逐滴加入NaOH溶液至過量。下列圖象中,能正確表示上述反應的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2在O2中燃燒生成氣態H2O的反應是一個放熱反應,在反應過程中
A. 核能轉化成熱能 B. 化學能轉化成熱能
C. 生成物的總能量等于反應物的總能量 D. 生成物的總能量大于反應物的總能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知水的電離平衡曲線如圖所示,試回答下列問題:

(1)圖中五點kw間的關系是_____________。
(2)若從A點到D點,可采用的措施是 。
a.升溫 b.加入少量的鹽酸 c.加入少量的NH4Cl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關儀器的使用正確的是()
A. 手持試管給試管內的物質加熱
B. 用燃著的酒精燈去點燃另一盞酒精燈
C. 用天平稱量藥品時用手直接拿砝碼
D. 用滴管滴加液體時滴管應垂直懸垂在容器上方且不能觸及容器內壁
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作能達到實驗目的的是
A. 用排水法收集銅粉與濃硝酸反應產生的NO2
B. 用氨水鑒別NaCl、MgCl2、AlCl3、NH4Cl四種溶液
C. 用酸性KMnO4溶液驗證草酸的還原性
D. 用飽和NaHCO3溶液除去Cl2中混有的HCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知在1×105 Pa、298 K條件下,2 mol氫氣燃燒生成水蒸氣,放出484 kJ熱量,下列熱化學方程式正確的是( )
A. H2O(g)===H2(g)+![]() O2(g) ΔH=+242 kJ·mol-1
O2(g) ΔH=+242 kJ·mol-1
B. 2H2(g)+O2(g)===2H2O(l) ΔH=-484 kJ·mol-1
C. H2(g)+![]() O2(g)===H2O(g) ΔH=+242 kJ·mol-1
O2(g)===H2O(g) ΔH=+242 kJ·mol-1
D. 2H2(g)+O2(g)===2H2O(g) ΔH=+484 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】加壓降溫可以使空氣液化,在此過程中,下列說法正確的是
A.空氣中的分子質量變大 B.空氣中的分子間隔變小
C.空氣中的分子種類改變 D.空氣中的分子數目變少
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列能用勒沙特列原理解釋的是( )
A.Fe(SCN)3溶液中加入固體KSCN后顏色變深
B.棕紅色NO2加壓后顏色先變深后變淺
C.SO2催化氧化成SO3的反應,往往需要使用催化劑
D.H2、I2、HI平衡混和氣加壓后顏色變深
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com