
| ||
| ||


 陽光課堂課時作業系列答案
陽光課堂課時作業系列答案科目:高中化學 來源: 題型:閱讀理解
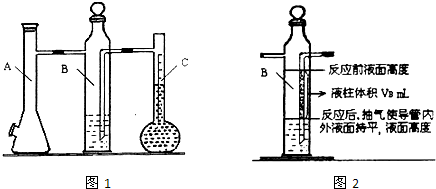
| 實驗次數 | m(Mg)/g | 硫酸體積/mL | 液體量瓶中液體體積/mL | 抽出氣體體積/mL | 氫氣體積/mL | 計算1mol氫體積/L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | X | |
| 2 | 0.115 | 10.0 | 121.0 | 8.0 |
| 實驗次數 | m(Mg) g |
硫酸體積mL | 液體量瓶中液體體積mL | 抽出氣體體積mL | B瓶的一段液柱體積mL | 水汽體積百分含量 | 計算1mol氫體積L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | VB | a% |
查看答案和解析>>
科目:高中化學 來源:江蘇省通州市石港中學2008屆高三化學科押寶卷 題型:058
某校興趣小組對氫氧化鈉溶液和稀鹽酸混合后的有關問題,進行了如下探究:
Ⅰ.(1)甲同學為了證明氫氧化鈉溶液與稀鹽酸能夠發生反應,設計并完成了如下圖所示實驗.
X溶液是________,滴入的量一般為________.

(2)乙同學也設計完成了另一個實驗,證明氫氧化鈉溶液與鹽酸能夠發生反應.在盛有氫氧化鈉溶液的試管中,用膠頭滴管慢慢滴入稀鹽酸,不斷振蕩溶液,同時測定溶液的pH,直至鹽酸過量.①寫出測定溶液pH的方法:_________________________.
②下圖中哪個圖像符合該同學的記錄________(填序號).

(3)你認為甲、乙兩位同學的實驗中,________(填“甲同學”、“乙同學”、“甲乙兩同學”)的實驗能充分證明氫氧化鈉溶液與鹽酸發生了反應,請說明理由:
____________________________________.
Ⅱ.丙同學利用“保溫瓶式量熱計”(圖略),測出10 mL 10% NaOH溶液和不同體積的10%鹽酸溶液混合過程中,溶液的溫度變化見下表(假設兩溶液密度相同).

就此實驗回答:
(1)鹽酸和氫氧化鈉的反應是________(填“吸熱”或“放熱”)反應.
(2)請在圖中繪制出溶液的溫度上升與加入鹽酸體積之間的變化關系圖,并在曲線上畫出能表示兩者之間恰好完全反應的點,并用字母P表示.

Ⅲ.丁同學為測定標示質量分數為32%的鹽酸的實際質量分數,用pH測定儀組成實驗裝置.實驗時先在燒杯中加入20 g 40%的氫氧化鈉溶液,再逐滴加入該鹽酸,測定儀打印出加入鹽酸的質量與燒杯中溶液的pH關系圖.

(1)請以此次測定的結果,列式計算該鹽酸的實際質量分數.
(2)請分析你的計算結果與標簽標示的質量分數不一致的可能原因.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com