
 H++Cl-+HClO。下列說法中正確的是( )
H++Cl-+HClO。下列說法中正確的是( )| A.光照一段時間后,c(HClO)減小 |
| B.加入碳酸鈣粉末后,溶液的pH增大,可以提高HClO濃度 |
| C.加入少量水,由水電離的c(H+)減小 |
D.加入少量NaOH固體,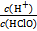 增大 增大 |
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:不詳 題型:填空題
 C(g)+D(g) ΔH<0。請回答下列問題:
C(g)+D(g) ΔH<0。請回答下列問題:查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題

| A.反應達到平衡時, X的轉化率為50% |
B.反應可表示為 |
| C.增大壓強可使平衡向生成Z的方向移動,平衡常數增大 |
| D.改變溫度可以改變此反應的平衡常數 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 pC(g)達到平衡時,測得c(A)為0.5 mol·L-1;在溫度不變的條件下,將容器體積擴大一倍,當達到平衡時,測得c(A)為0.3 mol·L-1。則下列判斷正確的是( )
pC(g)達到平衡時,測得c(A)為0.5 mol·L-1;在溫度不變的條件下,將容器體積擴大一倍,當達到平衡時,測得c(A)為0.3 mol·L-1。則下列判斷正確的是( )查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 N2O4(g) ΔH<0現將一定量NO2和N2O4的混合氣體通入體積為1 L的恒溫密閉容器中,反應物濃度隨時間變化關系如圖。下列說法中正確的是( )
N2O4(g) ΔH<0現將一定量NO2和N2O4的混合氣體通入體積為1 L的恒溫密閉容器中,反應物濃度隨時間變化關系如圖。下列說法中正確的是( )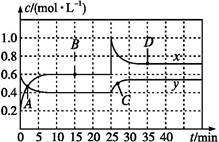
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
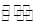 CO2(g)+H2(g) △H<0。
CO2(g)+H2(g) △H<0。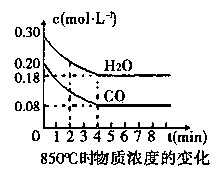
| 時間(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 | |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.與鹽酸反應產生氫氣 |
| B.在氯氣中燃燒 |
| C.放入硝酸汞溶液中表面形成鋁汞齊 |
| D.一定溫度下,用鋁與氧化鈣反應制得金屬鈣 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
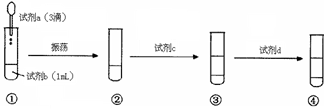
| A.試劑a是0.1mol·L–1KI溶液 |
| B.試劑d是KSCN溶液 |
| C.說明該反應已經發生的理由是③的下層呈紫色 |
| D.說明該反應是有限度的實驗現象是④的上層溶液出現血紅色 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO3(g) + 197 kJ實驗測得有關數據如下:
2SO3(g) + 197 kJ實驗測得有關數據如下:| 容器編號 | 起始時各物質的物質的量 / mol | 達到平衡時體系能量的變化/KJ | ||
| SO2 | O2 | SO3 | ||
| 甲 | 2 | 1 | 0 | 放出熱量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 放出熱量:Q2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com