
 (1)同一物質存在氣態的熵值最大,液態的熵值次之,固態的熵值最小.若同溫同壓下,一個反應生成物氣體的體積等于反應物氣體的體積就可粗略認為該反應的熵變為0.某化學興趣小組,專門研究了氧族元素及其某些化學物的部分性質.所查資料如下:
(1)同一物質存在氣態的熵值最大,液態的熵值次之,固態的熵值最小.若同溫同壓下,一個反應生成物氣體的體積等于反應物氣體的體積就可粗略認為該反應的熵變為0.某化學興趣小組,專門研究了氧族元素及其某些化學物的部分性質.所查資料如下:分析 (1)從圖象獲取反應熱的信息;
(2)氫氧根離子先與氫離子反應,再與鋁離子反應,然后與銨根離子反應,最后與Al(OH)3反應;
(3)析出沉淀時,AgCl溶液中c(Ag+)=$\frac{Ksp(AgCl)}{c(C{l}^{-})}$,AgBr溶液中c(Ag+)=$\frac{Ksp(AgBr)}{c(B{r}^{-})}$,Ag2CrO4溶液中c(Ag+)=$\sqrt{\frac{Ksp(A{g}_{2}Cr{O}_{4})}{c(Cr{{O}_{4}}^{2-})}}$,c(Ag+)越小,先生成沉淀;
(4)依據電離平衡常數判斷出的酸性H2CO3 >HClO>HCO3-;依據酸性強弱分析反應產物.
解答 解:(1)從圖象可知,S與H2的△H<0,Te和H2反應的△H>0,且反應的熵變約為0,不能自發進行,
故答案為:放出;由圖可知Te和H2反應的是吸熱反應,即△H>0,熵變約為0,所以該反應不自發;
(2)氫氧根離子先與氫離子反應①H++OH-═H2O,再與鋁離子反應②Al3++3OH-═Al(OH)3↓,再與銨根離子反應③NH4++OH-═NH3•H2O,最后與Al(OH)3反應④Al(OH)3+OH-═AlO2-+2H2O,
故答案為:Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-═AlO2-+2H2O;
(3)AgCl溶液中c(Ag+)=$\frac{Ksp(AgCl)}{c(C{l}^{-})}$=$\frac{1.56×1{0}^{-10}}{0.01}$mol/L=1.56×10-8mol/L,AgBr溶液中c(Ag+)=$\frac{Ksp(AgBr)}{c(B{r}^{-})}$=$\frac{7.7×1{0}^{-13}}{0.01}$mol/L=7.7×10-11mol/L,Ag2CrO4溶液中c(Ag+)=$\sqrt{\frac{Ksp(A{g}_{2}Cr{O}_{4})}{c(Cr{{O}_{4}}^{2-})}}$=$\sqrt{\frac{9.0×1{0}^{-12}}{0.01}}$mol/L=3×10-5,c(Ag+)越小,則越先生成沉淀,所以種陰離子產生沉淀的先后順序為Br-、Cl-、CrO42-;
故答案為:Br-、Cl-、CrO42-.
(4)①將少量的氯氣通入到過量的碳酸鈉溶液中,氯氣和水反應生成的鹽酸反應生成碳酸氫鈉,次氯酸酸性強于碳酸氫根離子,反應生成碳酸氫鈉,反應的離子方程式為:Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO-,
故答案為:Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO-;
②氯氣和碳酸鈉按照1:1的比例恰好反應,生成的鹽酸恰好和碳酸鈉反應生成碳酸氫鈉,次氯酸不參與反應,反應的離子方程式為:Cl2+CO32-+H2O═HCO3-+Cl-+HClO,
故答案為:Cl2+CO32-+H2O═HCO3-+Cl-+HClO.
點評 本題考查反應的自發性、離子方程式的書寫、難溶電解質的溶解平衡問題等知識點.注意碘和氫氣的反應特點及等效平衡的應用,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 強電解質溶液的導電能力一定比弱電解質溶液強 | |
| B. | 因醋酸是弱電解質,鹽酸是強電解質,因而中和等體積、等物質的量濃度的醋酸和鹽酸時,鹽酸消耗的NaOH比醋酸多 | |
| C. | NaHCO3溶于水,溶液中存在電離平衡 | |
| D. | 物質的量濃度相同的磷酸鈉溶液和磷酸溶液中C(PO43-)相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Mg | B. | Mg | C. | $\frac{M}{6.02×1{0}^{23}}$g | D. | Mg |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 碳是形成物種最多的元素之一,許多含碳物質對人類極其重要.
碳是形成物種最多的元素之一,許多含碳物質對人類極其重要.| 時間/min | 0 | 10 | 20 | 30 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鍋爐水垢中的CaSO4經飽和碳酸鈉溶液浸泡可轉化為CaCO3 | |
| B. | 常溫下,在含有Ag+和Cl-的溶液中,Ag+和Cl-濃度之積是個常數 | |
| C. | 當醋酸達到電離平衡后,改變某條件電離平衡向正反應方向移動,則溶液的導電能力一定變強 | |
| D. | 將濃度為0.1 mol/L的HF溶液加水不斷稀釋,溶液$\frac{c({F}^{-})}{c({H}^{+})}$始終保持增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 0min | 5min | 10min | |
| CO | 0.01 | 0.0056 | |
| H2O | 0.01 | 0.0156 | |
| CO2 | 0 | 0.0044 | |
| H2 | 0 | 0.0044 |
| A. | 0~5min 時用H2O(g)表示的平均反應速率為1.2×10-3 mol/( L.min) | |
| B. | 5min~10min 改變的條件是再加入了0.1mol H2O(g) | |
| C. | 200℃時,若向容器中充入0.01mol CO(g)、0.01mol H2O(g)、0.01molCO2(g)、0.01molH2(g),達平衡時,CO(g)為1.2×10-3mol/L | |
| D. | 300℃時,若向容器中充入0.01mol CO(g)、0.01mol H2O(g)、0.02molCO2(g)、0.02molH2(g),則開始反應時ν(正)<ν(逆) |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 常溫下,向含有AgCl固體的飽和溶液,加少量水稀釋,c(Ag+)和Ksp(AgCl)均保持不變 | |
| B. | pH=5的CH3COOH與CH3COONa的混合溶液中:c(Na+)>c(CH3COO-) | |
| C. | 將0.2mol/LCH3COOH溶液和0.1mol/LNaOH溶液等體積混合,則反應后的混合溶液中:2c(OH-)+c(CH3COO-)=2c(H+)+c(CH3COOH) | |
| D. | 將水加熱煮沸,能促進水的電離,Kw增大,pH增大,溶液呈堿性 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
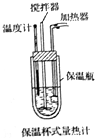 化學反應過程中總是伴隨著能量的變化,能量間可以相互轉化.
化學反應過程中總是伴隨著能量的變化,能量間可以相互轉化.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
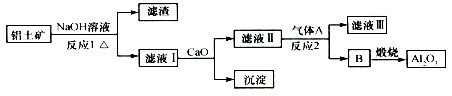
| A. | 氣體A一定為HCl | B. | 濾液Ⅰ中溶質可能含NaAlO2 | ||
| C. | 沉淀的主要成分不是硅酸鈣 | D. | 反應1、反應2均是氧化還原反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com