
【題目】甲醇是一種新型的汽車動力燃料。請回答下列問題:
(1)工業上可通過CO和H2化合來制備CH3OH(g)。已知某些化學鍵的鍵能數據如下表:
化學鍵 | C-C | C-H | H-H | C-O |
| H-O |
鍵能/kJmol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
已知:CO中的C與O之間形成的化學鍵為![]() 鍵。工業制備甲醇的熱化學方程式__________________;
鍵。工業制備甲醇的熱化學方程式__________________;
(2)在容積固定為2L的密閉容器內充入1molCO和2molH2,加入合適的催化劑(體積可以忽略不計)后,在250℃下開始反應,并用壓力計檢測容器內壓強的變化如下:
反應時間/min | 0 | 5 | 10 | 15 | 20 | 25 |
壓強/MPa | 10.8 | 9.6 | 8.4 | 7.8 | 7.2 | 7.2 |
則從反應開始到20min時,以CO表示的平均反應速率為___________,該溫度下平衡常數K= ______;若升高溫度,則CO的轉化率_______(填“增大”“減小”或“不變”);
(3)在三個容積均為1 L的恒容密閉容器中只發生反應:2CH3OH(g) ![]() C2H4(g)+2H2O(g),依據表中的相關數據可確定該反應的ΔH______0(填“>”“<”或“=”,下同);容器C達到平衡時,容器中總壓強p(C)/p(A)_______2;容器A達到平衡時,向容器中再充入CH3OH(g)、C2H4(g)、H2O(g)各0.1 mol,此時,υ(正)_______υ(逆)。
C2H4(g)+2H2O(g),依據表中的相關數據可確定該反應的ΔH______0(填“>”“<”或“=”,下同);容器C達到平衡時,容器中總壓強p(C)/p(A)_______2;容器A達到平衡時,向容器中再充入CH3OH(g)、C2H4(g)、H2O(g)各0.1 mol,此時,υ(正)_______υ(逆)。
容器 | 溫度/℃ | 起始加入量/mol | 平衡時乙烯/mol | ||
CH3OH(g) | C2H4(g) | H2O(g) | |||
A | 310 | 0.2 | 0 | 0 | 0.05 |
B | 327 | 0 | 0.1 | 0.2 | 0.047 |
C | 310 | 0.2 | 0.1 | 0.2 | / |
【答案】CO(g)+2H2(g)![]() CH3OH(g) ΔH=-116 kJmol-1 0.0125molL-1min-1 4 減小 < < <
CH3OH(g) ΔH=-116 kJmol-1 0.0125molL-1min-1 4 減小 < < <
【解析】
(1)依據△H=反應物鍵能總和-生成物鍵能總和計算ΔH,再寫出熱化學方程式;
(2)通過(1)寫出的熱化學方程式可知反應是氣體體積減小的放熱反應,當反應進行到20min時反應達到平衡狀態,依據反應速率概念υ= ![]() 計算速率,平衡常數是利用平衡狀態下生成物濃度冪次方乘積除以反應物濃度的冪次方乘積得到;結合溫度對平衡的影響分析判斷;
計算速率,平衡常數是利用平衡狀態下生成物濃度冪次方乘積除以反應物濃度的冪次方乘積得到;結合溫度對平衡的影響分析判斷;
(3)根據2CH3OH(g) ![]() C2H4(g)+2H2O(g),A、B起始充入的物質等效,根據容器A、B結合溫度對平衡的影響分析判斷;容器C中起始時氣體的物質的量相當于A的2倍,根據壓強對平衡的影響分析判斷;根據三段式計算A容器的平衡常數K,容器A達到平衡時,向容器中再充入CH3OH(g)、C2H4(g)、H2O(g)各0.1 mol,計算出Qc,根據Qc與K的大小分析判斷。
C2H4(g)+2H2O(g),A、B起始充入的物質等效,根據容器A、B結合溫度對平衡的影響分析判斷;容器C中起始時氣體的物質的量相當于A的2倍,根據壓強對平衡的影響分析判斷;根據三段式計算A容器的平衡常數K,容器A達到平衡時,向容器中再充入CH3OH(g)、C2H4(g)、H2O(g)各0.1 mol,計算出Qc,根據Qc與K的大小分析判斷。
(1)CO(g)+2H2(g)![]() CH3OH(g),反應的△H=反應物總鍵能之和-生成物總鍵能之和,依據圖表提供的化學鍵的鍵能,△H═1072kJ/mol+2×436kJ/mol-(3×413kJ/mol +358kJ/mol+ 463kJ/mol) =-116kJmol-1,故答案為:CO(g)+2H2(g)
CH3OH(g),反應的△H=反應物總鍵能之和-生成物總鍵能之和,依據圖表提供的化學鍵的鍵能,△H═1072kJ/mol+2×436kJ/mol-(3×413kJ/mol +358kJ/mol+ 463kJ/mol) =-116kJmol-1,故答案為:CO(g)+2H2(g) ![]() CH3OH(g) ΔH=-116 kJmol-1;
CH3OH(g) ΔH=-116 kJmol-1;
(2)從反應開始到20min時,設CO的濃度變化量是x,
CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
初始濃度(mol/L):0.5 1 0
變化濃度(mol/L): x 2x x
平衡濃度(mol/L):0.5-x 1-2x x
根據反應前后壓強之比等于物質的量之比,則![]() =
=![]() ,解得x=0.25mol/L,從反應開始到20min時,以CO表示的平均反應速率υ(CO)=
,解得x=0.25mol/L,從反應開始到20min時,以CO表示的平均反應速率υ(CO)=![]() =
=![]() =0.0125mol/(Lmin);平衡常數K=
=0.0125mol/(Lmin);平衡常數K= =
=![]() =4;該反應為放熱反應,溫度升高,平衡逆向移動,CO的轉化率減小,故答案為:0.0125mol/(Lmin);4;減小;
=4;該反應為放熱反應,溫度升高,平衡逆向移動,CO的轉化率減小,故答案為:0.0125mol/(Lmin);4;減小;
(3)根據2CH3OH(g) ![]() C2H4(g)+2H2O(g),A、B起始充入的物質等效,比較容器A、B可知,升高溫度,平衡時乙烯的量減少,說明升高溫度平衡逆向移動,因此正反應為放熱反應,即△H<0;容器C中起始時氣體的物質的量相當于A的2倍,若平衡等效,在體積相同時,平衡壓強應該為A的2倍,但增大壓強,平衡逆向移動,氣體的物質的量減少,因此平衡時容器中總壓強p(C)/p(A)<2;對于A容器,
C2H4(g)+2H2O(g),A、B起始充入的物質等效,比較容器A、B可知,升高溫度,平衡時乙烯的量減少,說明升高溫度平衡逆向移動,因此正反應為放熱反應,即△H<0;容器C中起始時氣體的物質的量相當于A的2倍,若平衡等效,在體積相同時,平衡壓強應該為A的2倍,但增大壓強,平衡逆向移動,氣體的物質的量減少,因此平衡時容器中總壓強p(C)/p(A)<2;對于A容器,
2CH3OH(g) ![]() C2H4(g)+2H2O(g),
C2H4(g)+2H2O(g),
初始濃度(mol/L):0.2 0 0
變化濃度(mol/L):0.1 0.05 0.1
平衡濃度(mol/L):0.1 0.05 0.1
平衡常數K=![]() =0.05,容器A達到平衡時,向容器中再充入CH3OH(g)、C2H4(g)、H2O(g)各0.1 mol,此時Qc=
=0.05,容器A達到平衡時,向容器中再充入CH3OH(g)、C2H4(g)、H2O(g)各0.1 mol,此時Qc=![]() =0.1>K,平衡逆向移動,說明υ(正)<υ(逆),故答案為:<;<;<。
=0.1>K,平衡逆向移動,說明υ(正)<υ(逆),故答案為:<;<;<。


科目:高中化學 來源: 題型:
【題目】B. [實驗化學]
次硫酸氫鈉甲醛(NaHSO2·HCHO·2H2O)在印染、醫藥以及原子能工業中應用廣泛。以Na2SO3、SO2、HCHO 和鋅粉為原料制備次硫酸氫鈉甲醛的實驗步驟如下:
步驟1:在燒瓶中(裝置如圖 所示) 加入一定量Na2SO3和水,攪拌溶解,緩慢通入SO2,至溶液pH 約為4,制得NaHSO3溶液。步驟2:將裝置A 中導氣管換成橡皮塞。向燒瓶中加入稍過量的鋅粉和一定量甲醛溶液,在80 ~ 90益下,反應約3h,冷卻至室溫,抽濾。步驟3:將濾液真空蒸發濃縮,冷卻結晶。
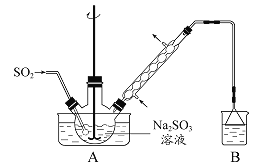
(1)裝置B 的燒杯中應加入的溶液是 。
(2)①步驟2 中,反應生成的Zn(OH)2會覆蓋在鋅粉表面阻止反應進行,防止該現象發生的措施是
。②冷凝管中回流的主要物質除H2O 外還有 (填化學式)。
(3)①抽濾裝置所包含的儀器除減壓系統外還有 、 (填儀器名稱)。②濾渣的主要成分有 、 (填化學式)。
(4)次硫酸氫鈉甲醛具有強還原性,且在120益以上發生分解。步驟3 中不在敞口容器中蒸發濃縮的原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列操作中,完全正確的一組是
①用試管夾夾持試管時,試管夾從試管底部往上套,夾在試管的中上部
②給盛有液體的體積超過![]() 容積的試管加熱
容積的試管加熱
③把鼻孔靠近容器口去聞氣體的氣味
④將試管平放,用紙槽往試管里送入固體粉末后,然后豎立試管
⑤加熱坩堝要墊上石棉網
⑥將燒瓶放在桌上,用力塞緊塞子
⑦用坩堝鉗夾取加熱后的蒸發皿
⑧將滴管豎直伸入試管內滴加液體
⑨稀釋濃硫酸時,應沿器壁緩緩地將水加入濃硫酸中
⑩用鑷子從煤油中取出金屬鈉,再用小刀切一小塊,然后將剩下的鈉放回原瓶
A.①④⑦⑩B.①④⑤⑦⑩C.①④⑤⑦⑧⑩D.④⑤⑦⑩
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式中,正確的是
A.侯氏制堿法:NH3+CO2+H2O=![]() +
+ ![]()
B.小蘇打溶液與稀硫酸混合:![]() +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
C.向Ba(OH)2溶液中加少量NaHCO3: ![]() +Ba2++OH-=BaCO3↓+H2O
+Ba2++OH-=BaCO3↓+H2O
D.硫酸亞鐵溶液與過氧化氫溶液混合:Fe2++2H2O2+4H+=Fe3++4H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 相對分子質量為72的某烷烴,一氯代物有8種
B. 聚合物![]() 可由單體CH2=CHCH3CH=CH2加聚制得
可由單體CH2=CHCH3CH=CH2加聚制得
C. CH3CH(OH)CH(CH3)2的名稱為2-甲基-3-丁醇
D. 植物油氫化、塑料和橡膠的老化過程中均發生了加成反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅的化合物有很多,其中Cu2S、Cu2O、CuCl都是用途非常廣泛的一價銅的化合物。回答下列問題:
(1)已知:2Cu(s)+O2(g)=2CuO(s) ΔH1=-314 kJmol-1
4CuO(s)=2 Cu2O(s)+ O2(g) ΔH2=+292 kJmol-1
固相法制備Cu2O的反應CuO(s)+ Cu(s)=Cu2O(s)的ΔH=________
(2)輝銅礦(主要成分為Cu2S)經火法冶煉,可制得Cu和H2SO4,流程如下圖所示:Ⅱ中,電解法精煉粗銅(含少量Ag、Fe),CuSO4溶液做電解質溶液:
① 粗銅應與直流電源的_____ 極(填“正”或 “負”)相連。
② 銅在陰極析出,而鐵以離子形式留在電解質溶液里的原因是________ 。
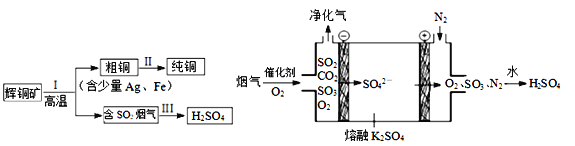
(3)Ⅲ中,煙氣(主要含SO2、CO2)在較高溫度經上右圖所示方法脫除SO2,并制得H2SO4,在陽極生成SO3的電極反應式是____________________________。
(4)反應2CuCl(s) + Hg22+(aq) ![]() Hg2Cl2(s) +2Cu+(aq)達到平衡時,平衡常數K≈_____(保留兩位有效數字)。[已知Ksp(CuCl)=1.2×10-6、Ksp (Hg2Cl2)=1.3×10-10]
Hg2Cl2(s) +2Cu+(aq)達到平衡時,平衡常數K≈_____(保留兩位有效數字)。[已知Ksp(CuCl)=1.2×10-6、Ksp (Hg2Cl2)=1.3×10-10]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組研究亞硝酸鈉,查閱下列資料,試根據信息回答下列問題。
藥品 | NaNO2 (亞硝酸鈉) |
性質 | 1.在酸性溶液中有較強氧化性,能將Fe2+ 氧化成Fe3+ ; 2.AgNO2是一種難溶于水、易溶于酸的鹽。 |
(1)已知NaNO2能發生如下反應:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。請用雙線橋表示電子轉移的方向和數目:___。
(2)誤食NaNO2會導致血紅蛋白中的Fe2+轉化為Fe3+ 而中毒,可服用維生素C 解毒。下列分析錯誤的是__(填序號)。
A.NaNO2被還原 B.維生素C具有還原性
C.還原性:維生素C>Fe2+ D.NaNO2是還原劑
(3)下列方法中,可用來區分NaNO2和NaCl的是___(填序號)。
A.焰色反應 B.分別滴加酸化FeSO4溶液和KSCN溶液
C.在酸性條件下加入KI 淀粉溶液 D.分別滴加AgNO3溶液
(4)某同學把新制的氯水加到NaNO2溶液中,觀察到氯水褪色,同時生成NaNO3和HCl,請寫出反應的離子方程式:___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】香豆素是用途廣泛的香料,合成香豆素的路線如下(其他試劑、產物及反應條件均省略):
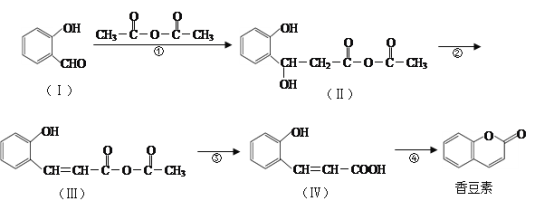
(1)Ⅰ的分子式為_____________;Ⅰ與H2反應生成鄰羥基苯甲醇,鄰羥基苯甲醇的結構簡式為______________________________________________________。
(2)反應②的反應類型是____________,反應④的反應類型是___________________。
(3)香豆素在過量NaOH溶液中完全水解的化學方程式為:_____________________________________________________________________。
(4)Ⅴ是Ⅳ的同分異構體,Ⅴ的分子中含有苯環且無碳碳雙鍵,苯環上含有兩個鄰位取代基,能發生銀鏡反應。Ⅴ的結構簡式為_______________(任寫一種)。
(5)一定條件下,![]() 與CH3CHO能發生類似反應①、②的兩步反應,最終生成的有機物的結構簡式為_____________。
與CH3CHO能發生類似反應①、②的兩步反應,最終生成的有機物的結構簡式為_____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com