
碳酸鈉(Na2CO3)俗稱純堿,是一種重要的基礎化工原料,廣泛應用于玻璃、造紙等工業。下列與碳酸鈉有關的說法正確的是:
| A.Na2CO3的穩定性介于Na2CO3·10H2O和NaHCO3之間 |
| B.“侯氏制堿法”制得的堿是指NaHCO3 |
| C.可用鹽酸鑒別Na2CO3和NaHCO3固體 |
| D.純堿有時可代替燒堿使用,比如溶解石英、促進乙酸乙酯的水解等 |
C
解析試題分析:A Na2CO3·10H2O加熱失去結晶水。NaHCO3之受熱分解:2NaHCO3=Na2CO3+CO2↑+H2O。所以Na2CO3的穩定性最強。錯誤。B“侯氏制堿法”制得的堿是指Na2CO3,錯誤。C鹽酸和Na2CO3 . 首先反應產生NaHCO3和氯化鈉,然后是第一步產生的NaHCO3和鹽酸繼續反應產生氯化鈉、二氧化碳、水。而NaHCO3和鹽酸直接反應放出二氧化碳氣體。二者現象不同,故可用鹽酸鑒別Na2CO3和NaHCO3固體。正確。D.在常溫下純堿與石英不反應,而氫氧化鈉與石英能發生反應,故常溫下不能用來溶解石英;乙酸乙酯在碳酸鈉溶液的的溶解度很小,不能促進其水解等。故這時不能用純堿有時可代替燒堿使用。錯誤。
考點:考查侯氏制堿法及Na2CO3和NaHCO3的性質、用途等的知識。


 黎明文化寒假作業系列答案
黎明文化寒假作業系列答案科目:高中化學 來源: 題型:單選題
120 mL含有0.20 mol碳酸鈉溶液和200 mL鹽酸,不管將前者滴加入后者,還是將后者滴加入前者,都有氣體產生,但最終生成的氣體體積不同,則鹽酸的濃度合理的是
| A.2.0mol/L | B.1.5 mol/L | C.0.18 mol/L | D.0.24mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列敘述正確的是
| A.將FeCl3溶液加熱蒸干得到FeCl3固體 |
| B.向Fe(NO3)2溶液中加少量鹽酸,無明顯現象 |
| C.向氫氧化鎂懸濁液中滴加FeCl3溶液,無明顯現象 |
| D.向FeSO4溶液中滴加NaOH溶液,先出現白色沉淀,最終沉淀轉化成紅褐色 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一些不法商人在面粉生產中添加過氧化鈣(CaO2)等添加劑對食品進行增白。下列關于過氧化鈣(CaO2)的敘述正確的是
| A.CaO2中陰、陽離子的個數比為1:1 |
| B.CaO2對面粉增白原理與SO2漂白原理相似 |
| C.CaO2和水反應時,每產生1 molO2轉移電子4 mol |
| D.CaO2放入NaHCO3溶液中,會放出二氧化碳,并產生白色渾濁 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
4.6g鈉投入100g水中,下列敘述錯誤的是
| A.鈉浮在水面,熔化成銀色光亮的小球 | B.鈉貯存在煤油中 |
| C.所得溶液的質量分數為4.4﹪ | D.該反應中轉移0.2mole- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列實驗方案中,不能測定Na2CO3和NaHCO3,混合物中Na2CO3質量分數的是
| A.取a克混合物與足量稀硫酸充分反應,逸出氣體用堿石灰吸收,增重b克 |
| B.取a克混合物與足量稀鹽酸充分反應,加熱、蒸干、灼燒,得b克固體 |
| C.取a克混合物充分加熱,得b克固體 |
| D.取a克混合物與足量Ca(OH)2溶液充分反應,過濾、洗滌、烘干,得b克固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
Al、Cu都是重要的金屬元素。下列說法正確的是
| A.兩者對應的氧化物均為堿性氧化物 |
| B.兩者的單質都能與稀硫酸反應產生氫氣 |
| C.常溫條件下,兩種金屬都能溶解于濃硝酸中 |
| D.用惰性電極電解AlCl3、CuCl2的水溶液均可得到氯氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業上用含有鋁、鐵、銅的廢棄合金為主要原料制取硫酸鋁溶液、硝酸銅晶體和無水氯化鐵,其生產流程如下圖所示。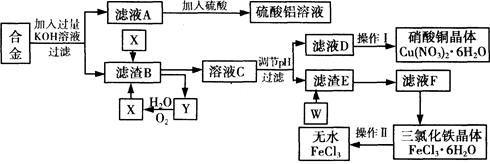
已知:調節適當PH范圍可使Fe3+沉淀完全而Cu2+不會沉淀。
請回答下列問題:
(1)寫出向合金中加入KOH溶液后所發生反應的離子方程式: 。
(2)在濾液A中直接加入硫酸后所得到的硫酸鋁溶液中除含少量硫酸外,還一定含有的雜質是
(填化學式)。
請設計一個更合理的實驗方案由濾液A制備純凈的硫酸鋁溶液,仿照上圖形式畫出制備流程圖(提示:在箭頭上下方標出所用試劑和實驗操作) 。
(3) 寫出試劑X的名稱 。
(4) 實驗操作I的順序依次為 (選填序號)。
| A.蒸餾 | B.蒸發濃縮 | C.過濾 | D.冷卻結晶 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)下列框圖中的字母分別代表一種常見的物質或其溶液,相互之間的轉化關系如下圖所示(部分產物及反應條件已略去)。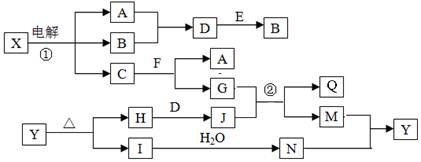
已知A、B為氣態單質,F是地殼中含量最多的金屬元素的單質:E、H、I為氧化物,E為黑色固體,H為紅棕色粉末,I為紅棕色氣體;M為紅褐色沉淀,Q為白色膠狀物質。
請回答下列問題:
(1)組成單質F的元素在周期表中的位置是______;C中存在的化學鍵類型為____;E的化學式是___。
(2)A在B中燃燒的現象是_______ 。
(3) D+E→B的反應中,被氧化與被還原的物質的物質的量之比是_______。
(4)反應①的化學方程式為___________________________________ 。
(5)反應②的離子方程式為___________________________________。
(6)Y受熱分解可生成H、I和氧氣,.寫出該反應的化學方程式:______________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com