
【題目】X、Y、Z、P、Q、W、R、T是元素周期表短期中最常見的主族元素,且原子序數依次增大,其相關信息如下表:
元素 | 相關信息 |
X | 其某一種同位素,被用作相對原子質量的標準 |
Y | 其最高價氧化物對應水化物能與其氣態氫化物發生化合反應 |
P | 是短周期中(除稀有氣體外)原子半徑最大的元素 |
Q | 存在質量數為25、中子數為13的核素 |
W | 位于周期表第13列 |
R | 與Z同族, 且最高價氧化物對應水化物的濃溶液常溫下與W 單質會出現鈍化現象 |
(1)W元素位于周期表第________周期______族;T離子的結構示意圖為____________。
(2)將Q、Z、R的簡單離子的半徑從大到小排序___________(用離子符號表示);R、T兩種元素的最高價氧化物對應水化物的酸(或堿)性由強到弱的順序為__________(用化學式表示)。
(3) X、Y、Z三種元素的簡單氫化物中,穩定性最強的化合物的電子式為_________,化合物P2R溶液在空氣中長期放置,會和氧氣反應生成與過氧化鈉的結構相似的物質P2R2,其溶液顯黃色,則P2R2的電子式為______________。
(4)根據下表中的信息,判斷下列化合物固態時的晶體類型(填“離子晶體”……等)。
化合物 | x3Y4 | R2T2 |
主要物理性質 | 硬度可以和金剛石相媲美,熔點>3600℃ | 常溫下是一種橙黃色液體,熔點為-76°C |
晶體類型 | ________ | _________ |
(5)Q的單質能與X、Z形成的某種化合物反應,寫出其化學方程式:______________。
(6)X與Q形成的lmol化合物Q2X3與水反應,生成2molMg(OH)2和1mol某氣態烴,該烴分子中碳氫質量比為9: 1,寫出該氣態烴的結構簡式_______,并寫出Q2X3與水反應的化學方程式________。
【答案】 三 ⅢA 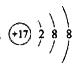 S2->O2->Mg2+ HClO4>H2SO4
S2->O2->Mg2+ HClO4>H2SO4 ![]()
![]() 原子晶體 分子晶體 【答題空10】2Mg+CO2
原子晶體 分子晶體 【答題空10】2Mg+CO2![]() 2MgO+C CH3C≡CH Mg2C3+4H2O=2Mg()+C3H4↑
2MgO+C CH3C≡CH Mg2C3+4H2O=2Mg()+C3H4↑
【解析】元素周期表短周期中的常見主族元素中,X元素的一種同位素可被用作相對原子質量的標準,則X為C元素;Y元素的最高價氧化物對應水化物能與其氣態氫化物相互間發生化合反應,則Y為N元素;P是短周期中(除稀有氣體外)原子半徑最大的元素,則P為Na;Q存在質量數為25,中子數為13的核素,其質子數為25-13=12,則Q為Mg;W位于周期表第13列,原子序數大于Mg,故W為Al;R與Z同族,且最高價氧化物對應水化物的濃溶液常溫下與W單質(Al)會出現鈍化現象,則R為S元素,Z為O元素;T的原子序數最大,則T為Cl;
(1)Al元素的核電荷數為13,位于周期表第三周期ⅢA族;氯元素的核電荷數為17,Cl-的結構示意圖為![]() ;
;
(2)Q、Z、R的簡單離子分別為Mg2+、O2-、S2-,Mg2+、O2-是電子層結構相同的離子,核電荷數越大離子半徑越小,故離子半徑:O2->Mg2+,O2-離子結構比S2-少一個電子層,離子半徑小,則離子半徑的大小關系為:S2->O2->Mg2+;氯的非金屬性比硫強,最高價氧化物對應水化物的酸(或堿)性由強到弱的順序為HClO4>H2SO4;
(3) C、N、O三種元素中氧元素的非金屬性最強,則簡單氫化物中,穩定性最強的化合物為H2O,其電子式為![]() ;化合物Na2S溶液在空氣中長期放置,與氧氣反應會生成Na2S2,與過氧化鈉的結構相似,則Na2S2的電子式為
;化合物Na2S溶液在空氣中長期放置,與氧氣反應會生成Na2S2,與過氧化鈉的結構相似,則Na2S2的電子式為![]() ;
;
(4)X3Y4的熔點高于3600℃,熔點很高,屬于原子晶體,R2T2的熔點為-76℃,熔點很低,屬于分子晶體;
(5)Mg能在CO2中燃燒,生成氧化鎂和碳,其反應化學方程式為2Mg+CO2![]() 2MgO+C;
2MgO+C;
(6)該烴分子中碳氫質量比為9:1,C、H的物質的量之比為=3∶4,根據“碳與鎂生成的1mol化合物Q與水反應生成2mol Mg(OH)2和1mol烴”可知該烴的分子式為C3H4;Q的化學式為Mg2C3,Mg2C3與水反應生成氫氧化鎂和C3H4,結構簡式為CH3C≡CH;反應的化學方程式為Mg2C3+4H2O=2Mg(OH)2+C3H4↑;


科目:高中化學 來源: 題型:
【題目】下表為元素周期表的一部分,用元素符號或化學式回答下列問題。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)10種元素中,化學性質最不活潑的是_________,除⑩外原子半徑最大的是________。
(2)①③⑤三種元素最高價氧化物對應的水化物堿性最強的是__________ ;⑧⑨形成氫化物的穩定性由強到弱順序為_________________。
(3)①②③⑤⑧五種元素形成的離子半徑由大到小的順序為______________________
(4)元素⑥的名稱是____;元素④的原子結構示意圖是/span>_______;元素⑦的氫化物和元素①單質反應的化學方程式為________________。
(5)①⑨形成的化合物灼燒時火焰焰色為________;該化合物的溶液與元素⑧的單質反應的化學方程式為_______________________。
(6)①、⑤和⑧最高價氧化物對應的水化物之間兩兩相互反應的離子方程式為____________________。
(7)元素③的單質在元素⑥⑦形成的某化合物中燃燒的化學方程式為____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已建立化學平衡的某可逆反應,當改變條件使化學平衡向正反應方向移動時,下列有關敘述正確是( )
①生成物的質量分數一定增加
②生成物的產量一定增大
③反應物的轉化率一定增大
④反應物的濃度一定降低
⑤正反應速率一定大于逆反應速率
⑥平衡常數一定增大
A.①② B.③⑤ C.②⑤ D.④⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)反應Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常數為K1
FeO(s)+CO(g) ΔH1,平衡常數為K1
反應Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常數為K2在不同溫度時K1、K2的值如下表:
FeO(s)+H2(g) ΔH2,平衡常數為K2在不同溫度時K1、K2的值如下表:
700 ℃ | 900 ℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
反應CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH,平衡常數K,則ΔH=___________(用ΔH1和ΔH2表示),K=___________(用K1和K2表示),且由上述計算可知,反應CO2(g)+H2(g)
CO(g)+H2O(g) ΔH,平衡常數K,則ΔH=___________(用ΔH1和ΔH2表示),K=___________(用K1和K2表示),且由上述計算可知,反應CO2(g)+H2(g)![]() CO(g)+H2O(g)是________反應(填“吸熱”或“放熱”)。
CO(g)+H2O(g)是________反應(填“吸熱”或“放熱”)。
(2)一定溫度下,向某密閉容器中加入足量鐵粉并充入一定量的CO2氣體,發生反應Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的濃度與時間的關系如圖所示:
FeO(s)+CO(g) ΔH>0,CO2的濃度與時間的關系如圖所示:
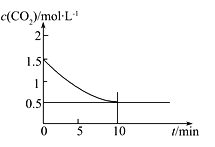
①該條件下反應的平衡常數為___________;若鐵粉足量,CO2的起始濃度為2.0 mol·L-1,則平衡時CO2的濃度為____________mol·L-1。
②下列措施中能使平衡時![]() 增大的是__________(填序號) 。
增大的是__________(填序號) 。
A.升高溫度 B.增大壓強 C.再充入一定量的CO2 D.再加入一定量鐵粉
③一定溫度下,在一個固定容積的密閉容器中發生上述反應,下列能判斷該反應達到化學平衡狀態的是________(填字母)。
a.容器中的壓強不變
b.氣體的密度不再改變
c.v正(CO2)=v逆(CO)
d.c(CO2)=c(CO)
e.容器內氣體總物質的量不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物F是一種最新合成的溶瘤藥物,可通過以下方法合成:

⑴F中所含官能團名稱為_____________。
⑵A→B的反應類型是_____________。
⑶C的結構簡式為_____________。
⑷寫出同時滿足下列條件的![]() 的一種同分異構體G的結構簡式:
的一種同分異構體G的結構簡式:
_____________。
①G分子中有4種不同化學環境的氫;
②G的水解產物均能發生銀鏡反應,其中一種產物還能與FeCl3溶液發生顯色反應。
⑸請寫出以![]() 、(C6H5)3P為原料制備化合物
、(C6H5)3P為原料制備化合物 的合成路線流程圖________(無機試劑任選,合成路線流程圖示例見本題題干)。
的合成路線流程圖________(無機試劑任選,合成路線流程圖示例見本題題干)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于下列圖象及其相關說法正確的是( )
圖①: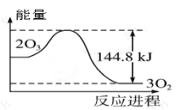 圖②:
圖②: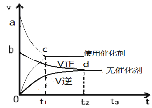
圖③: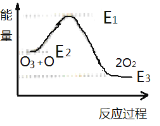 圖④ :
圖④ :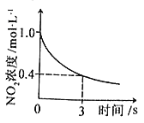
A.據圖①可判斷:2O3(g)=3O2(g);△H= - 44.8KJ/mol
B.據圖②可判斷:某反應在使用催化劑時比無催化劑時反應速率大,且面積Saco>Sbdo
C.據圖③可判斷: 2O2(g)═O3(g)+O(g)△H>0
D.據圖④可判斷:2NO2(g)+O3(g) ![]() N2O5(g)+O2(g),0~3s內,反應速率為V(N2O5)=0.2mol·L-1·S-1
N2O5(g)+O2(g),0~3s內,反應速率為V(N2O5)=0.2mol·L-1·S-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用Cl2生產某些含氯有機物時會產生副產物HCl。利用反應A,可實現氯的循環利用。
反應A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:I.反應A中,4molHCl被氧化,放出115.6kJ熱量。
II.
判斷下列說法正確的是( )
A. 反應A的△H>-115.6kJ·mol-1
B. H2O中H—O鍵比HCl中H—Cl鍵弱
C. 由II中的數據判斷氯元素的非金屬性比氧元素強
D. 斷開1molH—O鍵與斷開1molH—Cl鍵所需能量相差31.9kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將2molSO2和1molO2分別置于相同體積的甲乙兩密閉容器中發生反應2SO2+O2(g)![]() 2SO3(g),并達到平衡。在這過程中,甲容器保持恒溫恒容,乙容器保持恒溫恒壓,達到平衡時,下列說法正確的是( )
2SO3(g),并達到平衡。在這過程中,甲容器保持恒溫恒容,乙容器保持恒溫恒壓,達到平衡時,下列說法正確的是( )
A.達到平衡所需的時間為:甲>乙 B.甲的轉化率>乙的轉化率
C.混合氣體中SO3的含量為:甲>乙 D.氣體的總物質的量:甲<乙
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com