
用硝酸氧化淀粉水解的產物(C6H12O6)可制得少量草酸,裝置如圖A所示(加熱、攪拌和儀器固定裝置均已略去):已知硝酸氧化淀粉水解液過程中可發生下列反應:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
實驗過程如下:
① 將1∶1的淀粉水乳液與少許硫酸(98%)加入燒杯中,
水浴加熱至85℃~90℃,保持30 min,然后逐漸將溫度降至60℃左右;
②將一定量的淀粉水解液加入容器X中;
③控制反應液溫度在55~60℃條件下,邊攪拌邊緩慢滴加一定量含有適量催化劑的混酸(65%HNO3與98%H2SO4的質量比為2:1.5)溶液;
④反應3h左右,冷卻,減壓過濾后再重結晶得草酸晶體。
請回答下列問題:
(1)容器X的名稱: 。
(2)冷凝管水的進口是 (填a或b);冷凝管冷凝回流的主要物質是 。
(3)實驗中若混酸滴加過快,將導致草酸產量下降,其原因是 。
(4)該裝置最大的一個缺點是 。
(5)草酸重結晶的減壓過濾裝置如圖B。儀器Y接在水龍頭上,其作用是 。
減壓過濾的操作有:①將含晶體的溶液倒入漏斗;②將濾紙放入漏斗并用水濕潤;③打開水龍頭;④關閉水龍頭;⑤拆下橡皮管。正確的順序是 。
(6) 將產品在恒溫箱內約90℃以下烘干至恒重,得到二水合草酸。用KMnO4標準溶液滴定,該反應的離子方程式為:
2MnO4-+ 5H2C2O4 + 6H+ = 2Mn2++ 10CO2↑+ 8H2O
稱取該樣品0.12 g,加適量水完全溶解,然后用0.020 mol·L-1
的酸性KMnO4溶液滴定至終點(雜質不參與反應),此時溶液
顏色由 變為 。滴定前后滴定管中的液面讀數如圖所
示,則該草酸晶體樣品中二水合草酸的質量分數為 。
科目:高中化學 來源: 題型:
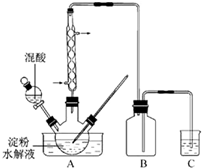 (2011?江蘇)草酸是一種重要的化工產品.實驗室用硝酸氧化淀粉水解液制備草酸的裝置如圖14所示(加熱、攪拌和儀器固定裝置均已略去)
(2011?江蘇)草酸是一種重要的化工產品.實驗室用硝酸氧化淀粉水解液制備草酸的裝置如圖14所示(加熱、攪拌和儀器固定裝置均已略去)查看答案和解析>>
科目:高中化學 來源:2011年普通高等學校招生全國統一考試化學卷(江蘇) 題型:填空題
A.原子序數小于36的X、Y、Z、W四種元素,其中X是形成化合物種最多的元素,Y原子基態時最外層電子數是其內層電子數的2倍,Z原子基態時2p原子軌道上有3個未成對的電子,W的原子序數為29。
回答下列問題:
(1) 分子中Y原子軌道的雜化類型為 ,1mol
分子中Y原子軌道的雜化類型為 ,1mol 含有
含有 鍵的數目為 。
鍵的數目為 。
(2)化合物 的沸點比化合物
的沸點比化合物 的高,其主要原因是
的高,其主要原因是  。
。
(3)元素Y的一種氧化物與元素Z的一種氧化物互為等電子體,元素Z的這種氧化物的分子式是 。
(4)元素W的一種氯化物晶體的晶胞結構如圖13所示,該氯化物的化學式是 ,它可與濃鹽酸發生非氧化還原反應,生成配合物 ,反應的化學方程式為 。
,反應的化學方程式為 。
B.草酸是一種重要的化工產品。實驗室用硝酸氧化淀粉水解液制備草酸的裝置如圖14所示(加熱、攪拌和儀器固定裝置均已略去)
實驗過程如下:
①將一定量的淀粉水解液加入三頸瓶中
②控制反應液溫度在55~60℃條件下,邊攪拌邊緩慢滴加一定量含有適量催化劑的混酸(65%HNO3與98%H2SO4的質量比為2:1.5)溶液
③反應3h左右,冷卻,抽濾后再重結晶得草酸晶體。
硝酸氧化淀粉水解液過程中可發生下列反應:
C6H12O6+12HNO3 →3H2C2O4+9NO2↑ +3NO↑ +9H2O
C6H12O6+8HNO3 →6CO2+8NO↑ +10H2O
3H2C2O4+2HNO3 →6CO2+2NO↑ +4H2O
(1)檢驗淀粉是否水解完全所需用的試劑為
(2)實驗中若混酸滴加過快,將導致草酸產率下降,其原因是
(3)裝置C用于尾氣吸收,當尾氣中n(NO2):n(NO)=1:1時,過量的NaOH溶液能將NO,全部吸收,原因是 (用化學方程式表示)
(4)與用NaOH溶液吸收尾氣相比較,若用淀粉水解液吸收尾氣,其優、缺點是 。
(5)草酸重結晶的減壓過濾操作中,除燒杯、玻璃棒外,還必須使用屬于硅酸鹽材料的儀器有 。
查看答案和解析>>
科目:高中化學 來源:2012屆浙江省衢州二中高三下學期第一次綜合練習理科綜合試卷(化學部分) 題型:實驗題
用硝酸氧化淀粉水解的產物(C6H12O6)可制得少量草酸,裝置如圖A所示(加熱、攪拌和儀器固定裝置均已略去):已知硝酸氧化淀粉水解液過程中可發生下列反應:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
實驗過程如下:
將1∶1的淀粉水乳液與少許硫酸(98%)加入燒杯中,
水浴加熱至85℃~90℃,保持30 min,然后逐漸將溫度降至60℃左右;
②將一定量的淀粉水解液加入容器X中;
③控制反應液溫度在55~60℃條件下,邊攪拌邊緩慢滴加一定量含有適量催化劑的混酸(65%HNO3與98%H2SO4的質量比為2:1.5)溶液;
④反應3h左右,冷卻,減壓過濾后再重結晶得草酸晶體。
請回答下列問題:
(1)容器X的名稱: 。
(2)冷凝管水的進口是 (填a或b);冷凝管冷凝回流的主要物質是 。
(3)實驗中若混酸滴加過快,將導致草酸產量下降,其原因是 。
(4)該裝置最大的一個缺點是 。
(5)草酸重結晶的減壓過濾裝置如圖B。儀器Y接在水龍頭上,其作用是 。
減壓過濾的操作有:①將含晶體的溶液倒入漏斗;②將濾紙放入漏斗并用水濕潤;③打開水龍頭;④關閉水龍頭;⑤拆下橡皮管。正確的順序是 。
(6) 將產品在恒溫箱內約90℃以下烘干至恒重,得到二水合草酸。用KMnO4標準溶液滴定,該反應的離子方程式為:
2MnO4-+ 5H2C2O4 + 6H+ = 2Mn2++ 10CO2↑+ 8H2O
稱取該樣品0.12 g,加適量水完全溶解,然后用0.020 mol·L-1
的酸性KMnO4溶液滴定至終點(雜質不參與反應),此時溶液
顏色由 變為 。滴定前后滴定管中的液面讀數如圖所
示,則該草酸晶體樣品中二水合草酸的質量分數為 。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年浙江省高三下學期第一次綜合練習理科綜合試卷(化學部分) 題型:實驗題
用硝酸氧化淀粉水解的產物(C6H12O6)可制得少量草酸,裝置如圖A所示(加熱、攪拌和儀器固定裝置均已略去):已知硝酸氧化淀粉水解液過程中可發生下列反應:
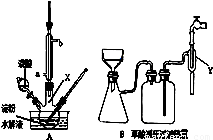
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
實驗過程如下:
① 將1∶1的淀粉水乳液與少許硫酸(98%)加入燒杯中,
水浴加熱至85℃~90℃,保持30 min,然后逐漸將溫度降至60℃左右;
②將一定量的淀粉水解液加入容器X中;
③控制反應液溫度在55~60℃條件下,邊攪拌邊緩慢滴加一定量含有適量催化劑的混酸(65%HNO3與98%H2SO4的質量比為2:1.5)溶液;
④反應3h左右,冷卻,減壓過濾后再重結晶得草酸晶體。
請回答下列問題:
(1)容器X的名稱: 。
(2)冷凝管水的進口是 (填a或b);冷凝管冷凝回流的主要物質是 。
(3)實驗中若混酸滴加過快,將導致草酸產量下降,其原因是 。
(4)該裝置最大的一個缺點是 。
(5)草酸重結晶的減壓過濾裝置如圖B。儀器Y接在水龍頭上,其作用是 。
減壓過濾的操作有:①將含晶體的溶液倒入漏斗;②將濾紙放入漏斗并用水濕潤;③打開水龍頭;④關閉水龍頭;⑤拆下橡皮管。正確的順序是 。
(6) 將產品在恒溫箱內約90℃以下烘干至恒重,得到二水合草酸。用KMnO4標準溶液滴定,該反應的離子方程式為:
2MnO4-+ 5H2C2O4 + 6H+ = 2Mn2+ + 10CO2↑+ 8H2O
稱取該樣品0.12 g,加適量水完全溶解,然后用0.020 mol·L-1
的酸性KMnO4溶液滴定至終點(雜質不參與反應),此時溶液
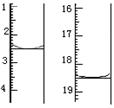
顏色由 變為 。滴定前后滴定管中的液面讀數如圖所
示,則該草酸晶體樣品中二水合草酸的質量分數為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com